Clear Sky Science · ru
Моделирование на основе структуры раскрывает молекулярную основу новой активности CYP153A6 по отношению к производным толуола
Передача сложных химических задач природе
Химики и промышленность полагаются на реакции, которые вводят кислород в стойкие связи углерод–водород — например, чтобы очищать загрязнения или синтезировать компоненты для лекарств и ароматов. Выполнить это чисто, без агрессивных реагентов и тяжелого металлического отхода, трудно. В этом исследовании рассматривается природный катализатор, фермент CYP153A6 из почвенной бактерии, и ставится простой, но важный вопрос: можно ли направить этот фермент так, чтобы он селективно «модернизировал» соединения типа толуола — распространенные компоненты топлива и растворителей — в более полезные и экологичные продукты?
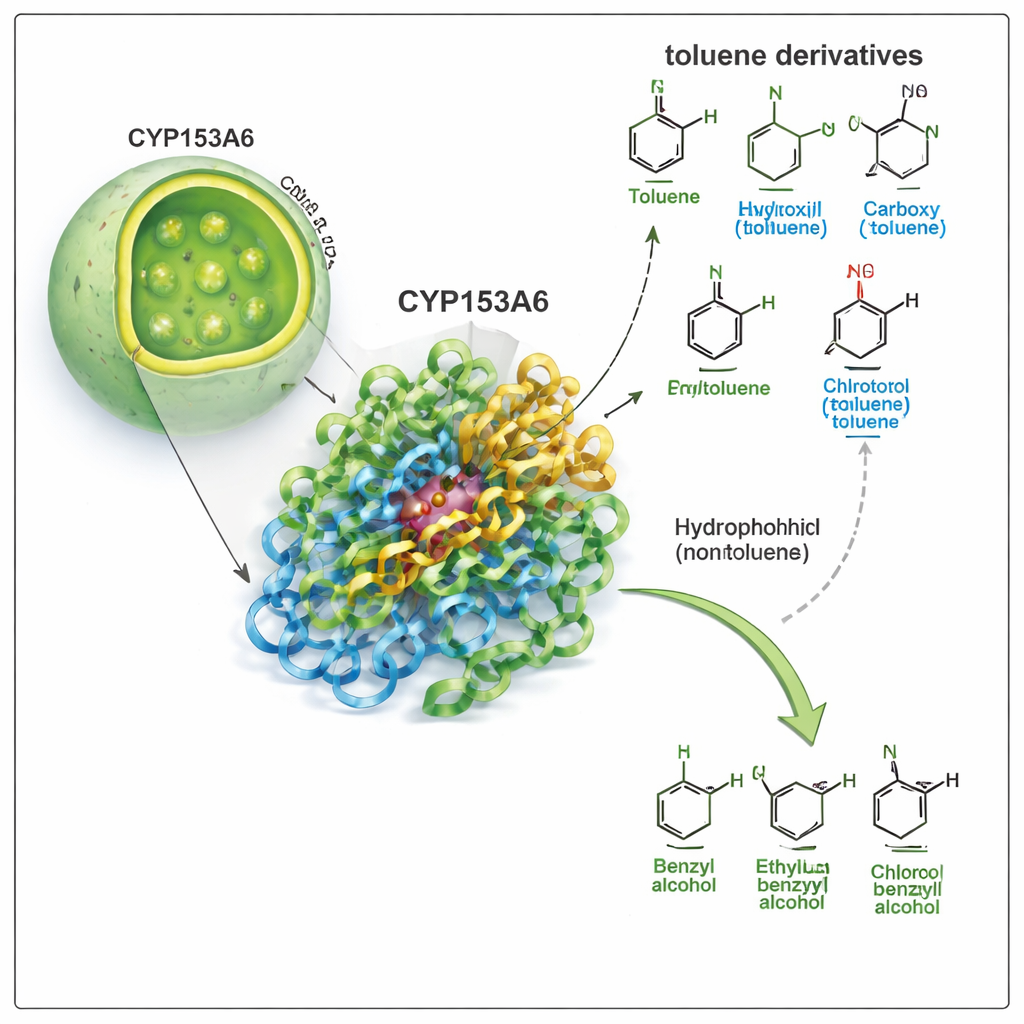
Фермент, выбирающий одно конкретное место
CYP153A6 относится к большой семье цитохромов P450, универсальных окислительных специалистов природы. В отличие от многих промышленных катализаторов, этот фермент работает в воде, при умеренной температуре и выбирает очень конкретные позиции в молекуле. Ранние работы показали, что CYP153A6 вводит кислород на концевые участки простых углеводородных цепей и в некоторые растительные ароматические молекулы. Здесь авторы проверяют, может ли он также атаковать «бензильную» позицию — малую боковую цепочку, присоединённую к бензольному кольцу — в толуоле и родственных соединениях. Эта трансформация превращает производные толуола в бензиловые спирты, ценные строительные блоки для фармацевтики, ароматизаторов и тонкой химии.
Проверка, какие молекулы нравятся ферменту
Команда сначала провела биотрансформационные эксперименты с использованием генетически модифицированных клеток E. coli, синтезирующих CYP153A6, как в виде цельных клеток, так и в виде клеточных экстрактов. Они подвергали фермент панели производных толуола, варьируя группу, присоединённую к ароматическому кольцу (например, метил, хлор, метокси, гидроксил или нитро) и её положение (пара-, мета- или орто-). Фермент хорошо работал с аполярными или слабо полярными соединениями, такими как p-цимен, p-ксилол, p-метилани́зол и p-хлор-толуол, последовательно превращая бензильную метильную группу в бензиловый спирт. Поразительно, что он полностью игнорировал более сильно полярные молекулы, такие как p-крезол, p-метилбензиловый спирт и p-нитротолуол, хотя они структурно похожи. Эта картина указывала на то, что карман фермента сильно гидрофобен и не благоволит полярным группам.
Построение трёхмерной карты молекулярного аппарата
Поскольку трёхмерная структура CYP153A6 не была экспериментально определена, исследователи создали качественную компьютерную модель, используя близкородственный P450 с известной структурой. Они верифицировали эту модель, проверив её геометрию и проведя длительные молекулярно-динамические симуляции, чтобы убедиться, что белок остаётся стабильным со временем — и это подтвердилось. Симуляции выявили зарытую активную область, связанную с внешней средой узкими туннелями, через которые субстраты входят, а продукты выходят. Эти туннели формируются и перекрываются гибкими петлями на поверхности белка, что помогает объяснить, как фермент может направлять гидрофобные молекулы к реакционноспособному центру гема, одновременно позволяя воде и окисленным продуктам уходить.
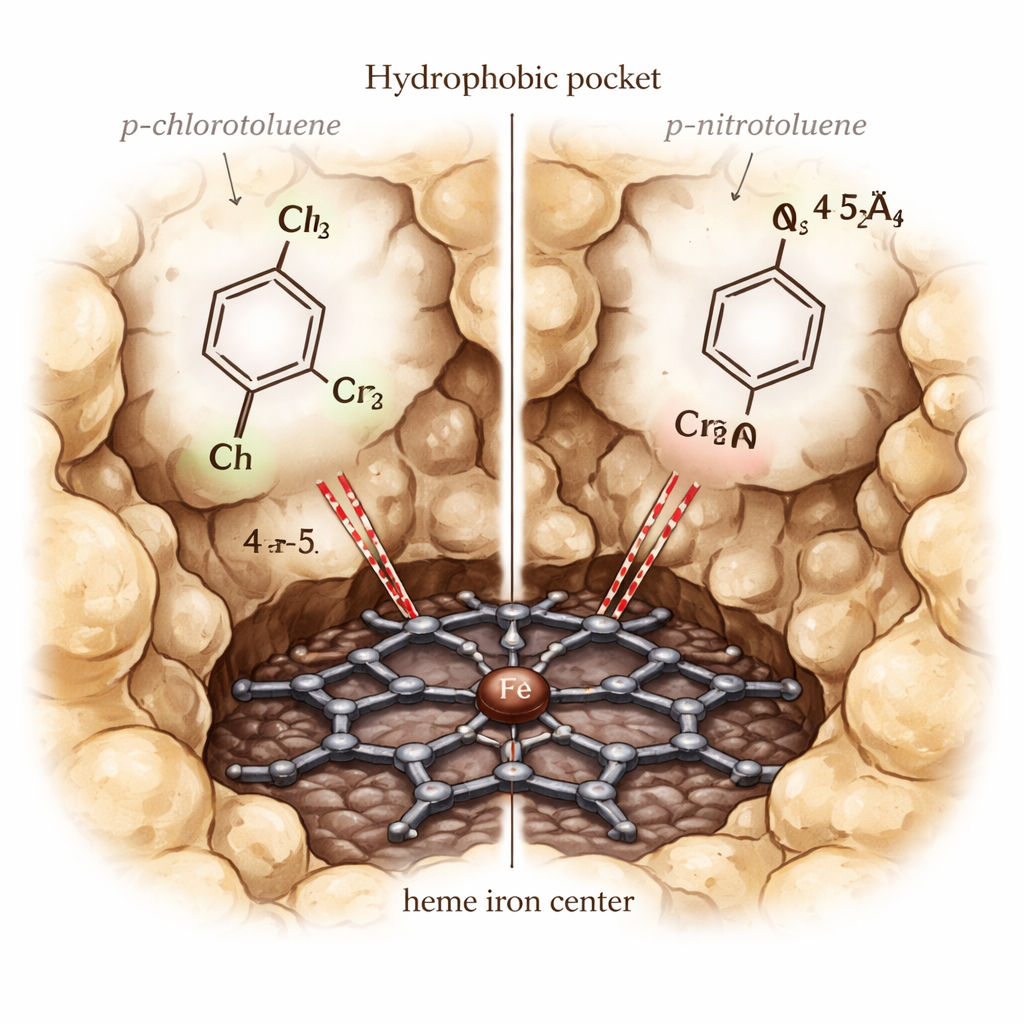
Наблюдение за посадкой, движением и реакцией молекул
Имея модель, авторы смоделировали, как разные производные толуола связываются внутри CYP153A6. Они использовали подход, называемый ансамблевым докингом, тестируя множество слегка отличающихся конформаций белка и несколько электронных состояний гема, чтобы определить, какие варианты лучше всего разделяют истинные субстраты и несубстраты. Победивший сценарий использовал железо в его покоящемся феррическом состоянии и отсутствие лишних молекул воды в кармане, и он правильно отдавал предпочтение известным субстратам. Дальнейшие симуляции отслеживали, кадр за кадром, как каждая молекула располагалась относительно гема. Хорошие субстраты, такие как p-цимен и p-ксилол, оставались близко к железу с бензильной метильной группой, повернутой к нему, и их предсказанные энергии связывания были сильно благоприятны. Плохие субстраты обычно отдалялись, принимали неудобные ориентации или взаимодействовали неблагоприятно с преимущественно «маслянистыми» боковыми цепями, выстилающими карман.
Почему один близнец реагирует, а другой — нет
Выделялось одно противоречие: p-хлор-толуол эффективно окисляется CYP153A6, тогда как p-нитротолуол — нет, хотя оба помещаются в карман и в моделях связываются с похожой силой. Чтобы разобраться, авторы провели более детальные квантово-механико/молекулярно-механические (QM/MM) расчёты для высокореактивного состояния фермента, известного как «Соединение I». Эти расчёты показали, что нитро‑группа оттягивает настолько много электронной плотности от бензильного углерода, что его становится очень трудно окислить, несмотря на геометрическую близость. Напротив, хлорогруппа обеспечивает более благоприятную электронную связь между гемом и субстратом, что отражается в большем спиновом переносе на ароматическое кольцо и метильную группу и более реакционноспособном выравнивании для критического шага абстракции водорода.
Что это значит для чистой химии
Проще говоря, CYP153A6 ведёт себя как крошечная, маслянистая перчатка, которая удерживает некоторые молекулы, похожие на топливо, в точном положении, чтобы туда можно было добавить кислород — превращая их в более водорастворимые, полезные и в конечном счёте более разлагаемые продукты. Исследование показывает, что фермент предпочитает неполярные заместители и что как форма, так и поток электронов определяют, будет ли данное производное толуола преобразовано. Прояснив, как CYP153A6 распознаёт и активирует эти молекулы, работа прокладывает дорожную карту для инженерии улучшенных вариантов, которые могли бы помочь очищать ароматические загрязнения или производить сложные химикаты более устойчивым способом.
Цитирование: Wei, Y., Donzella, S., Foiadelli, S. et al. Structure-based modeling reveals molecular basis for CYP153A6’s novel activity toward toluene derivatives. Sci Rep 16, 7570 (2026). https://doi.org/10.1038/s41598-026-38986-7
Ключевые слова: биокатализ, цитохром P450, гидроксилирование толуола, инженерия ферментов, зеленая химия