Clear Sky Science · ru
Транспластомная биофабрика для производства функционального человеческого α‑лактальбумина для пищевых и терапевтических применений
Преобразуем растения в фабрики молочных белков
Современные рационы сильно зависят от молочных белков, но масштабное разведение коров влечёт за собой экологические издержки и этические вопросы. В этом исследовании рассматривается принципиально иной способ получения ключевого белка человеческого молока — научить листья растений его производить. Работа показывает, что табак можно перепрограммировать на синтез человеческого α‑лактальбумина, белка, важного для питания младенцев и обладающего потенциальными антираковыми свойствами, открывая путь к ингредиентам детских смесей без животных источников и новым пищевым компонентам с противораковым действием.
Почему этот молочный белок важен
Грудное молоко — это не просто пища; это тонко настроенный коктейль белков, жиров и сахаров, который меняется в зависимости от потребностей ребёнка. Один из важнейших его белков — α‑лактальбумин, который участвует в синтезе лактозы, основного молочного сахара и критического источника энергии для младенцев. α‑Лактальбумин богат незаменимыми аминокислотами, включая триптофан — строительный блок для серотонина, нейромедиатора, связанного с настроением — и ассоциирован с лучшей устойчивостью к стрессу и возможной защитой от некоторых видов рака. Он легко усваивается, имеет мягкий вкус и устойчив в широком диапазоне кислотности, поэтому широко используется в детских смесях и питательных напитках — и спрос на него растёт.
Проблемы традиционного молочного производства
Зависимость от коров для получения молочных белков имеет недостатки. Животноводство даёт значительную долю глобальных выбросов парниковых газов, а крупные молочные фермы требуют больших площадей земли, воды и корма. Кроме того, фермерские практики могут приводить к попаданию в молоко гормонов, антибиотиков и патогенов. Эти факторы стимулируют интерес к «клеточному сельскому хозяйству», где молочные белки производят микробы или культивируемые клетки, а не животные. Однако многие такие системы остаются дорогими, трудно масштабируемыми или дают белки, не полностью идентичные человеческим. Растения, особенно их хлоропласты — крошечные зелёные фабрики фотосинтеза — предлагают перспективную альтернативную платформу.
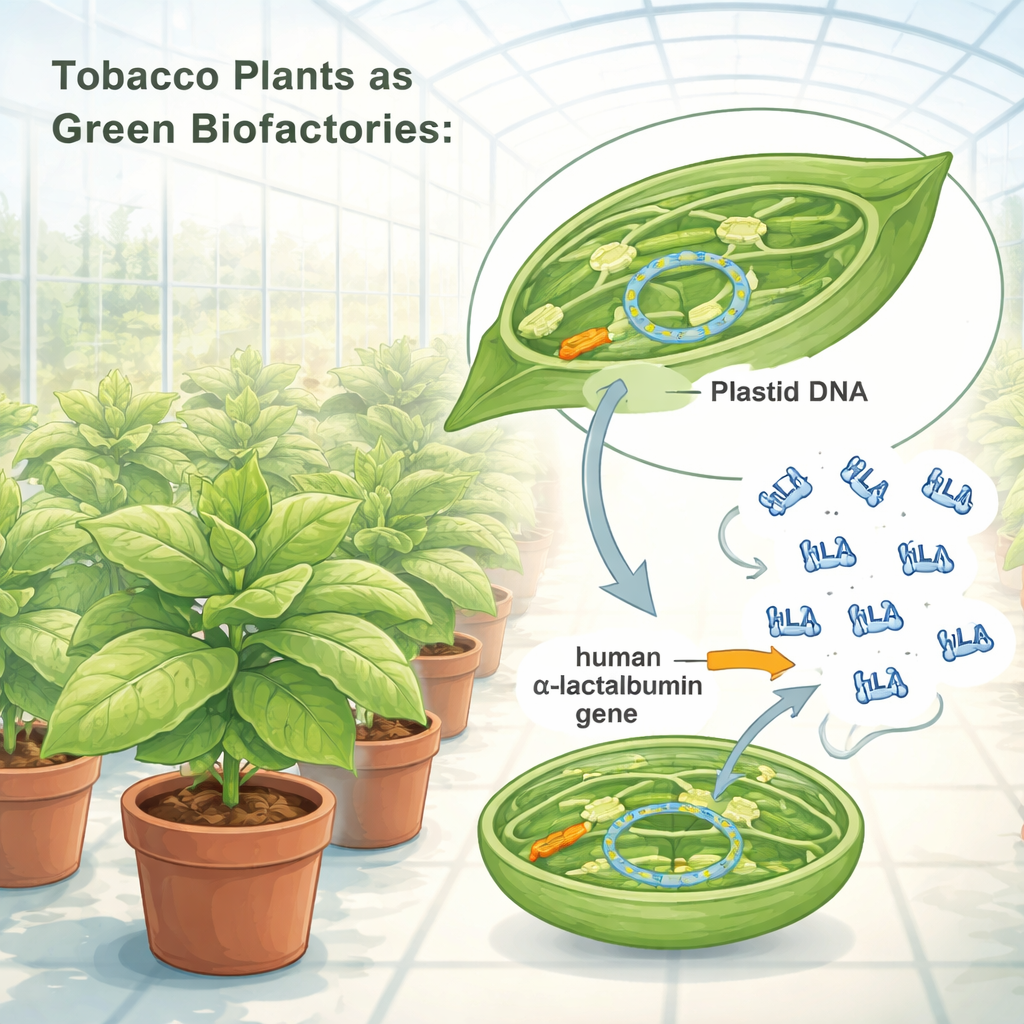
Перепрограммирование хлоропластов в биофабрики
Исследователи переписали генетические инструкции для человеческого α‑лактальбумина так, чтобы хлоропласты табака могли эффективно их считывать. Они вставили оптимизированный ген в ДНК хлоропластов, используя «генную кассету», собранную из сильных растительных регуляторных элементов, действующих как мощные выключатели. Методом бомбардировки частиц кассету доставили в клетки листа табака, затем отобрали проростки, чьи хлоропласты полностью приняли новый ген. Генетические тесты подтвердили, что все копии ДНК хлоропластов в этих растениях теперь содержат чертёж человеческого белка. Модифицированные растения нормально росли в условиях теплицы, образовывали семена и не проявляли видимых изменений в размере, форме или плодовитости, что говорит о том, что дополнительная нагрузка белком не вредила здоровью растений.
Доказательство работоспособности растительного белка
Далее команда проверила, ведёт ли себя растительно‑произведённый α‑лактальбумин как настоящий человеческий белок. Они экстрагировали растворимые белки из листьев, очистили α‑лактальбумин и изучили его структуру с помощью метода, дающего спектральный «отпечаток» свёрнутой формы белка. Спектр растительного белка почти совпал со спектром коммерческого человеческого α‑лактальбумина, что указывает на схожую свёртку. Функционально растительный белок активировал фермент синтеза лактозы почти так же эффективно, как нативный белок, обеспечивая образование лактозы примерно на 93% от скорости стандартного протеина. Примечательно, что α‑лактальбумин накапливался до примерно 23% от всех растворимых белков в листьях — один из самых высоких показателей для человеческих белков, произведённых в растительных хлоропластах — что говорит о промышленно значимых урожаях этой системы.
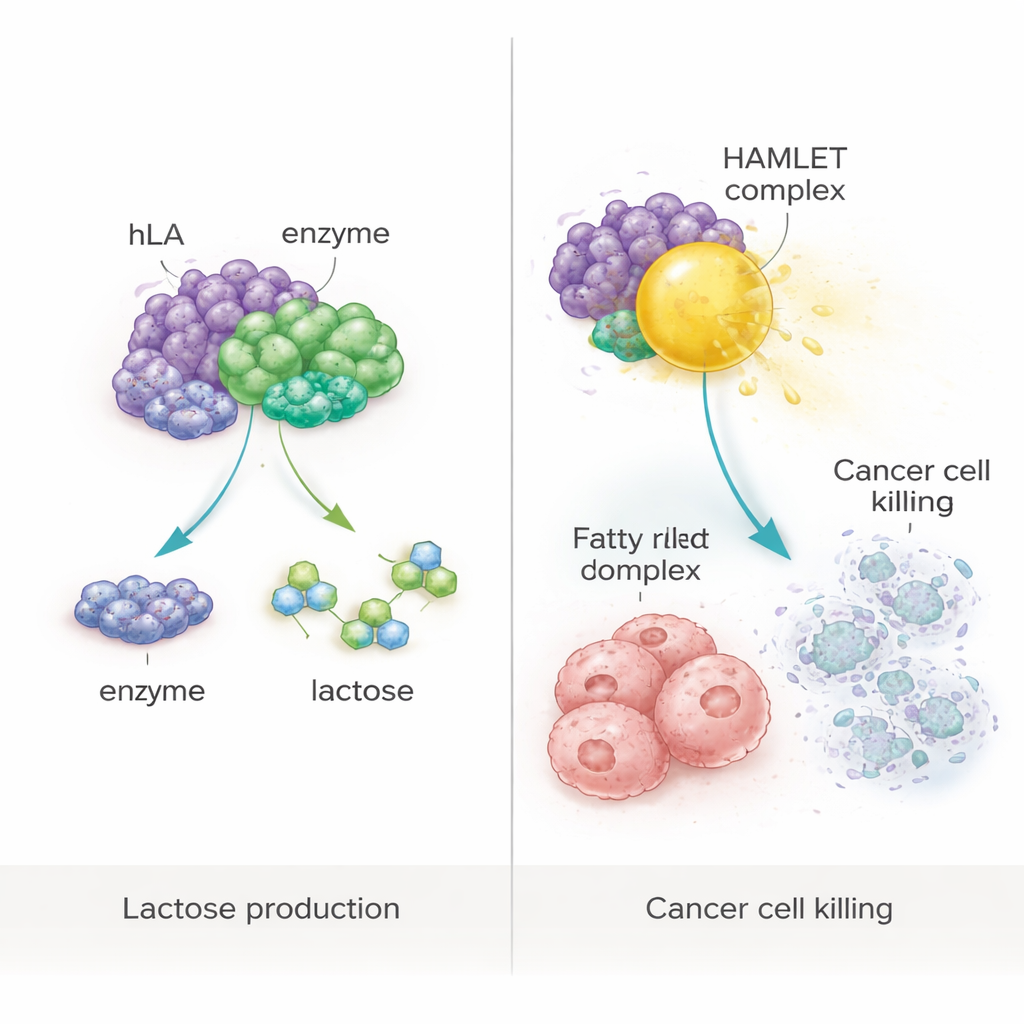
От питания к противораковым комплексам
Исследование также проверяло более амбициозную идею: использовать растительно‑произведённый белок как строительный блок для известного антиракового комплекса HAMLET, который образуется при плотном связывании α‑лактальбумина с олеиновой кислотой, обычной жирной кислотой. Путём мягкого нагревания очищенного растительного белка с олеиновой кислотой в контролируемых условиях исследователи получили комплекс, похожий на HAMLET. При обработке этим комплексом культуры человеческих клеток колоректального (WiDr) и молочного (MCF‑7) происхождения выживаемость клеток резко снизилась ниже 10%. Последующий анализ показал, что большинство поражённых клеток претерпевают апоптоз — форму программируемой гибели, а не неконтролируемого разрушения. Важно, что ни сам белок, ни жирная кислота по отдельности, ни экстракты немодифицированных растений не вызывали значительной гибели клеток, что подтверждает: противораковый эффект зависел от специфического комплекса.
Что это может значить для будущих продуктов питания и лекарств
В совокупности работа демонстрирует, что хлоропласты растений могут надёжно производить большие количества человеческого молочного белка, который одновременно имеет питательную ценность и терапевтическую активность. Для неспециалиста это означает, что будущие детские смеси, функциональные продукты питания или добавки могут однажды изготавливаться с использованием белков, выращенных в листьях, а не получаемых от коров — снижая воздействие на окружающую среду и лучше соответствуя человеческой биологии. В то же время тот же растительно‑произведённый белок можно в лаборатории превратить в целенаправленный противораковый комплекс, что намекает на пути создания доступных биотерапевтических средств на растительной основе. Хотя необходимы дополнительные исследования для подтверждения безопасности и эффективности в животных и людях — а также для переноса технологии на съедобные культуры — исследование даёт убедительный набросок будущего, в котором растения выполняют роль мини‑фабрик для питания и медицины следующего поколения.
Цитирование: Ehsasatvatan, M., Kohnehrouz, B.B. Transplastomic biofactory for the production of functional human α-lactalbumin for nutritional and therapeutic applications. Sci Rep 16, 7359 (2026). https://doi.org/10.1038/s41598-026-38965-y
Ключевые слова: молочные белки, произведённые растениями, хлоропластная биофабрика, человеческий альфа‑лактальбумин, устойчивые молочные альтернативы, ракотерапия HAMLET