Clear Sky Science · ru
Интегрин αv способствует регуляции жесткости гладкомышечных клеток сосудов
Почему «упругость» артерий важна
С возрастом или при повышенном кровяном давлении крупные сосуды постепенно теряют свою естественную упругость и становятся жестче. Это заставляет сердце работать сильнее и повышает риск инфарктов, инсультов и других сердечно‑сосудистых осложнений. Ученым давно известно, что на жесткость влияют материалы стенки артерий — белки вроде эластина и коллагена. В этом исследовании ставится более тонкий вопрос: могут ли сами мышечные клетки в стенке сосуда становиться жестче и помогает ли небольшая группа поверхностных рецепторов, называемых интегрином αv, сохранять эти клетки, а значит и наши артерии, более гибкими?
Мышечные клетки, которые формируют кровоток
Крупные артерии — это не просто пассивные трубы. Их средний слой заполнен сосудистыми гладкомышечными клетками, которые могут сокращаться и расслабляться, чтобы тонко регулировать кровоток и давление. Эти клетки прикреплены к окружающему каркасу — внеклеточному матриксу. Исследователи сосредоточились на одной группе молекул‑якорей, интегрине αv, который проходит через мембрану клетки и физически связывает внутренний скелет клетки с внешним матриксом. Ранее было показано, что интегрин αv участвует в рубцевании и ремоделировании сосудов, но оставалось неясным, контролирует ли он также жесткость самих мышечных клеток, особенно под воздействием гормонов, таких как ангиотензин II, повышающих артериальное давление и способствующих фиброзу.
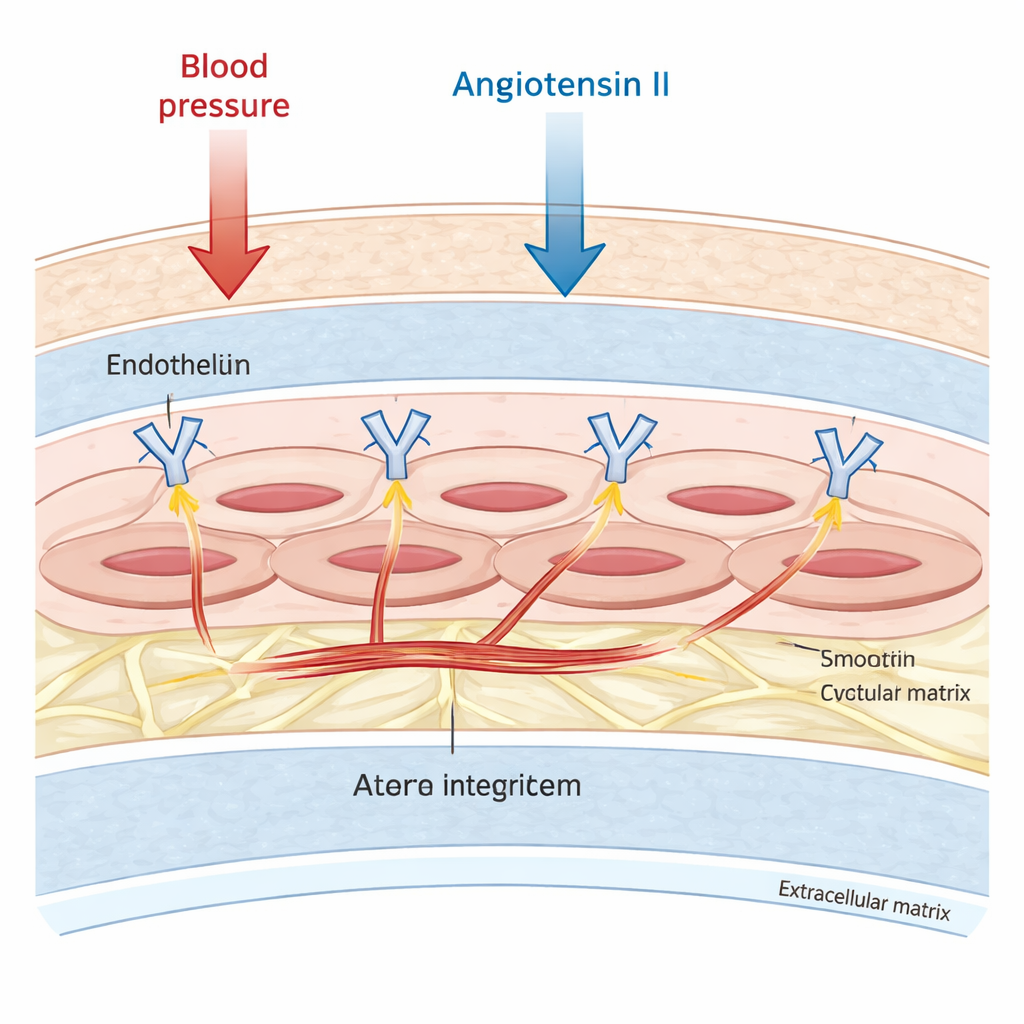
Измерение жесткости по одной клетке
Чтобы разобраться в этом, команда использовала культивируемые мышиные гладкомышечные клетки и мышей, у которых интегрин αv был утрачен специально в сосудистых мышечных клетках. Они измеряли жесткость клеток с помощью атомно‑силового микроскопа — техники, в которой ультратонкий зонд аккуратно вдавливает поверхность клетки и фиксирует, какая сила требуется. Клетки без интегрина αv были вдвое и более жестче, чем контрольные клетки в спокойных условиях. После двухдневного воздействия ангиотензина II эти дефектные клетки стали примерно в три раза жестче, тогда как нормальные клетки почти не изменялись. Поскольку измерения проводились при очень мелких вдавлениях, авторы создали детальную компьютерную модель гладкомышечной клетки и смоделировали более глубокие вдавления. Симуляции показали, что мелкие тесты подчеркивают вклад наружной оболочки клетки и кортикального слоя, и результаты оставались в диапазоне, наблюдаемом у жестких мутантных клеток, что поддерживает биологические выводы.
Преобразованный внутренний скелет
Далее ученые заглянули внутрь клеток. С помощью флуоресцентных красителей и микроскопии они исследовали актин — ключевой филамент, формирующий внутренний каркас клетки. Контрольные мышечные клетки демонстрировали относительно рассеянную сеть актиновых волокон, даже после обработки ангиотензином II. Напротив, клетки, лишенные интегрина αv, образовывали толстые стресс‑волокна, пересекающие клетку, и после воздействия гормона — интенсивную полосу актина прямо под мембраной, известную как кортикальный актин. Количественная оценка накопления актина у края клетки подтвердила, что этот кортикальный слой был значительно обогащен только в интегрин‑дефицитных клетках. Эти клетки также формировали необычно длинные структуры адгезии, с помощью которых они захватывают матрикс, что согласуется с переходом к более натяженным, фибриллярным сайтам адгезии, способным «зафиксировать» клетку в жестком состоянии.
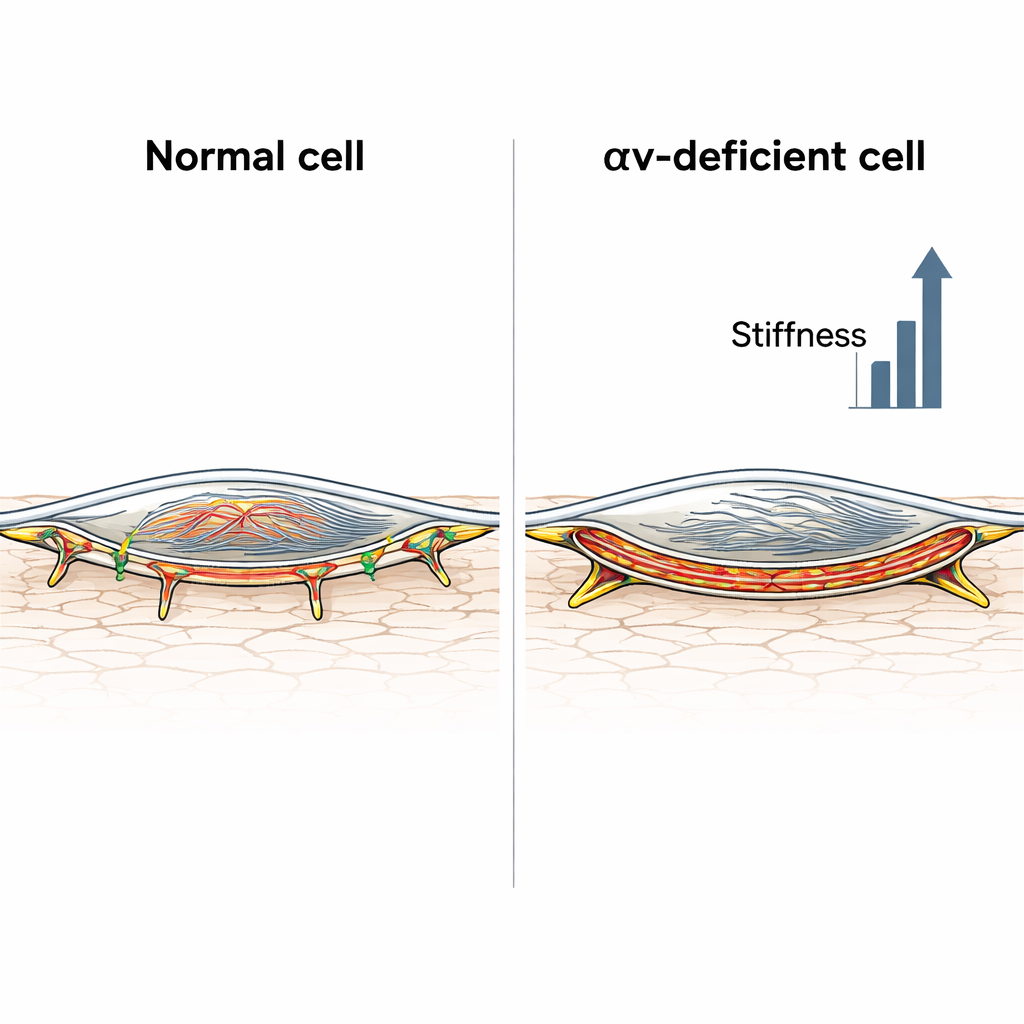
Когда стена выглядит одинаково, но ведет себя иначе
Поскольку артерии — это не только мышечные клетки, ученые также измерили механические свойства сонных артерий у живых мышей с интегрином αv в сосудистых мышечных клетках и без него, а также при хронической инфузии ангиотензина II и без нее. Удивительно, но общие артериальные параметры и жесткость стенки — оцененные по ультразвуковым кривым «давление–диаметр» — оказались похожими в обоих линиях мышей как в исходных условиях, так и после лечения гормоном. Тем не менее микроскопический состав стенки различался. При введении ангиотензина II у контрольных мышей наблюдалось снижение эластина и увеличение коллагена — классические признаки жесткого матрикса, тогда как у мышей без интегрина αv изменение коллагена было сравнительно скромным, но их мышечные клетки стали значительно жестче. Иными словами, у нормальных мышей главным двигателем жесткости был матрикс; у интегрин‑дефицитных мышей сами мышечные клетки стали настолько ригидными, что это фактически нейтрализовало их более скромные матричные изменения.
Что это означает для стареющих артерий
Для неспециалиста главный вывод в том, что жесткость артерий зависит не только от износа эластичных волокон, но и от того, как мышечные клетки в стенке организуют свои крошечные внутренние «канаты». Интегрин αv обычно помогает удерживать эти клетки от избыточного огрубления при воздействии гормонов, таких как ангиотензин II. При потере этого контроля клетки перестраивают свой актиновый скелет — особенно в кортикальном слое прямо под мембраной — и «заклиниваются» в более жестком состоянии, что может приводить к усугублению жесткости артерий даже без радикальных изменений окружающего матрикса. Это наблюдение открывает новые идеи для терапии: препараты, мягко релаксирующие или реорганизующие кортикальную сеть актина или модулирующие сигналы, связанные с интегрином, могут в будущем дополнить антигипертензивную терапию и более прямо восстанавливать «упругость» стареющих артерий.
Цитирование: Bascetin, R., Belozertseva, E., Regnault, V. et al. Integrin αv contributes to the regulation of vascular smooth muscle cell stiffness. Sci Rep 16, 7682 (2026). https://doi.org/10.1038/s41598-026-38948-z
Ключевые слова: жесткость артерий, гладкомышечные клетки сосудов, интегрин альфа v, цитоскелет актин, ангиотензин II