Clear Sky Science · ru
A2-панкортины взаимодействуют с Bcl-xL и WAVE1, усиливают контакты митохондрий и ЭПР (MERCs) и увеличивают митохондриальное накопление кальция, способствуя гибели клеток при инсульте
Почему важны крошечные связи в мозге новорождённых
Инсульт часто воспринимается как заболевание взрослых, но у новорождённых он может незаметно повредить развивающийся мозг и привести к пожизненным проблемам. В этом исследовании авторы изучают, что происходит внутри нервных клеток во время такой кризисной ситуации. Они сосредотачиваются на малоизвестном семействе белков — панкортинах — и показывают, как две развивающиеся формы действуют как опасные «усилители», укрепляя связи между ключевыми структурами клетки и вызывая поток кальция, который может привести молодые нейроны к смерти.
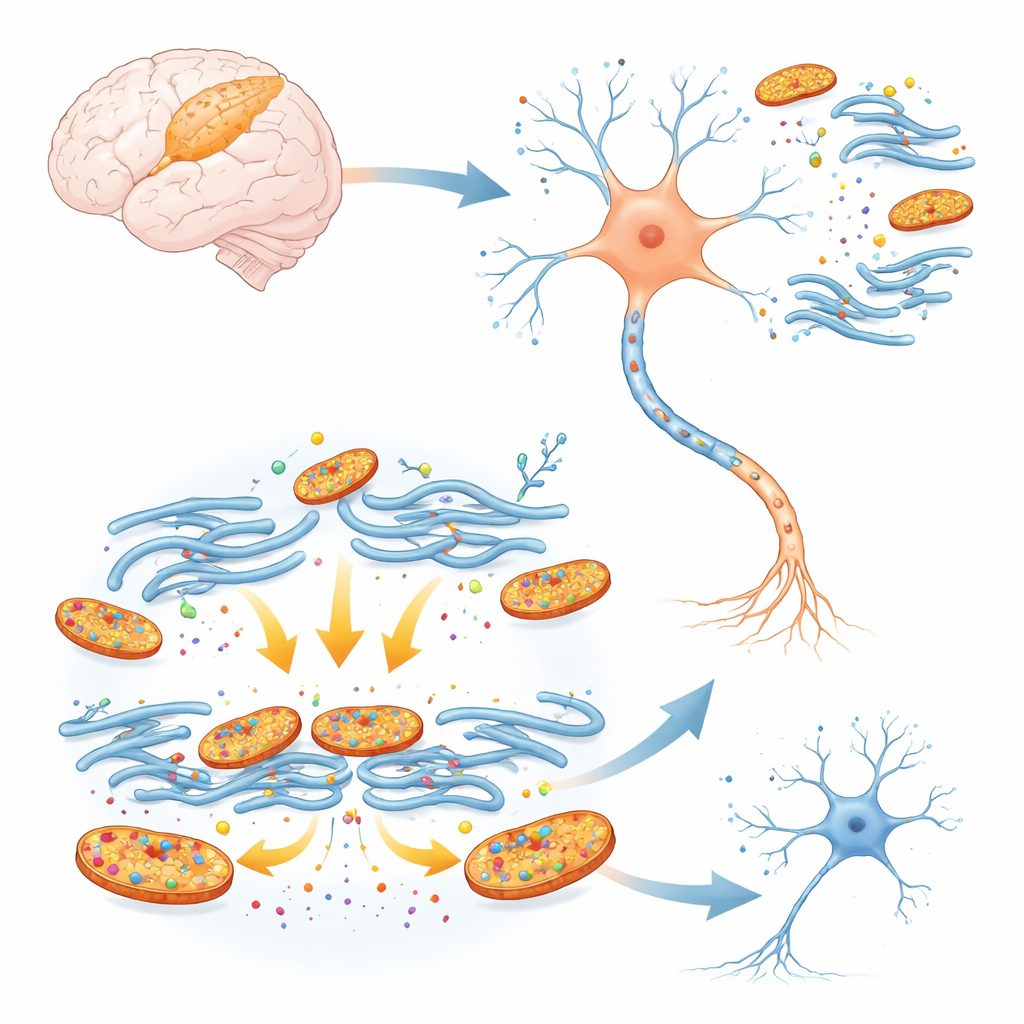
Скрытые виновники в мозге новорождённого
Панкортины — это белки, подобные каркасам, которые помогают формировать растущий мозг. Две формы, называемые A2-панкортинами, многочисленны в раннем развитии и затем в значительной мере исчезают по мере созревания мозга. Поскольку мозг новорождённых особенно уязвим к потере кислорода, исследователи спросили, не усугубляют ли эти белки повреждение при кратковременном прекращении кровоснабжения коры, как при неонатальном инсульте. В культурах корковых нейронов мыши они с помощью генетических инструментов снизили уровень всех панкортинов и затем подвергли клетки дефициту кислорода и глюкозы, имитирующему инсульт. Нейроны с пониженным содержанием панкортинов выживали значительно чаще, что наводит на мысль, что эти белки, вместо защиты молодых клеток, при стрессе способствуют их повреждению.
От моделей инсульта у мышей до спасённой ткани мозга
Чтобы проверить, проявляется ли эта вредная роль в живом мозге, команда создала мышей, лишённых именно развивающихся форм A2-панкортинов. Молодых двухнедельных нокаутных мышей и их нормальных собратьев подвергли блокаде крупной мозговой артерии — стандартной модели ишемического инсульта. Через день у обеих групп наблюдались повреждения в глубоких областях мозга, но кора у мышей без A2-панкортинов была повреждена примерно вдвое меньше, чем у нормальных животных. Поразительно, что этот защитный эффект исчезал у пяти недельных мышей, когда доминируют взрослые варианты панкортинов. Эти зависящие от возраста результаты указывают на A2-панкортины как ключевые факторы, способствующие гибели в неонатальной коре, связывая программу развития с уязвимостью к инсульту.
Опасные зоны контакта внутри нейронов
Внутри клеток митохондрии, производящие энергию, находятся вблизи эндоплазматического ретикулума (ЭПР) — сложенной мембранной сети, запасающей кальций. В местах, где эти две мембраны приближаются, так называемые контакты митохондрий и ЭПР действуют как микроскопические туннели, по которым может проходить кальций. Умеренная передача поддерживает выработку энергии, но избыточная может перегрузить митохондрии и вызвать гибель клетки. Исследователи обнаружили, что A2-панкортины вместе с двумя партнёрами — Bcl-xL и WAVE1 — собирают трёхчастный комплекс, локализующийся в этих зонах контакта. Когда они заставляли клетки экспрессировать дополнительные A2-панкортины вместе с этими партнёрами, митохондрии и ЭПР контактировали чаще и плотнее, что было зафиксировано специализированным сплит-флуоресцентным датчиком. Белок-тетчер GRP75 входил в этот комплекс и способствовал стабилизации зон контакта.
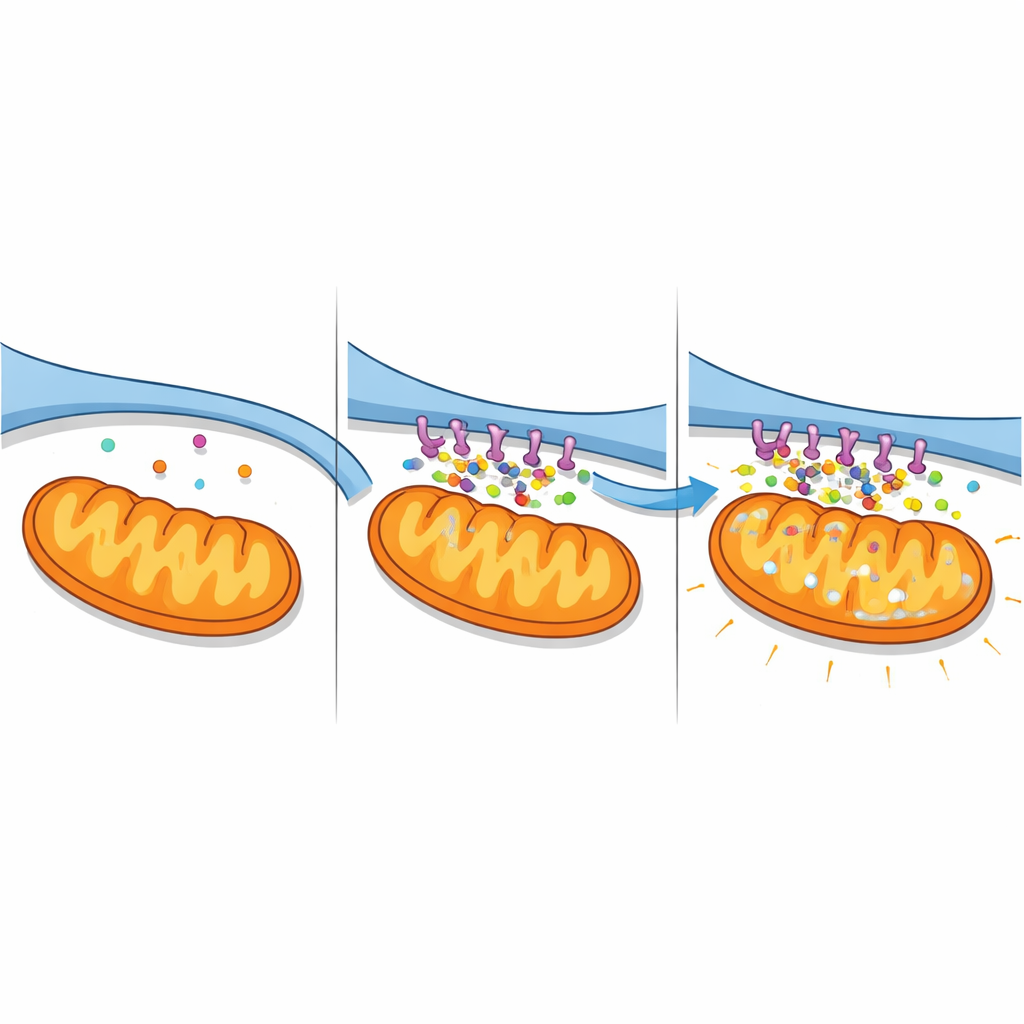
Потоки кальция и выход из строя энергетических станций
Укрепление контактов имело серьёзные последствия для баланса кальция. С помощью флуоресцентных индикаторов, отдельно регистрирующих кальций в цитозоле, ЭПР и митохондриях, авторы наблюдали динамику изменений. Клетки, экспрессирующие комплекс A2-панкортинов, демонстрировали постепенный рост кальция в митохондриях и в окружающей жидкости при одновременном снижении запасов в ЭПР — признак массового переноса из ЭПР в митохондрии. Блокирование ключевого канала высвобождения кальция на поверхности ЭПР (IP3R) в значительной мере предотвращало эти изменения, подтверждая, что комплекс усиливает специфический путь от ЭПР к митохондриям. В нервоподобных клетках, подвергнутых инсультоподобному дефициту кислорода и глюкозы, снижение уровня панкортинов имело обратный эффект: избыток кальция был ослаблен, а запасы ЭПР лучше сохранялись. Вместе эти данные показывают, что A2-панкортины организуют «супермаршрут» для кальция, который становится смертельным при ишемическом стрессе.
Что это значит для защиты мозга новорождённых
Для неспециалистов главный вывод таков: работа выявляет новый молекулярный переключатель, который помогает решить, выживут ли молодые нейроны после инсульта. Укрепляя микроскопические соединения между мембранами, хранящими кальций, и клеточными энергетическими станциями, A2-панкортины приводят к тому, что митохондрии захлёбываются избытком кальция и выходят из строя. Удаление этих белков у молодых мышей смягчает последствия экспериментального инсульта, что даёт надежду на то, что лекарства или генно-ориентированные терапии, направленные на разрушение комплексов A2-панкортинов или ослабление поддерживаемых ими зон контакта, однажды смогут уменьшить повреждение мозга у пострадавших новорождённых. Хотя такие подходы пока остаются перспективой, исследование прокладывает ясный и проверяемый путь от белков развития к перегрузке кальция и потере нейронов при неонатальном инсульте.
Цитирование: Yang, Q., Wang, CC., Matsuyama, T. et al. A2-pancortins interact with Bcl-xL and WAVE1 to promote mitochondria-ER contact sites (MERCs) and exacerbate mitochondrial calcium elevation to mediate cell death in stroke. Sci Rep 16, 8467 (2026). https://doi.org/10.1038/s41598-026-38928-3
Ключевые слова: неонатальный инсульт, контакты митохондрий и ЭПР, избыток кальция, белки панкортины, гибель нейронов