Clear Sky Science · ru
Новая регуляторная ось C/EBPα–miR-335-5p–PRKAA2 стимулирует накопление жира в печени при MASLD
Почему важна жировая болезнь печени
Многие люди, которые почти не употребляют алкоголь, все же развивают «жировую печень» — состояние, ныне называемое стеатотической болезнью печени, связанной с нарушением обмена веществ (MASLD). Оно тесно связано с ожирением и сахарным диабетом 2 типа и может бессимптомно прогрессировать до фиброза, цирроза и даже рака печени. В этом исследовании задаются простым, но ключевым вопросом: что происходит внутри печеночных клеток, из‑за чего в них откладывается столько жира, и можно ли найти молекулярный переключатель, который можно было бы выключить, чтобы защитить печень?
Скрытая цепная реакция в печеночных клетках
Исследователи сосредоточились на молекулярной цепочке, связывающей питание и обмен веществ с накоплением жира в печени. Они изучали мышей, получавших богатую жирами диету, и культивированные печеночные клетки, погружённые в жирные кислоты, чтобы моделировать MASLD. В этих моделях животные набирали вес, уровень липидов в крови повышался, а в печени появились маслянистые капли, воспроизводя ключевые черты человеческой жировой печени. В таких жировых печенях команда заметила, что уровень определённого регулятора генов — фактора транскрипции C/EBPα — и небольшой РНК‑молекулы miR‑335‑5p повышался, тогда как защитная субъединица фермента PRKAA2, часть известного энергетического сенсора AMPK, снижалась.
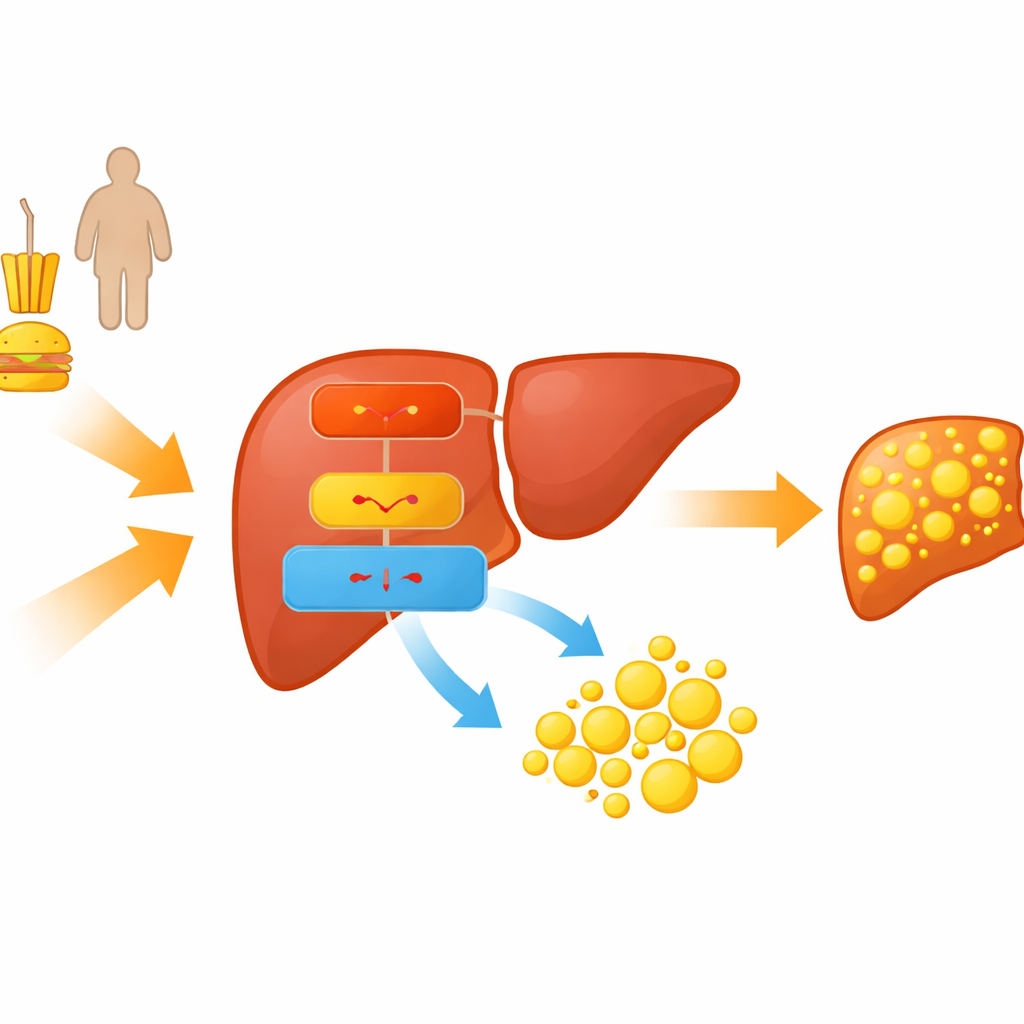
Как малая РНК сдвигает баланс в сторону жира
Малые РНК‑молекулы, называемые микрорНК, действуют как молекулярные регуляторы, приглушая экспрессию конкретных генов. Команда показала, что miR‑335‑5p прямо связывается с матрицей, кодирующей PRKAA2, и препятствует синтезу этого белка. PRKAA2 помогает собирать комплекс AMPK, который обычно распознаёт низкий уровень энергии и отвечает подавлением синтеза жиров и стимулированием их окисления. Когда уровни miR‑335‑5p искусственно повышали в печёночных клетках, уровни PRKAA2 снижались, активность AMPK падала, а белки, ведущие синтез липидов, возрастали, что приводило к заметному накоплению жировых капель. При блокировании miR‑335‑5p наблюдалось обратное: PRKAA2 и активность AMPK возрастали, а накопление жира уменьшалось.
Главный переключатель, запускающий каскад
Что же включает miR‑335‑5p изначально? Просканировав ДНК‑последовательность, контролирующую эту микрорНК, учёные предсказали несколько возможных «главных переключателей» и сосредоточились на C/EBPα, уже известном как фактор, влияющий на обмен жиров и углеводов. Они подтвердили, что C/EBPα напрямую связывается с регуляторной областью miR‑335‑5p и усиливает её активность. Увеличение C/EBPα в печёночных клетках повышало уровни miR‑335‑5p, снижало PRKAA2, ослабляло сигналы AMPK и способствовало накоплению жира. Подавление C/EBPα давало противоположный эффект — усиливало энергетическое «торможение» клетки и уменьшало количество липидов. Эксперименты восстановления, в которых блокировали miR‑335‑5p или восстанавливали PRKAA2, показали, что большая часть жиропродуцирующего эффекта C/EBPα проходит через эту единую цепочку.
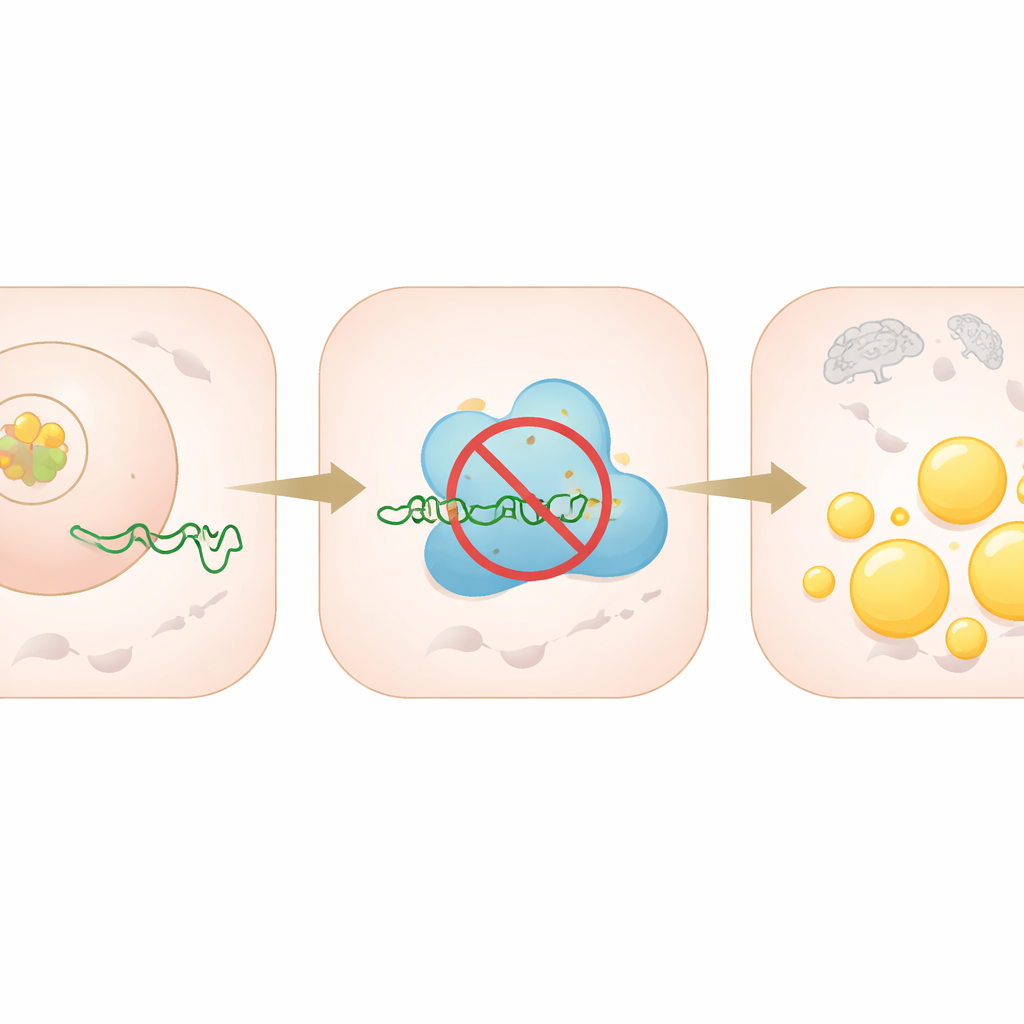
От чашек Петри до живых мышей
Чтобы проверить, важен ли этот путь в живом организме, исследователи использовали инженерные вирусы для доставки генетических инструментов непосредственно в печень мышей, получавших высокожировую диету. Один инструмент снижал уровень C/EBPα; другой «поглощал» избыточный miR‑335‑5p. В обоих случаях в печени животных было меньше жира, микроскопическая структура улучшалась, а уровни PRKAA2 и активность AMPK восстанавливались, в то время как белки, ответственные за синтез жиров, снижались. Эти результаты in vivo согласовывались с данными клеточных культур и подчёркивали, что цепочка C/EBPα–miR‑335‑5p–PRKAA2 — не просто лабораторная особенность, а мощный драйвер жировой болезни печени в живом организме.
Что это значит для будущих лечений
Проще говоря, исследование выявляет трёхшаговую молекулярную передачу, заставляющую печёночные клетки запасать жир: C/EBPα включает miR‑335‑5p, который, в свою очередь, подавляет PRKAA2 и ослабляет AMPK — энергетическое «тормозное устройство» клетки. Когда этот тормоз выключен, механизмы синтеза жира работают без контроля, и печень наполняется липидами. Прерывание любой звена этой цепи — снижение C/EBPα, блокировка miR‑335‑5p или усиление PRKAA2/AMPK — уменьшало количество жира в печени мышей. Хотя до безопасного применения у людей предстоит ещё много работы, этот путь предлагает ясную и проверяемую цель для будущих лекарств, направленных на замедление или обращение MASLD.
Цитирование: Zeng, X., Xu, Y., You, S. et al. A novel C/EBPα–miR-335-5p–PRKAA2 regulatory axis drives hepatic lipid accumulation in MASLD. Sci Rep 16, 9255 (2026). https://doi.org/10.1038/s41598-026-38918-5
Ключевые слова: жировая болезнь печени, микрорНК, AMPK, липидный метаболизм, метаболическое заболевание