Clear Sky Science · ru
Профили микробиоты кишечника и метаболических путей у инфицированных и неинфицированных пациентов после трансплантации сердца до и после операции
Почему ваш кишечник важен после пересадки сердца
Трансплантация сердца даёт людям с тяжёлой сердечной недостаточностью второй шанс на жизнь, но инфекции в первые недели после операции по‑прежнему представляют серьёзную угрозу. В этом исследовании задаётся на вид простой, но важный вопрос: как сообщество микроорганизмов, обитающее в наших кишечниках — микробиота — меняется в период вокруг трансплантации сердца, и могут ли эти изменения помочь объяснить, кто заболевает инфекцией, а кто остаётся здоровым?
Крошечная экосистема внутри пациентов с трансплантатом
Наши кишечники населены триллионами бактерий, которые помогают переваривать пищу, обучают иммунную систему и препятствуют захвату среды патогенами. Операция, сильные иммунодепрессанты и широкоспектровые антибиотики могут нарушить эту хрупкую экосистему. Чтобы отследить происходящее у пациентов после трансплантации сердца, исследователи в Китае наблюдали 20 взрослых, получавших донорские сердца. Они собрали образцы кала примерно за неделю до операции и ещё раз через 30 дней после, затем с помощью секвенирования ДНК каталогизировали присутствующие бактерии и использовали компьютерные инструменты для прогнозирования возможной метаболической активности этих микробов.
Четыре группы пациентов — четыре микробных паттерна
Команда разделила пациентов на четыре группы: с инфекцией и без инфекции до операции, а также с инфекцией и без инфекции в первый месяц после операции. До трансплантации общая диверсификация и структура микробиоты выглядели удивительно схожими как у пациентов с уже развившейся инфекцией, так и без неё. У людей без предоперационных инфекций преимущественно доминировал знакомый род Bacteroides, часто ассоциируемый со стабильным состоянием кишечника. В свою очередь у инфицированных пациентов наблюдалась смесь, включавшая потенциально вредный Enterococcus casseliflavus вместе с бактериями, обычно считающимися «дружелюбными», такими как Limosilactobacillus и Weissella cibaria, что указывает на сообщество кишечных микробов в хрупком, меняющемся равновесии.
После операции: развилка в микробном развитии событий
К 30‑му дню после операции микробиота пациентов, избежавших инфекции, сформировала один узнаваемый паттерн, тогда как у пациентов, у которых развились инфекции, картина была совсем иная. У неинфицированных пациентов сообщества микробов были более богатыми и равномерными, с множеством представителей рода Blautia и родственных бактерий, вырабатывающих бутират — короткоцепочечную жирную кислоту, известную тем, что питает клетки кишечника и поддерживает иммунную стабильность. Их кишечные экосистемы выглядели разнообразными и сбалансированными. У пациентов с инфекциями, напротив, диверсификация снизилась, и сообщество доминировало Enterococcus faecium — выносливая бактерия, часто встречающаяся при госпитальных инфекциях и известная своей устойчивостью к антибиотикам. Статистический анализ показал, что микробные сообщества этой группы значительно отличались от всех остальных, что указывает на явную послеоперационную дисбактерию.
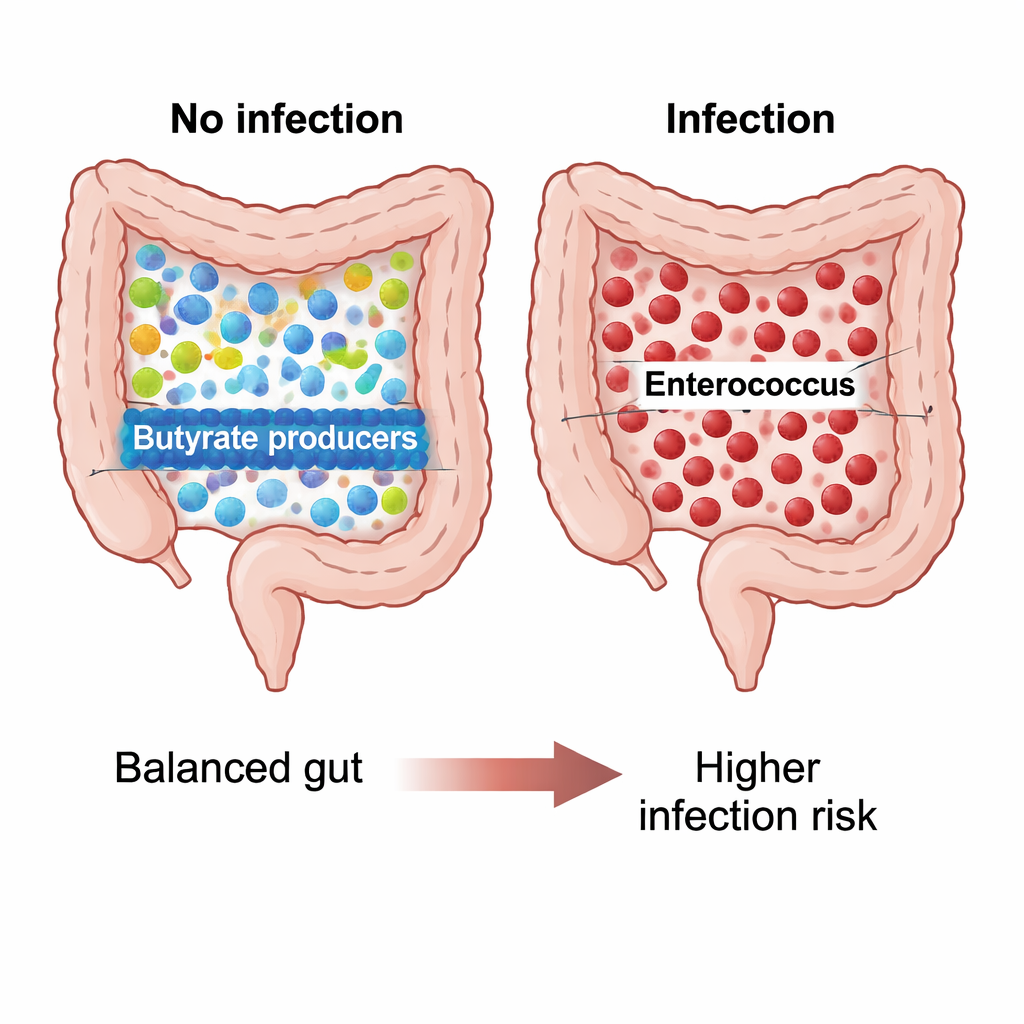
Микробная химия, связанная с защитой или риском
Ученые также выясняли, какие химические функции эти микробы могли бы выполнять. С помощью предиктивного программного обеспечения они обнаружили, что у неинфицированной группы после операции Blautia связывается с метаболическими путями, расщепляющими соединение L‑1,2‑пропандиол — промежуточный продукт ферментации клетчатки, который в конечном счёте участвует в образовании полезных жирных кислот, таких как пропионат. У инфицированных пациентов этот прогнозируемый метаболический потенциал был заметно ниже, что согласуется с идеей, что их кишечное сообщество менее способно вырабатывать защитные молекулы. До операции Enterococcus casseliflavus у инфицированных пациентов ассоциировался с необычными ферментационными путями, что может отражать напряжённую, испытывающую дефицит энергии микробную среду — однако это требует подтверждения в лабораторных экспериментах.
Что это означает для пациентов и клинических команд
Для людей, которым предстоит трансплантация сердца, эти результаты подразумевают, что кишечник — не просто наблюдатель: он может влиять на риск опасных инфекций. Исследование показывает динамическое смещение от доминирования Bacteroides до операции к либо защитному обогащению Blautia, либо вредоносному разрастанию Enterococcus после операции, в зависимости от того, как проходит ранний период восстановления. Сильный стресс, связанный с инфекциями, и приём антибиотиков, по‑видимому, сдвигают сообщество в сторону низкодивергентного состояния, доминируемого Enterococcus, наблюдаемого у инфицированных пациентов. Авторы предлагают «двойную цель»: поддерживать восстановление бактерий, вырабатывающих бутират — возможно, с помощью диеты или тщательно подобранных пробиотиков, — одновременно внимательно следя за уровнями Enterococcus. Хотя нужны более масштабные и длительные исследования, эта работа открывает путь к тому, чтобы настройка микробиоты кишечника стала рутинной частью защиты пациентов от угрожающих жизни инфекций после трансплантации.
Цитирование: Han, J., Hua, L., Yang, B. et al. Gut microbiota and metabolic pathway profiles in infected and non-infected heart transplant patients before and after surgery. Sci Rep 16, 7697 (2026). https://doi.org/10.1038/s41598-026-38911-y
Ключевые слова: трансплантация сердца, микробиота кишечника, послеоперационная инфекция, антибиотики, бактерии, вырабатывающие бутират