Clear Sky Science · ru
Сигнальная система Wnt/β-катенин формирует поведение макрофагов при повреждении и восстановлении поднижнечелюстной железы у мышей
Почему сухость во рту важна
Ксеростомия, или хроническая сухость во рту, — это не просто мелкое неудобство. Она может делать приём пищи болезненным, затруднять речь и значительно повышать риск инфекций и кариеса. У многих людей развивается выраженная сухость во рту после лучевой терапии головы и шеи или при аутоиммунных заболеваниях, таких как синдром Шёгрена. Повреждённые слюнные железы часто заживают плохо, и нынешние методы лечения в основном ослабляют симптомы, но не восстанавливают функцию. Это исследование изучает, как конкретная группа иммунных клеток — макрофаги — и ключевой путь межклеточной связи Wnt/β‑катенин совместно определяют, будет ли повреждённая слюнная железа рубцеваться или регенерировать.
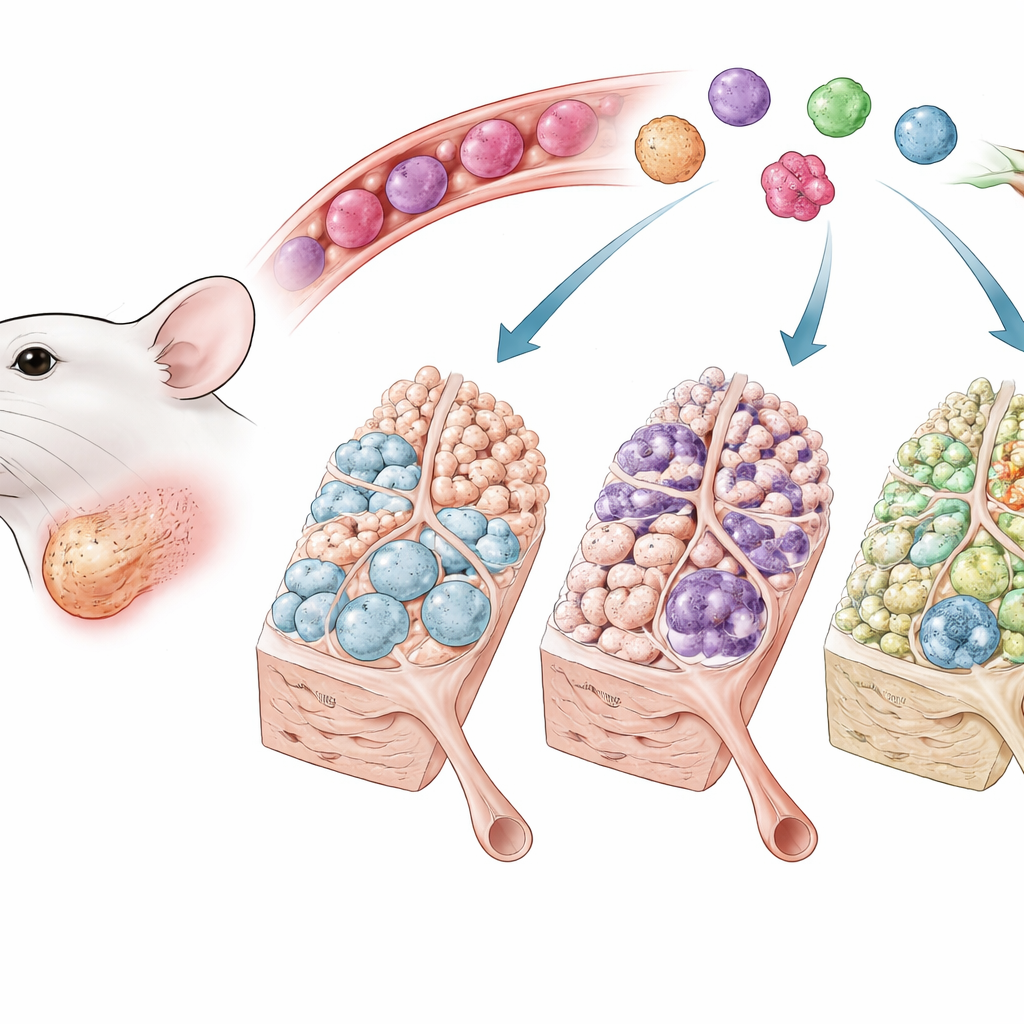
Стражи у ворот
Слюнные железы состоят из многочисленных ацинусов, которые вырабатывают слюну, и выводных протоков, по которым она попадает в ротовую полость. При закупорке главного протока эти хрупкие структуры спадаются, ткань воспаляется, и накапливается волокнистая рубцовая ткань. Макрофаги — первичные иммунные клетки, устремляющиеся в повреждённую ткань; они могут либо подогревать воспаление и рубцевание, либо способствовать спокойному, упорядоченному восстановлению. Авторы использовали хорошо зарекомендовавшую модель на мышах, в которой главный проток поднижнечелюстной железы временно пережимают, имитируя обструктивное повреждение, а затем вновь открывают для восстановления. Они сочетали эту модель с генетическими репортёрными мышами, которые светятся при активации Wnt/β‑катенин‑сигнализации, что позволило увидеть, какие клетки «слышат» этот сигнал после повреждения.
Сигналы в поддерживающих тканях
После закупорки протока исследователи наблюдали драматические повреждения ткани: потерю ацинусов, вздутие протоков и утолщённую капсулу, богатую коллагеном. Одновременно отмечался всплеск Wnt‑реагирующих клеток не внутри слюнообразующих единиц, а преимущественно в поддерживающей строме — в капсуле, внутренних перегородках и пространствах между протоками и ацинусами. Большинство этих Wnt‑реагирующих клеток несли маркеры иммунных клеток и макрофагов, что указывает на то, что макрофаги составляют значительную Wnt‑активную популяцию при повреждении. Измерения экспрессии генов во временном разрезе показали, что как ген‑ответ на Wnt (Axin2), так и маркер макрофагов (F4/80) достигают пика примерно на третьи и шестые сутки после повреждения, свидетельствуя о тесной связи между приходом макрофагов и активацией Wnt‑сигнализации на ранних и средних этапах восстановления.
Макрофаги — и отправители, и получатели
Чтобы выяснить, откуда исходят Wnt‑сигналы, команда измерила все известные гены Wnt в повреждённых железах. Несколько из них были повышены, причём Wnt2 и Wnt2b особенно выделялись увеличением на третьи и шестые сутки. Микроскопия показала, что эти белки Wnt присутствуют внутри макрофагов, что предполагает: одни и те же клетки, выделяющие Wnt‑сигналы, также на них реагируют. Дальнейшие эксперименты показали, что многие из Wnt‑активных макрофагов были недавно рекрутированы из кровотока, а не были долгоживущими резидентами железы. По сути, повреждение привлекает новые макрофаги, которые затем включают Wnt‑опосредованный петлевой механизм, потенциально влияющий на их поведение и на то, как окружающие поддерживающие клетки перестраивают ткань.
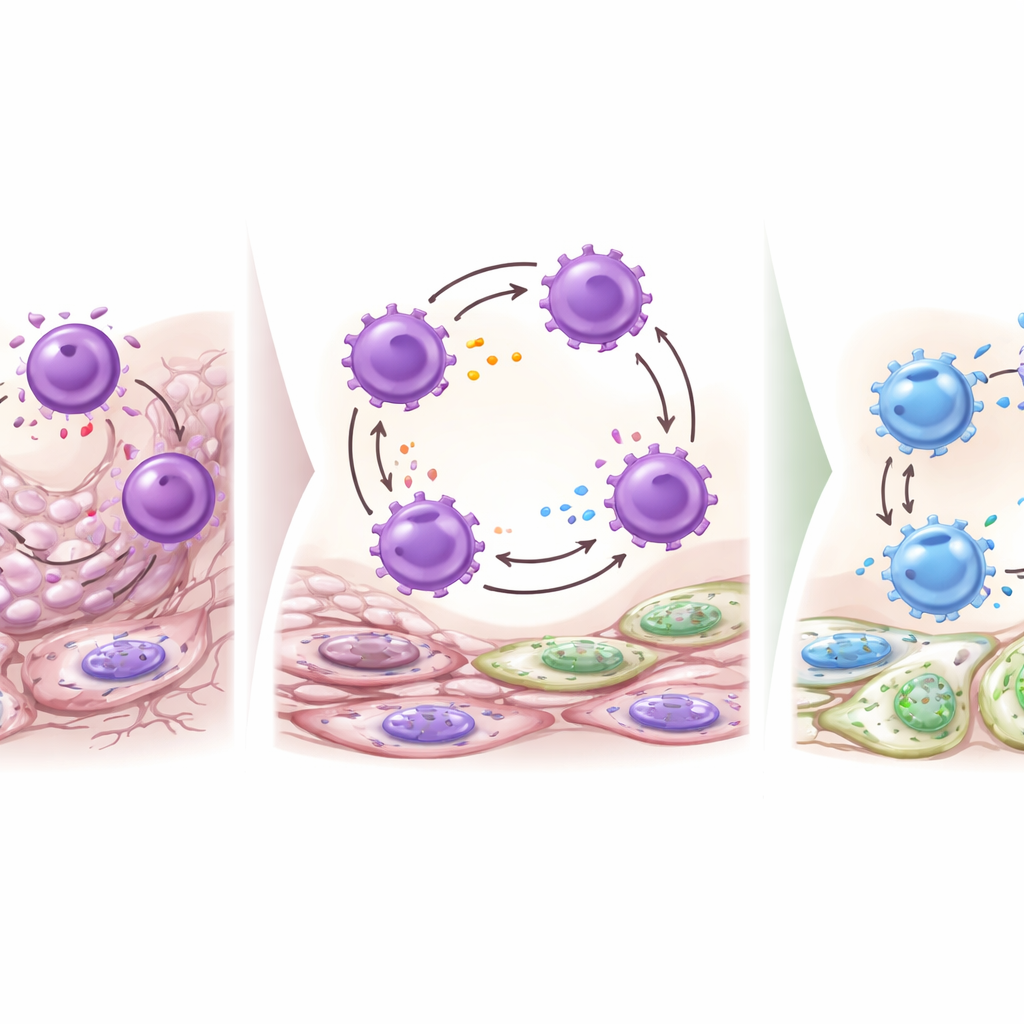
Рубцевание против мягкого заживления
Авторы также проверили, восстанавливают ли Wnt‑реагирующие клетки сами ацинусы, производящие слюну. Несмотря на сильную Wnt‑активность в строме и клетках протоков после повреждения, эксперименты по прослеживанию родословной показали, что эти помеченные по Axin2 клетки не превращались в новые ацинусы после повторного открытия протока и восстановления железы. Вместо этого они преимущественно участвовали в поддержании протоковой системы. Чтобы проверить, как Wnt‑сигнализация влияет на качество восстановления, команда частично подавляла секрецию Wnt‑лигандов, удаляя ген Wntless (Wls) либо повсеместно, либо специфически в Wnt‑реагирующих клетках. У таких мышей повреждённые железы имели более тонкие фиброзные капсулы, меньше расширенных протоков и заметное увеличение числа CD206‑положительных макрофагов — популяции, обычно ассоциируемой с более восстановительным, про‑лечебным профилем. Это предполагает, что снижение выхода Wnt сдвигает макрофагов в сторону более мягкого, менее рубцующего ответа.
Что это значит для людей с сухостью во рту
В совокупности результаты показывают Wnt/β‑катенин‑сигнализацию как ключевой переключатель, который помогает определить, будут ли макрофаги в повреждённой слюнной железе способствовать вредному фиброзу или более конструктивному восстановлению. Макрофаги в этой системе, похоже, напрямую не восстанавливают клетки, производящие слюну, но их сигналы сильно влияют на баланс между рубцеванием и регенерацией в поддерживающем каркасе железы. У пациентов с лучевой ксеростомией или аутоиммунными поражениями слюнных желез аккуратно направленное влияние на Wnt‑сигнализацию в макрофагах — вместо тотального устранения этих клеток — могло бы в будущем помочь уменьшить рубцевание, восстановить более здоровую архитектуру ткани и улучшить функцию железы. Эта работа закладывает механистическую основу для терапий, нацеленных на изменение среды заживления слюнной железы, а не только на замену утраченных структур.
Цитирование: Ahmed, A., Sachdeva, S., Whawell, S. et al. Wnt/β -catenin signalling shapes macrophage behaviour during injury and repair in the mouse submandibular gland. Sci Rep 16, 8972 (2026). https://doi.org/10.1038/s41598-026-38873-1
Ключевые слова: восстановление слюнной железы, макрофаги, Wnt‑сигнализация, фиброз, ксеростомия