Clear Sky Science · ru
Кадмий вызывает ферроптоз в сперматоцитах мыши через активацию пути ROS–ЦТК
Почему обычный металл важен для мужского здоровья
Кадмий — мягкий металл, используемый в батареях, пигментах и других промышленных изделиях. Он может накапливаться в почве, воде и пище, постепенно попадая в наши организмы. Многие исследования связывают воздействие кадмия с уменьшением числа сперматозоидов и ухудшением их качества у мужчин, но точный механизм повреждения клеток, создающих сперму, оставался неясным. В этом исследовании подробно изучили проблему и выяснили, как кадмий направляет сперматоциты мышей по специфическому пути клеточной гибели, связанному с железом и перенапряжением энергетической системы в митохондриях — «электростанциях» клетки.
От загрязнения до уязвимых сперматоцитов
Кадмий давно известен как вредный фактор для мужской репродуктивной системы. У мужчин, подвергшихся воздействию на рабочем месте или проживающих в загрязнённых районах, часто отмечают снижение количества сперматозоидов, их подвижности и нормальной формы, а также повреждения ДНК в сперме. Животные исследования подтверждают эти данные: наблюдают уменьшение размеров тестикул, нарушение защитных барьеров, снижение тестостерона и массовую гибель зародышевых клеток. Ранее авторы заметили, что кадмий способен вызывать редкую железозависимую форму гибели клеток — ферроптоз — в тестикуллярной ткани. В настоящей работе они сосредоточились на сперматоцитах мыши — клетках в процессе превращения в сперматозоиды — чтобы понять, как именно кадмий повреждает их и играет ли роль этот железосвязанный путь гибели.
Перегрузка железом и особая форма гибели клеток
Для изучения механизма группа выращивала линию сперматоцитов мыши в культурах и подвергала клетки воздействию кадмия, с добавлением или без препаратов, известных как блокаторы ферроптоза. Кадмий примерно наполовину снизил выживаемость клеток и замедлил их деление. Внутри клеток резко увеличились уровни свободного железа и маркера окислительного повреждения липидов — малондиальдегида, тогда как ключевой защитный фермент GPX4 сократился. Другие белки, участвующие в хранении и выведении железа, возросли, что указывает на серьёзные сбои в обработке железа. При добавлении ингибиторов ферроптоза — хелатора железа и молекулы, защищающей липиды, — многие из этих вредных изменений ослабевали, а выживаемость клеток улучшалась. В совокупности эти сдвиги соответствуют подписи ферроптоза, что указывает на то, что кадмий убивает клетки не абстрактно, а направляет их в эту специфическую железо‑ и липидозависимую программу гибели.
Митохондрии под ударом
Ситуация углубилась, когда учёные обратили внимание на митохондрии — энергетические центры, которые также производят побочные продукты в виде реактивных форм кислорода (ROS). Под микроскопом здоровые клетки демонстрировали длинные нитевидные митохондрии, тогда как у клеток, подвергшихся кадмию, митохондрии были короткими и фрагментированными — признак структурного повреждения. Измерения подтвердили всплеск митохондриального ROS и падение электрического потенциала митохондриальной мембраны — ключевого показателя функции. Клетки реагировали повышением внутренних защитных систем, включая белки, регулируемые стрессовым сенсором Nrf2, но этих мер оказалось недостаточно. Важно, что препараты-ингибиторы ферроптоза снижали митохондриальный ROS и частично восстанавливали здоровье митохондрий, напрямую связывая повреждение «электростанций» с железозависимым путём гибели.
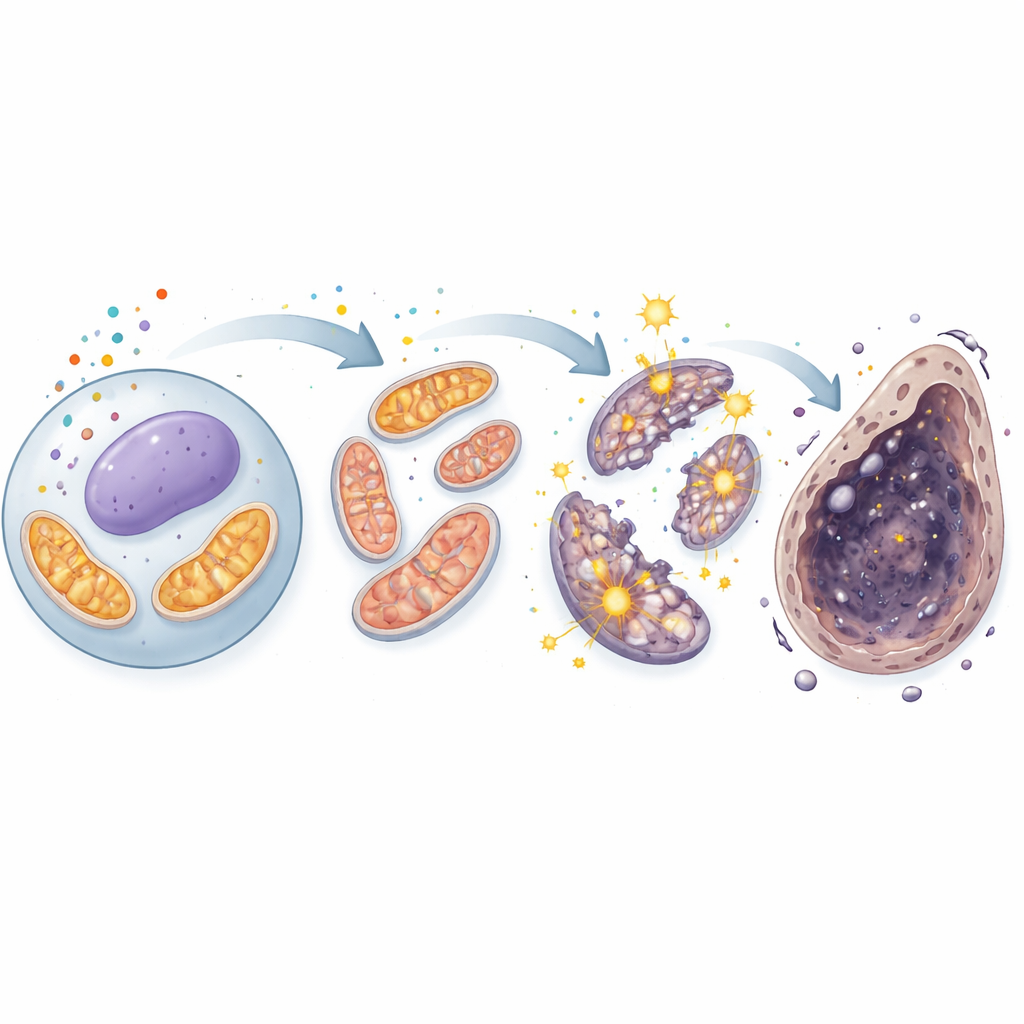
Порочный круг в «электростанции» клетки
Сочетая профилирование активности генов и измерения метаболитов, исследователи обнаружили, что кадмий делает не только прямой вред митохондриям — он, по-видимому, перенастраивает их основной энергетический цикл, цикл трикарбоновых кислот (ЦТК). Уровни двух ключевых промежуточных соединений ЦТК — α‑кетоглутарата и сукцината — заметно возросли, а активность пируваткарбоксилазы, фермента, подающего «свежее топливо» в цикл, усилилась. Это указывает на то, что ЦТК в повреждённых клетках парадоксально оказался гиперактивным, заставляя больше электронов проходить через дыхательную цепь и усиливая утечку ROS. Эти дополнительные ROS затем взаимодействовали с железом и повреждали мембраны, укрепляя ферроптоз. Опять же, ингибиторы ферроптоза ослабляли эти метаболические искажения, подчёркивая тесную связь между кадмием, митохондриальным разгоном и железозависимой гибелью клеток.
Что это значит для фертильности и дальнейших исследований
Проще говоря, исследование показывает, что кадмий атакует сперматоциты, напрямую повреждая их митохондрии и выбивая энергетический цикл из равновесия. Эта комбинация заливает клетки реактивными формами кислорода и нарушает баланс железа, подталкивая их к ферроптозу. Поскольку сперматоциты необходимы для производства здоровой спермы, их потеря может помочь объяснить сильную связь между воздействием кадмия и сниженной мужской фертильностью. Хотя эксперименты проведены на клетках мыши в культуре, они дают ясную механистическую карту, которую можно проверить в будущих исследованиях на животных и людях. Работа также указывает на возможные защитные стратегии: препараты или нутриенты, которые снижают митохондриальный стресс, корректируют ЦТК или предотвращают железозависимое повреждение мембран, могут помочь защитить мужскую репродуктивную систему от воздействия таких окружающих металлов, как кадмий.
Цитирование: Xiong, L., Yi, L., Zeng, X. et al. Cadmium induces ferroptosis in mouse spermatocytes by activating the ROS–TCA pathway. Sci Rep 16, 8449 (2026). https://doi.org/10.1038/s41598-026-38827-7
Ключевые слова: токсичность кадмия, мужская фертильность, митохондриальный стресс, ферроптоз, реактивные формы кислорода