Clear Sky Science · ru
Вычислительная оптимизация растворимости калапина DEK1 посредством интегрированного структурного моделирования и обучения, ориентированного на направленную мутагенезу
Почему важно заставить растительные белки вести себя предсказуемо
Многие белки, контролирующие рост растений, — это крупные, хрупкие молекулы, которые отказываются растворяться, когда учёные пытаются изучить их в лаборатории. Один из таких белков, называемый DEK1, формирует тело растения, начиная от отдельных клеток и выше. Но потому что ключевая часть DEK1 агрегирует при продукции в бактериях, её трёхмерная структура оставалась неизвестной, что замедляло попытки понять и использовать этот белок. В этом исследовании показано, как компьютерное моделирование и умный, основанный на данных дизайн могут перестроить проблемный участок, сделав его более растворимым, не нарушив при этом его строение — предлагая общий рецепт по приручению трудно выражаемых белков.
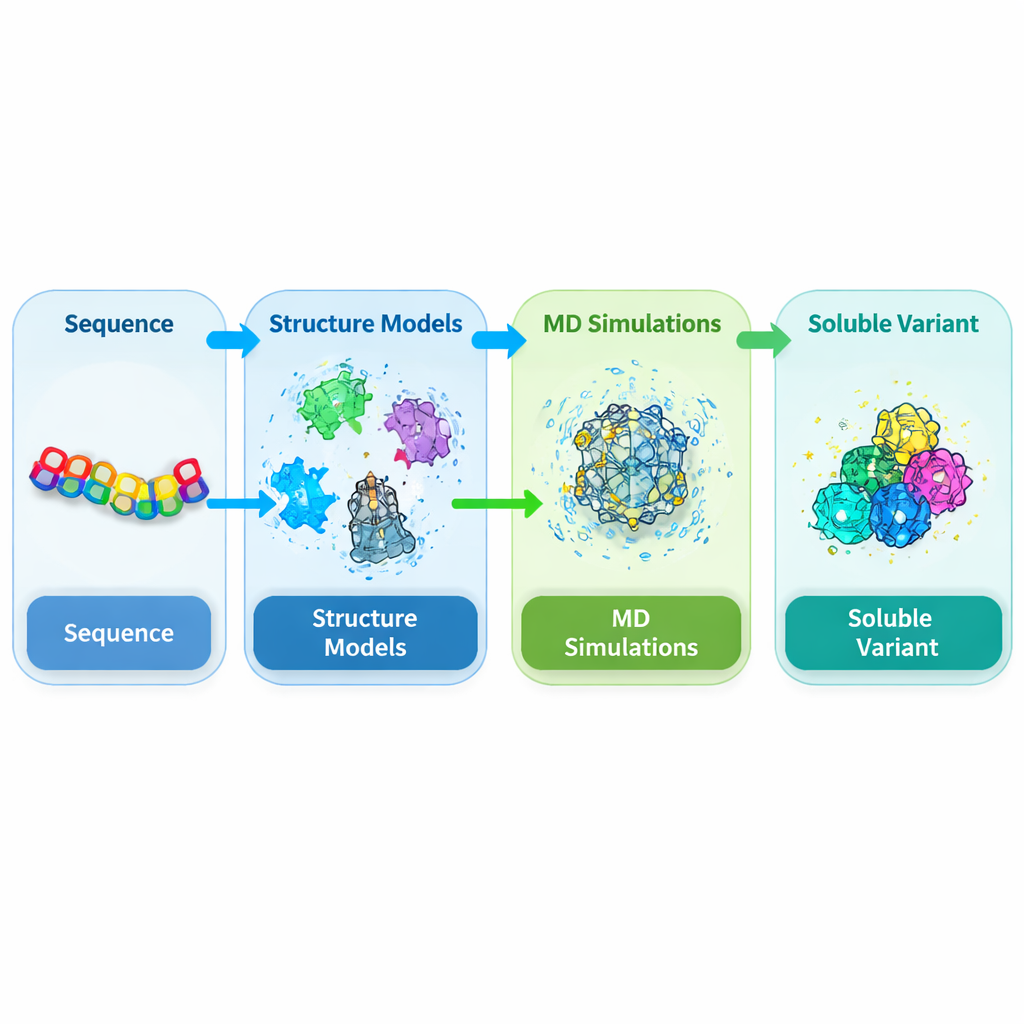
Нацеливание на проблемный участок в ключевом растительном белке
DEK1 — необычно крупный белок, встроенный в мембраны клеток и заканчивающийся каталитическим участком, известным как калапиновый домен. Генетические исследования показали, что этот домен необходим для нормального развития таких растений, как мхи и сельскохозяйственные культуры, однако его структура никогда не была экспериментально разрешена. Когда учёные пытаются получить этот калапиновый «ядро» (называемое CysPc) в обычном бактериальном хозяине Escherichia coli, оно склонно становиться нерастворимым и образовывать плотные включения. Это делает практически невозможным очистку в объёмах и качестве, необходимых для детальных структурных и функциональных исследований. Авторы поэтому поставили задачу переработать домен CysPc так, чтобы он легче растворялся, сохраняя при этом свою общую форму.
Построение надёжной 3D-модели с нуля
Поскольку для этого растительного калапина не существовало экспериментальной структуры, команде сначала пришлось предсказать его трёхмерную форму. Они объединили несколько современных инструментов предсказания структур, включая AlphaFold2, SWISS-MODEL и I-TASSER, и привязали эти предсказания к известным структурам родственных млекопитающих калапинов. Используя консенсусный подход, они уточняли и проверяли полученные модели с помощью множества тестов качества, оценивающих геометрию основной цепи, упаковку и соответствие известным структурным закономерностям. Эти независимые проверки показали, что интегрированная модель домена CysPc была надёжнее любой отдельной предсказанной структуры, предоставляя прочную отправную точку для изучения того, как небольшие изменения аминокислотной последовательности могут улучшить растворимость.
Тестирование виртуальных мутаций в смоделированном растворителе
Имея 3D-модель, авторы провели обширные молекулярно-динамические симуляции, в которых белок и окружающие молекулы воды отслеживались со временем на компьютере. Они сосредоточились на остатках на поверхности белка, которые были подвижными, гидрофобными или предположительно способствовали агрегированию. Кандидатные позиции мутилировали поодиночке в более водоориентированные аминокислоты и затем симулировали по 200 наносекунд для каждого варианта. Для каждой версии измеряли признаки, связанные с растворимостью, такие как площадь поверхности, контактирующая с водой, насколько компактен белок и насколько сильно флуктуируют атомы. Многие одиночные мутации умеренно увеличивали контакт с растворителем или внутренние водородные связи, оставляя при этом общую укладку неизменной, что указывает на то, что базовый каркас CysPc может переносить тщательно подобранные замены.
Позволяя алгоритмам искать в пространстве мутаций
Изменение всего одного остатка редко даёт существенный эффект на растворимость, поэтому исследователи далее изучили комбинации из двух и трёх мутаций. Они сгенерировали библиотеку двойных и тройных вариантов, построенных из лучших одиночных мутаций, и снова симулировали каждый вариант. Для справедливой оценки и ранжирования дизайнов они определили взвешенный индекс, который объединяет несколько признаков симуляции, известных своей корреляцией с растворимостью, поощряя усиление гидратации и внутренних связей и штрафуя чрезмерную подвижность. Затем использовали алгоритм обучения с подкреплением (Proximal Policy Optimization), чтобы пробраться через огромное пространство возможных тройных мутантов и предложить наиболее перспективные комбинации. Этот поиск, основанный на данных, сошёлся на конкретном тройном мутанте, названном MUT347, в качестве лучшего кандидата.
Более компактная, лучше гидратированная версия фермента
Детальные симуляции дикого типа домена CysPc и MUT347 показали, чем отличается сконструированный вариант. MUT347 быстрее выходил на равновесие и демонстрировал меньшие общие отклонения от исходной формы, что указывает на большую структурную стабильность в растворе. Его петли и концы цепей были несколько менее «болтливыми», в то время как ядро каталитического региона сохранило свою исходную подвижность, предполагая сохранение функционально важных движений. Тройной мутант имел больше внутренних водородных связей и большую доступную для воды поверхность в ключевых областях — признаки более упорядоченной и лучше гидратированной поверхности. При различных концентрациях солей и уровнях pH MUT347 последовательно сохранял меньшие флуктуации по сравнению с оригинальным белком, поведение, связанное со сниженной склонностью к агрегированию.
Что это значит для изучения и повторного использования белков
Для неспециалистов ключевой вывод заключается в том, что авторы создали в основном компьютерный рецепт превращения неловкого, скапливающегося фрагмента жизненно важного растительного белка в более растворимую, предсказуемую версию, без необходимости иметь его экспериментальную структуру заранее. Объединив современные методы предсказания структур, длительные симуляции и алгоритмы обучения, способные одновременно учитывать множество дизайнерских решений, они идентифицировали тройную мутацию, которая, по прогнозам, стабилизирует укладку и делает поверхность более благоприятной для взаимодействия с водой. Хотя экспериментальные работы по-прежнему необходимы для подтверждения выигрышей в реальных пробирках, эта рамочная методика может быть широко полезна для спасения других трудно выражаемых эукариотических белков, в конечном счёте помогая учёным раскрывать структуры и функции, которые сейчас недоступны.
Цитирование: Dabiri, M., Levarski, Z., Struhárňanská, E. et al. Computational optimization of DEK1 calpain domain solubility through integrated structural modelling and data-driven targeted mutagenesis. Sci Rep 16, 7767 (2026). https://doi.org/10.1038/s41598-026-38805-z
Ключевые слова: растворимость белков, вычислительный мутагенез, молекулярная динамика, растительный калапин DEK1, инжиниринг белков