Clear Sky Science · ru
Определяющие на уровне остатков факторы термостабильности экстремофильной эндолизины Ts2631
Почему вирусы, любящие жару, важны для будущих антибиотиков
По мере роста устойчивости к антибиотикам учёные ищут новые способы уничтожения опасных бактерий. Обещающий подход заимствует «орудия» у вирусов, инфицирующих бактерий — бактериофагов. Эти вирусы производят ферменты, называемые эндолизинами, которые пробивают стенки бактерий. В обсуждаемом исследовании рассматривается исключительно термостабильная эндолизина Ts2631, взятая из вируса, обитающего в исландских горячих источниках. Выявляя отдельные строительные блоки белка, обеспечивающие его устойчивость при температурах близких к кипению, исследователи надеются спроектировать более прочные и долговечные антибактериальные ферменты для медицины и биотехнологии. 
Вирусный инструмент, закалённый в кипящих источниках
Ts2631 происходит от бактериофага, инфицирующего термофильную бактерию Thermus scotoductus, которая процветает в воде с температурами значительно выше 60 °C. Фермент Ts2631 расщепляет определённую связь в пептидогликане — жёсткой сети, окружающей бактериальную клетку. Особенность Ts2631 — её экстремальная термостабильность: белок сохраняет свёрнутое состояние примерно до 100–105 °C, в зависимости от раствора. Это значительно выше температур, при которых большинство белков денатурирует. Авторы сравнили Ts2631 с её наилучше изученным «родственником» из вируса умеренных температур, лизоцимом T7, чтобы выяснить, какие структурные приёмы использовала природа, чтобы сохранить Ts2631 целой в таких жёстких условиях.
Короткие петли и другой набор строительных блоков
Белки состоят из цепочек 20 типов аминокислот, свернутых в сложные формы. При наложении трёхмерных структур Ts2631 и лизоцима T7 исследователи обнаружили, что общая архитектура очень похожа: у обоих есть компактное ядро из спиралей и β-цепей. Ключевое различие — гибкие петли, соединяющие эти элементы. В Ts2631 петли короче и менее подвижны, тогда как у лизоцима T7 они длиннее и более «вялые». В Ts2631 также больше некоторых аминокислот, часто связанных с термостойкостью: жёсткого пролина; ароматических остатков, таких как тирозин и триптофан; и положительно заряженного аргинина. Одновременно в ней меньше серина, аспарагиновой и глутаминовой кислот, которые могут делать белки более уязвимыми при высоких температурах. Эта закономерность подтверждается не только при сравнении с лизоцимом T7, но и при сопоставлении Ts2631 со стами тысяч вирусных и миллионами бактериальных белков.
Замена отдельных аминокислот для проверки их значения
Чтобы перейти от корреляции к причинно-следственным связям, команда систематически заменяла 55 отдельных аминокислот в Ts2631 и измеряла, как каждая мутация влияет на температуру плавления (Tm) и способность фермента разрушать бактериальные стенки. Некоторые изменения вокруг цинксодержащего активного центра оказались особенно разрушительными. При изменении трёх остатков, координирующих цинк (H30, H131 и C139), Tm белка падала примерно до 20 °C, и активность терялась. Два консервативных тирозина (Y60 и Y69) также вносили вклад в стабильность. Что удивительно, удаление дисульфидной связи — ковалентной связи между цистеинами C80 и C90 — фактически повысило температуру плавления, хотя и разрушило активность. Это показывает, что высокая стабильность в пробирке не всегда означает улучшенную функциональность белка в реальных условиях. 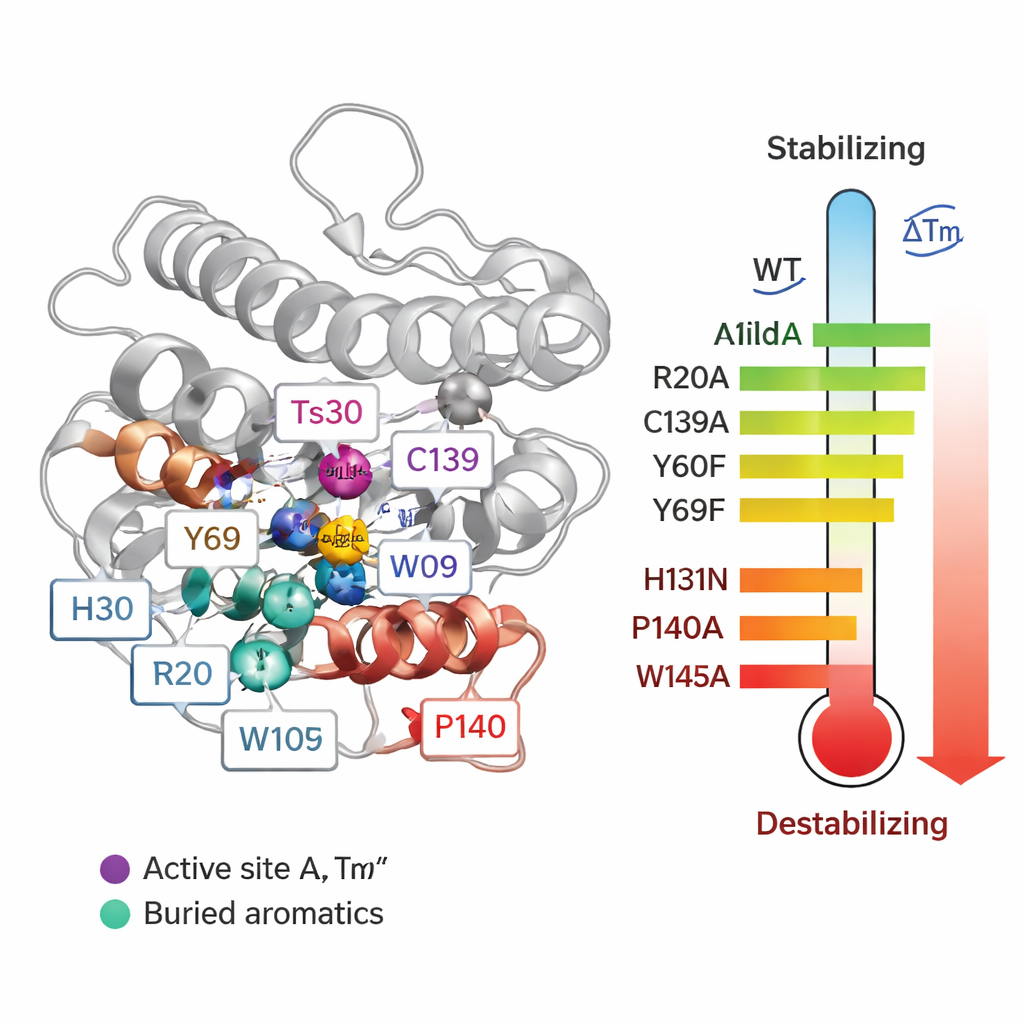
Скрытые ароматические «якоря» и ключевой захват бактериальной стенки
Наиболее поразительные результаты получены при мутациях пролина и триптофана. Замена одного пролина (P140), расположенного рядом с цинк-связывающей C139, снизила Tm более чем на 21 °C и ослабила активность после нагрева, поскольку мутация нарушила особую геометрию связи, необходимую для правильного связывания металла. Несколько глубоко спрятанных триптофанов (W102, W109 и особенно W145) также оказались критическими: замена их на аланин вызвала падение Tm на 14–24 °C и сделала фермент гораздо более чувствительным к нагреву в тестах активности. Эти ароматические остатки действуют как внутренние якоря, фиксирующие ядро белка. Среди аргининов большинство оказывало небольшое влияние на стабильность, но R20 оказался необходим для захвата пептидогликана. При замене R20 фермент плохо связывал бактериальную стенку и терял активность при нагреве, показывая, что некоторые остатки больше влияют на функцию, чем на чистую термостойкость.
От ферментов горячих источников к более прочным антибактериальным средствам
В сумме исследование показывает, что выдающаяся термостойкость Ts2631 опирается на небольшое число удачно расположенных аминокислот, а не на равномерное усиление всего белка. Остатки, связывающие цинк, консервативный пролин вблизи активного центра и погружённые ароматические боковые цепи формируют стабилизирующее ядро, тогда как некоторые классические стабилизирующие элементы, такие как дисульфидные связи или солевые мостики, здесь менее важны, чем ожидалось. Для более широкой области это означает, что месофильные (умеренно-температурные) эндолизины можно сделать более долговечными, аккуратно заменяя отдельные позиции на триптофан или пролин без ущерба для бактерицидной активности. Иными словами, изучая, как природа строит ферменты, устойчивые к почти кипящим температурам, учёные получают практическую схему для проектирования более надёжных и долгоживущих белковых антибиотиков.
Цитирование: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
Ключевые слова: термостабильная эндолизина, ферменты бактериофагов, термостабильность белков, антибиотикорезистентность, инженерия белков