Clear Sky Science · ru
Исследование биомаркеров, связанных с трансформацией сосудистых гладкомышечных клеток в пенистые клетки под действием гомоцистеина
Почему закупорка артерий начинается с крошечных изменений в клетках
Атеросклероз — медленное забивание и уплотнение артерий — является одной из ведущих причин инфарктов и инсультов. Обычно говорят о холестерине и питании, но реже — о том, как отдельные клетки стенки сосуда меняются по мере развития болезни. В этом исследовании подробно рассмотрен один такой триггер, молекула крови гомоцистеин, и показано, как он может подтолкнуть обычно спокойные мышечные клетки артерий накапливать жир и превращаться в так называемые пенистые клетки — строительные блоки опасных бляшек.
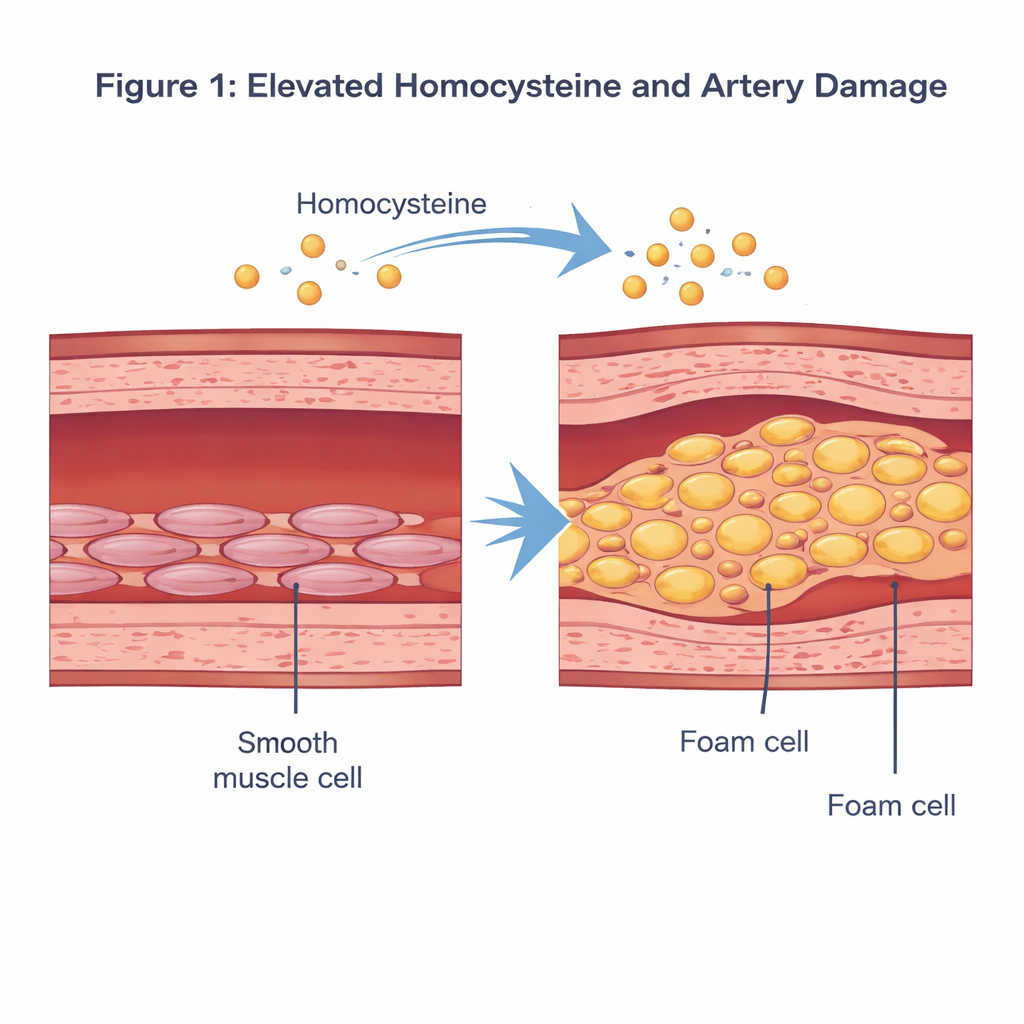
Аминокислотный «нарушитель» в кровотоке
Гомоцистеин — содержащая серу аминокислота, образующаяся при переработке организмом пищевой метионина. В норме ее уровень в крови низок. При повышении выше примерно 15 мкмоль/л — состоянии, называемом гипергомоцистеинемией — эпидемиологические исследования связывают это с повышенным риском сердечно‑сосудистых заболеваний. Ранее было показано, что избыток гомоцистеина может повреждать внутреннюю оболочку артерий, вызывать воспаление и изменять поведение сосудистых гладкомышечных клеток, которые находятся в среднем слое стенки сосуда и помогают регулировать артериальное давление за счет сокращения и расслабления.
Как мышечные клетки артерий превращаются в жиронасыщенные пенистые клетки
Исследователи сосредоточились на том, как гомоцистеин перестраивает эти гладкомышечные клетки. В лабораторных условиях они обрабатывали человеческие сосудистые гладкомышечные клетки дозой гомоцистеина, имитирующей патологическое состояние, и сравнивали их с необработанными клетками. С помощью обычных красителей и биохимических тестов они обнаружили, что клетки, обработанные гомоцистеином, заполнялись красными жировыми каплями, а уровни холестерина и триглицеридов резко возросли. Одновременно снизились белковые маркеры их обычной «сократительной» идентичности, а выросли маркеры более синтетического, образующего бляшки состояния. В совокупности эти изменения показывают, что гомоцистеин может отводить гладкомышечные клетки от их нормальной роли и направлять их к пенистоподобному, жиронасыщенному фенотипу, который напрямую способствует образованию бляшек.
Поиски молекулярных отпечатков внутри клеток
Чтобы понять, какие белки меняются в этой трансформации, команда обратилась к современной протеомике — технологии, позволяющей одновременно измерять тысячи белков. Они сравнили уровни белков в клетках, обработанных гомоцистеином, и в контроле и надежно количественно определили почти 4800 белков. Среди них 54 оказались существенно измененными: 13 повысились и 41 снизился. Многие из изменяющихся белков связаны с обращением липидов, выживанием клеток, окислительным стрессом и перестройкой клеточной структуры. Авторы затем использовали биоинформатические инструменты, чтобы сгруппировать эти белки по функциональным путям и построить карты их взаимодействий, выделив сети, связанные с метаболизмом холестерина и реакцией на стресс в стенке сосуда.
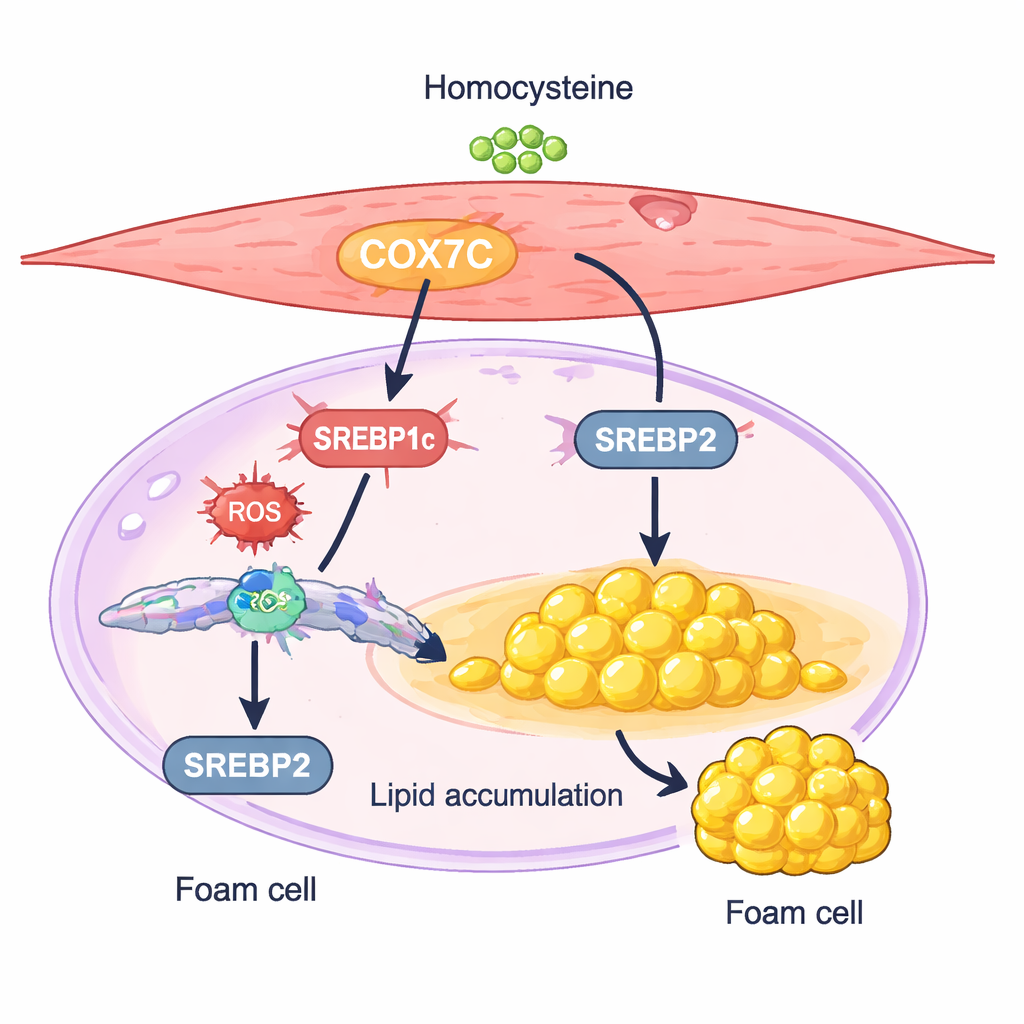
Митохондриальный переключатель, подталкивающий клетки к хранению жира
Один белок, называемый COX7C, выделился как особенно интересный подозреваемый. COX7C — компонент «энергетических станций» клетки, митохондрий, где он помогает управлять производством энергии. В гладкомышечных клетках, обработанных гомоцистеином, уровни COX7C были выше, чем в контроле. Исследователи показали, что дополнительное повышение COX7C ещё больше усиливало накопление жира в клетках и усиливало экспрессию двух главных регуляторов липидного синтеза — SREBP1c и SREBP2. Заглушение COX7C давало противоположный эффект: оно ослабляло активность SREBP, снижало накопление холестерина и триглицеридов и уменьшало изменения, характерные для пенистых клеток. Эти результаты поддерживают модель, в которой гомоцистеин повышает уровень COX7C в митохондриях, усиливает клеточные стресс‑сигналы и тем самым активирует SREBP‑опосредованный синтез липидов, сдвигая гладкомышечные клетки в состояние накопления липидов.
Что это значит для здоровья сердца и будущих терапий
Эта работа еще не доказывает, что то же самое происходит в артериях человека, и была выполнена в культурах клеток, а не на пациентах. Тем не менее она дает детальное представление о том, как повышенный гомоцистеин может способствовать превращению полезных мышечных клеток артерий в вредные пенистые клетки и выявляет COX7C и родственные белки как потенциальные биомаркеры или лекарственные мишени. Для неспециалиста главный вывод таков: помимо «хорошего» и «плохого» холестерина, небольшие изменения в химии крови — например, избыток гомоцистеина — могут перепрограммировать стенку сосуда изнутри. Указав на молекулярных игроков, таких как COX7C и путь SREBP, это исследование закладывает основу для будущих стратегий, направленных на предотвращение образования бляшек, удерживая артериальные клетки от превращения в миниатюрные депо для жира.
Цитирование: Wang, X., Ma, X., Zhang, X. et al. Study on biomarkers of homocysteine-induced transformation of vascular smooth muscle cells into foam cells. Sci Rep 16, 7411 (2026). https://doi.org/10.1038/s41598-026-38763-6
Ключевые слова: атеросклероз, гомоцистеин, пенистые клетки, сосудистые гладкомышечные клетки, COX7C