Clear Sky Science · ru
Ингибирование иммунных контрольных точек увеличивает антиген-специфический Т‑клеточный ответ при опухолях головы и шеи
Обращение защитных сил организма против рака головы и шеи
Опухоли головы и шеи остаются трудноизлечимыми, и даже мощные новые иммунотерапии помогают лишь небольшой части пациентов. В этом исследовании рассматривается перспективная идея: обучить иммунные клетки лучше распознавать раково-специфические сигналы, а затем снять с этих клеток молекулярные «тормоза», чтобы они могли эффективнее атаковать опухоли. Для людей, живущих с раком головы и шеи или находящихся в зоне риска, эта работа указывает путь к будущим вакцинам и сочетаниям препаратов, которые могли бы сделать текущие методы лечения более сильными и долговременными.
Почему современная иммунотерапия помогает немногим
Современная противораковая иммунотерапия часто нацелена на белки, называемые иммунными контрольными точками, которые действуют как тормоза на Т‑лимфоциты — белые кровяные клетки, способные уничтожать опухоли. При плоскоклеточном раке головы и шеи (HNSCC) уже применяются препараты, блокирующие PD‑1 — такие как Ниволумаб или Пембролизумаб. Тем не менее лишь около 20% пациентов получают от этого пользу, и у многих опухоль в конце концов прогрессирует. Авторы поставили задачу понять в контролируемой лабораторной модели, как блокада PD‑1 и родственных контрольных точек влияет на Т‑клетки, натренированные распознавать опухолевые маркеры, и добавляет ли комбинирование нескольких ингибиторов чего‑то сверх блокады PD‑1.
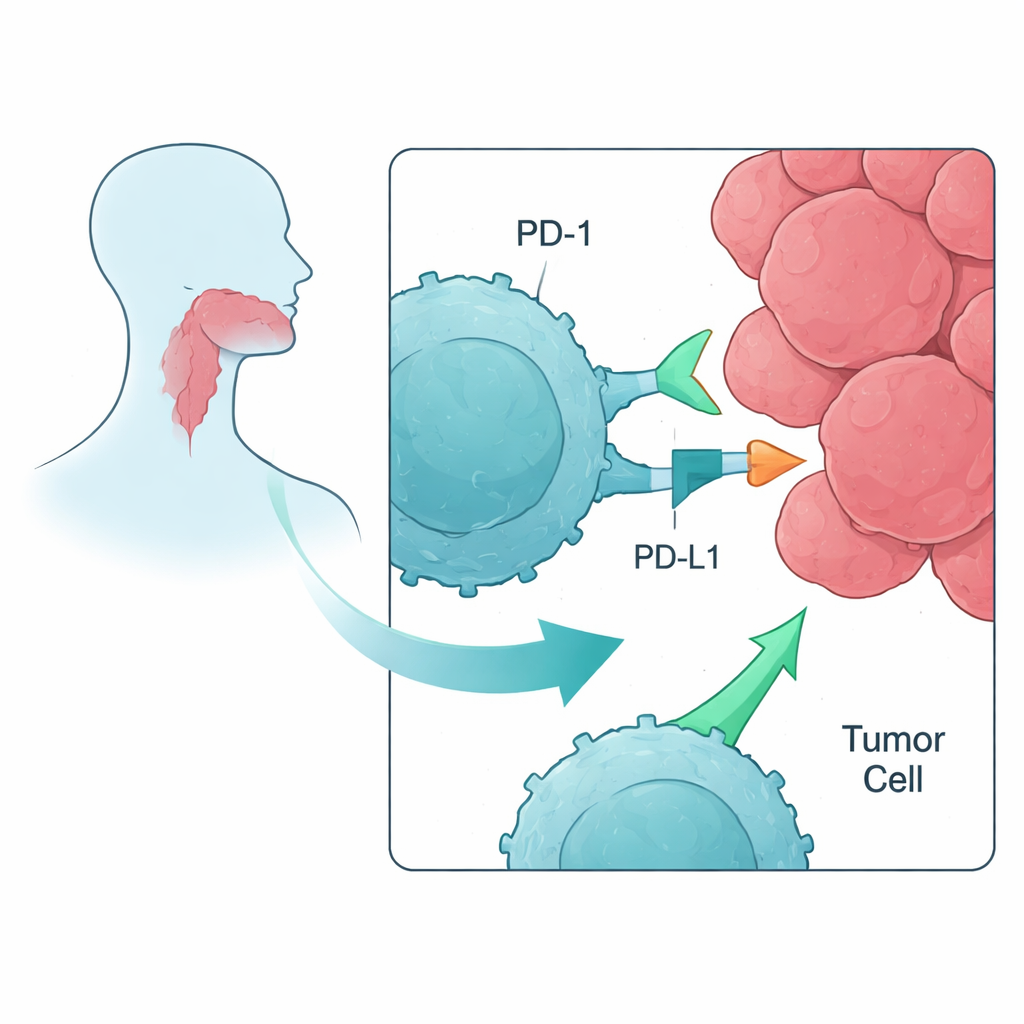
Обучение иммунных клеток распознавать раковые мишени
Исследователи начали с клеток крови здоровых добровольцев, а не пациентов, чтобы смоделировать, как менее поврежденная иммунная система может реагировать на ранней стадии болезни. Они выделили периферические мононуклеарные клетки крови, включающие Т‑клетки, и подвергли их воздействию коротких фрагментов белков — пептидов — взятых из опухолевых антигенов, обычно встречающихся при раке головы и шеи. Три таких мишени оказались особенно хороши в пробуждении Т‑клеток: MAGE, NY‑ESO‑1 и PRAME. В течение примерно недели в культурах лимфоцитов с пептидами эти фрагменты действовали как мини‑вакцины, расширяя редкие Т‑клетки, способные специфически распознавать каждый из связанных с опухолью маркеров.
Снятие тормозов с натренированных Т‑клеток
Далее команда проверила поведение этих натренированных Т‑клеток при контакте с реальными клетками рака головы и шеи в присутствии или отсутствии антител, блокирующих контрольные точки. Они использовали стандартный лабораторный тест (ELISPOT) для измерения выделения интерферона‑гамма и гранзима B — сигналов активации Т‑клеток и их способности убивать. У разных доноров добавление антитела против PD‑1 последовательно усиливало ответ антиген‑специфических Т‑клеток против опухолевой клеточной линии, часто увеличивая активность на 60–100% и более по сравнению с одной только пептидной стимуляцией. Напротив, блокада других контрольных точек, таких как LAG‑3 или TIM‑3, либо в одиночку, либо в сочетании с блокадой PD‑1, в этой системе давала мало или вовсе не давала дополнительного эффекта.
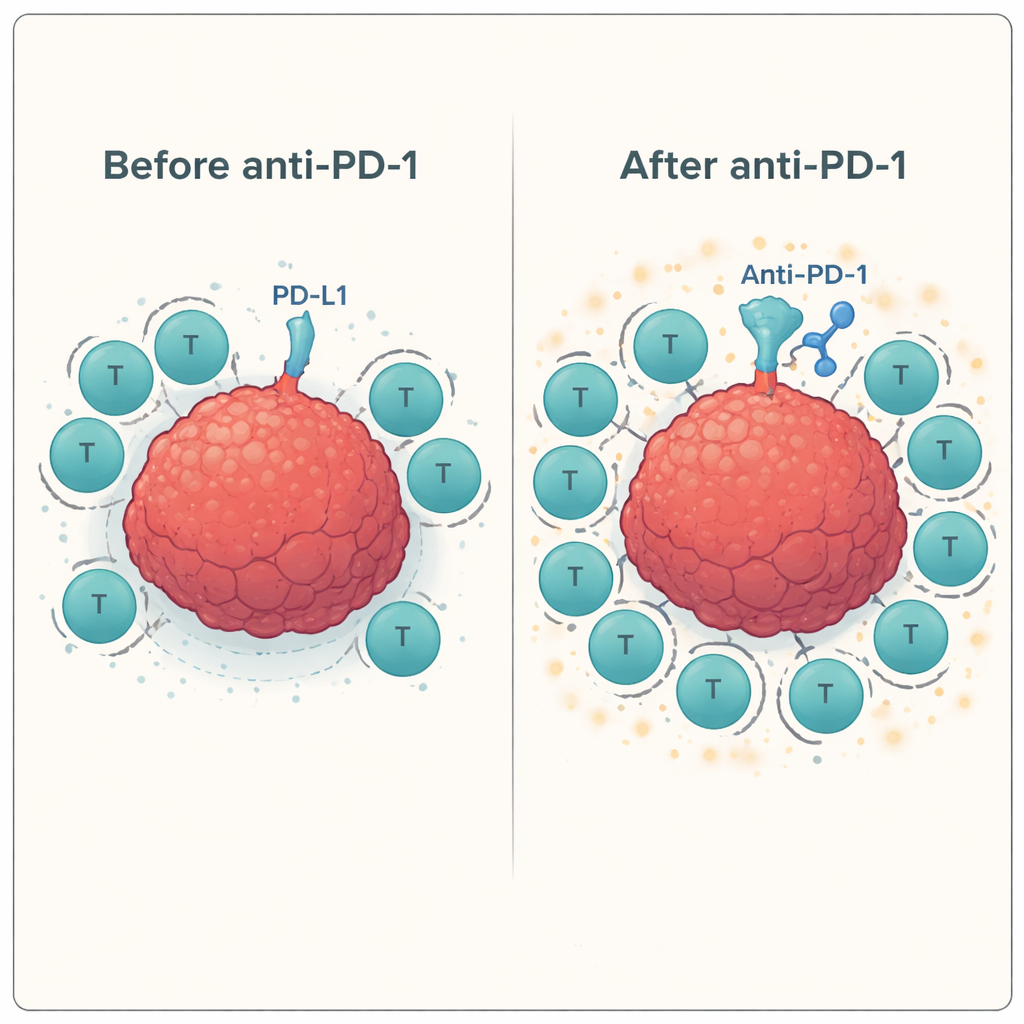
Детальная карта иммунного ландшафта
Чтобы понять, почему некоторые сочетания работали, а другие — нет, исследователи применили проточную цитометрию, метод подсчета и характеристики отдельных клеток. Они показали, что как Т‑клетки, так и опухолевые клетки экспрессируют PD‑1 и его лиганд(ы) PD‑L1 и PD‑L2 на значимых уровнях, создавая множество точек контакта, где тормоз PD‑1 может быть задействован — и, следовательно, заблокирован препаратами. Маркеры, связанные с LAG‑3 и TIM‑3, также присутствовали, но опухолевая линия экспрессировала лишь часть их партнерских молекул, что может объяснять ограниченное влияние таргетирования этих контрольных точек. Также наблюдалась тенденция к увеличению «сигналов газу» (ко‑стимулирующие молекулы, такие как CD137 и GITR) на Т‑клетках после пептидной стимуляции и блокады PD‑1, что предполагает: как только основной тормоз снят, «ускоритель» может действовать активнее.
Что это может значить для будущих пациентов
Поскольку эти эксперименты проводились вне организма, они не в состоянии полностью имитировать сложную опухолевую среду или зачастую ослабленную иммунную систему пациентов, прошедших химио‑ и лучевую терапию. Тем не менее полученные результаты дают ясный и практический вывод: если сначала обучить Т‑клетки распознавать специфические раковые маркеры (с помощью пептидной вакцины), а затем снять с них тормоз PD‑1, они становятся значительно лучше в атаке клеток опухоли головы и шеи. Добавление других ингибиторов контрольных точек сверх PD‑1 в этой модели не давало преимущества. Авторы делают вывод, что сфокусированная стратегия — вакцинация пациентов пептидами, ассоциированными с опухолью, такими как MAGE, NY‑ESO‑1 или PRAME, в сочетании с блокадой PD‑1 — заслуживает клинической проверки как способ превратить иммунитет большинства пациентов в эффективного борца с раком.
Цитирование: Schuler, P.J., Oliveri, F., Puntigam, L. et al. Immune checkpoint inhibition increases antigen-specific T cell response in head and neck cancer. Sci Rep 16, 5583 (2026). https://doi.org/10.1038/s41598-026-38740-z
Ключевые слова: рак головы и шеи, терапия ингибиторами контрольных точек, блокада PD-1, раковые вакцины, опухолевые антигены