Clear Sky Science · ru
Химический синтез новых производных аминопиримидин-4-ил-1H-пиразола в качестве ингибиторов тирозинкиназы селезёнки (SYK)
Почему блокировка одного фермента может помочь в борьбе с раком и воспалением
Наша иммунная система полагается на быстрые внутриклеточные сигналы, которые подсказывают клеткам, когда атаковать врагов, а когда отступить. Когда эти сигналы дают сбой, это может привести к аутоиммунным заболеваниям и способствовать развитию рака. В этом исследовании изучается перспективный способ приглушить такие неправильные сигналы посредством проектирования небольших лекареподобных молекул, селективно блокирующих ключевой фермент — тирозинкиназу селезёнки (SYK), находящуюся в центре многих иммунных реакций.
Переключатель сигналов в основе многих заболеваний
SYK действует как главный переключатель в некоторых иммунных клетках. При активации он стимулирует воспаление, выработку антител и рост клеток. В норме это помогает бороться с инфекциями. Но при таких состояниях, как ревматоидный артрит, астма и при ряде кровяных и солидных опухолей активность SYK может быть чрезмерной, удерживая иммунные клетки в активном состоянии и поддерживая выживание опухолей. Из-за этой центральной роли учёные по всему миру пытаются создать препараты-блокаторы SYK, достаточно мощные для лечебного эффекта, но достаточно точные, чтобы не поражать множество других ферментов и не вызывать побочных эффектов.
Создание семейства адаптированных малых молекул
Авторы разработали новую серию родственных соединений на основе общего химического остова — аминопиримидин-4-ил-1H-пиразола. Начиная с простых строительных блоков, они шаг за шагом собирали эти структуры и затем модифицировали одну часть молекулы, получив девять окончательных кандидатов. Каждое соединение было тщательно охарактеризовано стандартными аналитическими методами, чтобы подтвердить его строение и чистоту. Такой модульный подход позволил команде исследовать, как тонкие изменения формы и гибкости влияют на взаимодействие этих соединений с SYK.
Наблюдение за тем, как соединения захватывают мишень
Перед переходом к лабораторным экспериментам исследователи использовали компьютерное моделирование, чтобы оценить, насколько прочно каждое соединение может прикрепляться к SYK. Расчёты докинга показали, как хорошо соединения вписываются в карман связывания фермента, выделив один кандидат, обозначенный как 44, как особенно перспективный. Более детальные молекулярно-динамические симуляции, в которых комплекс белок–лекарство отслеживался в течение сотен наносекунд, показали, что 44 образует особенно стабильное взаимодействие с SYK. Белок оставался компактным, ключевые контакты сохранялись, и система устремлялась к единой низкоэнергетической конформации с множеством сильных водородных связей, особенно с участием аминокислот вроде триптофана и серина, которые помогают «поддержать» молекулу.
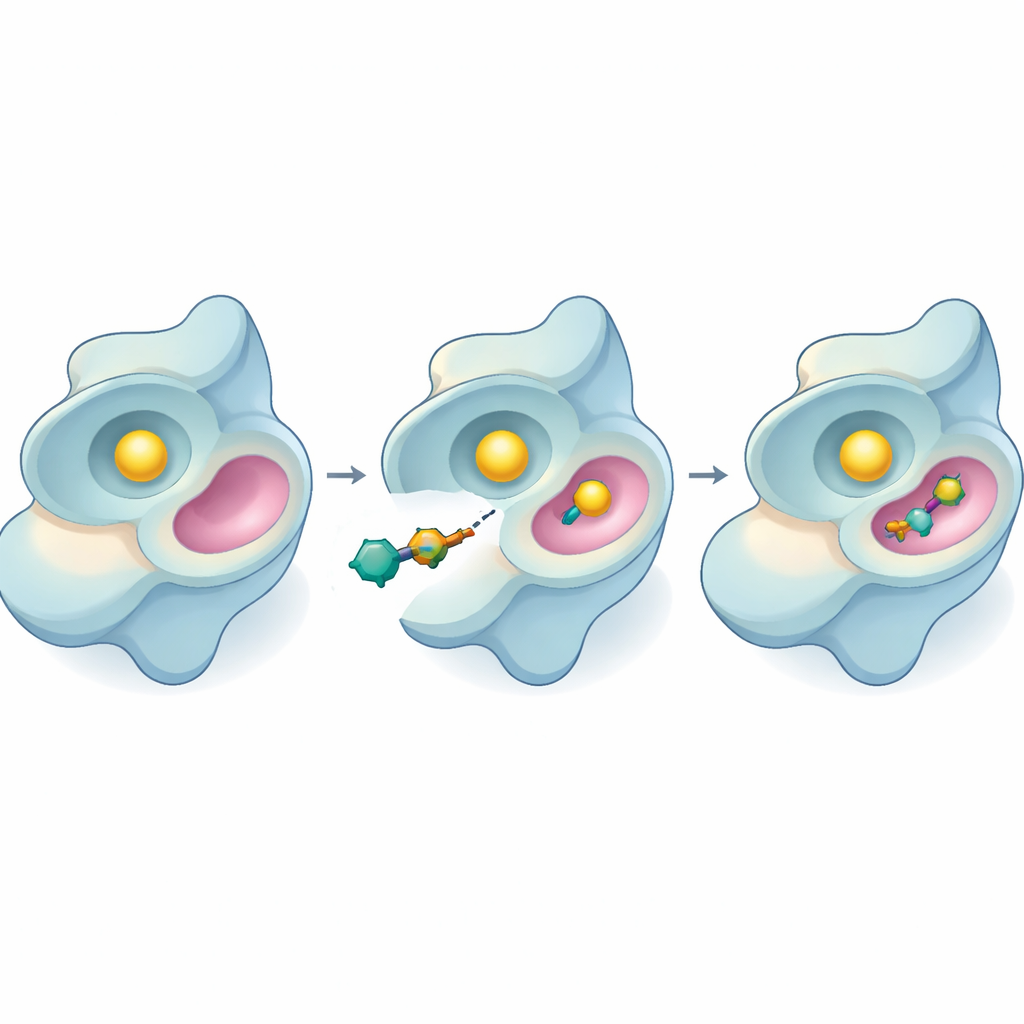
Проверка новых ингибиторов в деле
Затем команда перешла к лабораторным экспериментам, используя люминесцентный тест, измеряющий, насколько активно SYK потребляет свой «топливный» молекулу ATP. Несколько новых соединений замедляли фермент, но снова выделился 44. Он ингибировал SYK при очень низких концентрациях и становился более эффективным с увеличением времени контакта с ферментом. Варьируя концентрацию субстрата, исследователи смогли вывести механизм действия 44: вместо прямого конкурирования с ATP в основном активном сайте он, по-видимому, связывается в другом, аллостерическом участке и меняет поведение фермента на расстоянии. Это важно, потому что аллостерические ингибиторы часто сохраняют эффект даже при высоких уровнях ATP или при мутациях, изменяющих основной сайт.
Что это может значить для будущих терапий
В совокупности компьютерные модели и лабораторные измерения рисуют последовательную картину: молекула 44 сильно связывается с SYK, удерживает фермент в стабильном, менее гибком состоянии и подавляет его активность через косвенный, неконкурентный механизм. Для неспециалистов это означает, что исследователи нашли тонко настроенный химический «ключ», который подходит к «замку», важному для многих иммунно-опосредованных заболеваний, не просто блокируя главный вход. Хотя предстоит ещё много работы — особенно испытания в клетках, на животных и в более широких панелях родственных ферментов — этот остов представляет собой перспективную отправную точку для будущих препаратов, нацеленных на укрощение вредного воспаления и замедление некоторых видов рака путём ингибирования SYK.
Цитирование: Rajasheker, K.V., Pallavi, M.S., Singh, P. et al. Chemical synthesis of novel aminopyrimidin-4-yl-1H-pyrazole derivatives as spleen tyrosine kinase (SYK) inhibitors. Sci Rep 16, 8323 (2026). https://doi.org/10.1038/s41598-026-38719-w
Ключевые слова: тирозинкиназа селезёнки, ингибиторы киназ, противораковые препараты, аутоиммунные заболевания, аллостерические препараты