Clear Sky Science · ru
Валидация фенотипов химиорезистентности при плевральном мезотелиоме в 2D, 3D и in vivo моделях
Почему некоторые раки не поддаются химиотерапии
Для пациентов с диагнозом плеврального мезотелиомы — рака, связанного с воздействием асбеста — химиотерапия часто является главным вариантом лечения. Однако многие опухоли либо почти не реагируют, либо сначала сокращаются, а затем быстро возвращаются. В этом исследовании задают на первый взгляд простой, но крайне важный вопрос: насколько реалистичны лабораторные модели, которые используют исследователи для тестирования препаратов, и способны ли они предсказать то, что действительно происходит в организме пациента?
От плоских слоёв клеток до крошечных опухолевых шариков
Большинство противораковых препаратов сначала испытывают на клетках, выращенных в виде плоских слоёв на пластиковых планшетах. Эти двумерные (2D) культуры удобны, но они не похожи на настоящие опухоли — трёхмерные (3D) скопления плотных клеток, окружённые сложным «соседством» из кровеносных сосудов, структурных белков и иммунных клеток. Исследователи создали 3D-модель — сфероиды мезотелиомы, где раковые клетки образуют компактные мини-опухоли. Они сравнили, как клетки мезотелиомы всех основных подтипов — эпителиоидного, бипhasic и высокоагрессивного саркоматоидного — отвечали на стандартную химиотерапию в виде плоских 2D‑слоёв и в виде 3D-сфероидов.
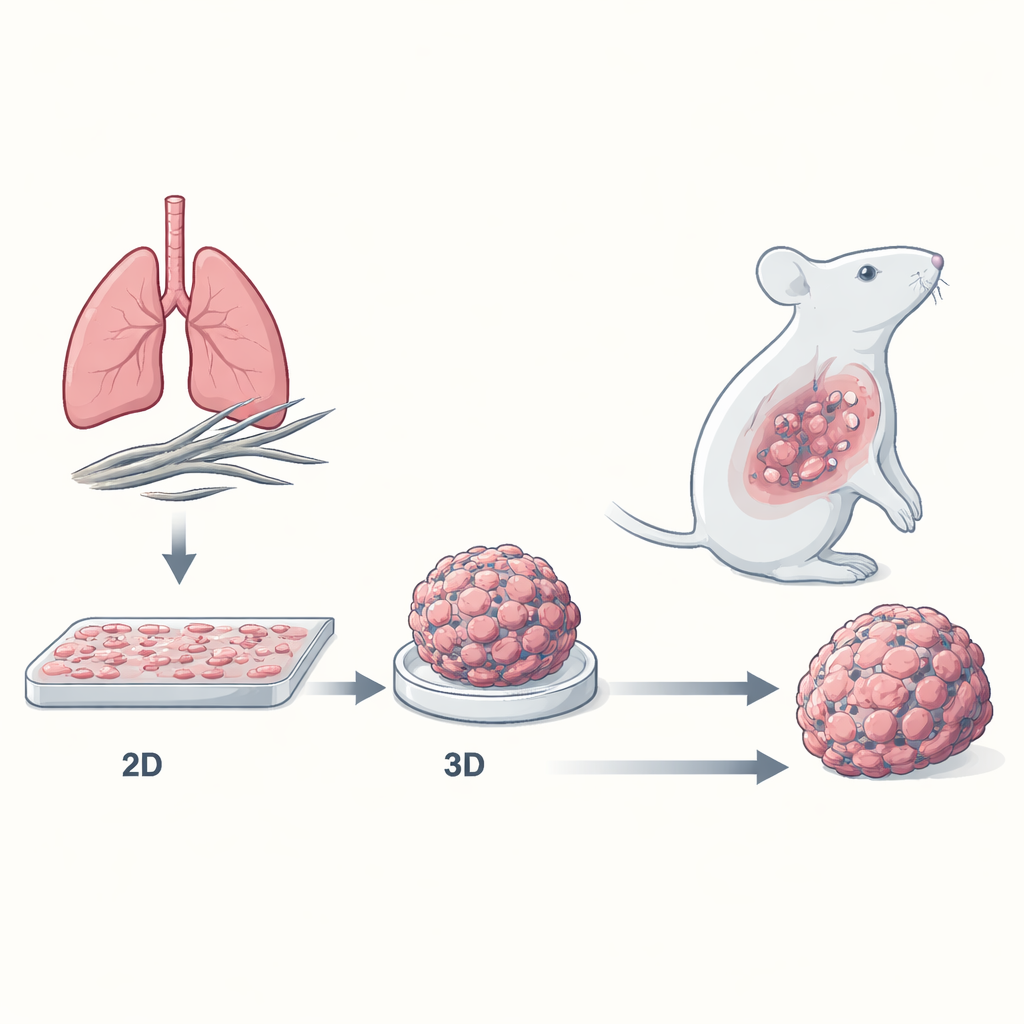
3D мини-опухоли гораздо труднее уничтожить
При воздействии широко используемой комбинации цисплатин–пеметрексед клетки мезотелиомы, выращенные в 2D, легко повреждались: их рост замедлялся, многие оказывались в остановленной «S‑фазе» клеточного цикла, и большое число клеток переживало программируемую гибель (апоптоз). Напротив, 3D‑сфероиды почти не уменьшались в размерах и требовали гораздо больших доз препарата для достижения подобных эффектов. Саркоматоидный подтип, известный у пациентов как наиболее трудно поддающийся лечению, также оказался наименее чувствителен к лекарствам в 3D‑модели — что соответствует клинической картине. Детальные измерения показали, что после лечения 2D‑клетки теряли жизнеспособность и шли к гибели, тогда как клетки в сфероидах в основном оставались живыми, с лишь умеренным увеличением ранних маркеров апоптоза.
Более тихий метаболизм и сигналы, способствующие выживанию
Команда изучила различия в использовании энергии между моделями с помощью метаболического «стресс‑теста». Химиотерапия переводила 2D‑клетки из активного, энергозатратного состояния в более тихий режим с резким падением митохондриального потребления кислорода — признак того, что лечение нарушает их внутренние «электростанции». Напротив, 3D‑сфероиды уже находились в состоянии с низким уровнем энергии и недостатком кислорода, которое почти не менялось при лечении — аналогично стрессовым, гипоксическим условиям, наблюдаемым внутри настоящих опухолей. Исследователи также измерили малые регуляторные молекулы — микроРНК — и обнаружили подтип‑специфические паттерны, связанные с лекарственной устойчивостью. В частности, неэпителиоидные сфероиды усиливали экспрессию микроРНК, ранее связанной с плохим прогнозом и снижением гибели клеток в других типах рака. В опухолях, выращенных у мышей из 3D‑сфероидов, белки, вовлечённые в мощные пути выживания — PI3K/AKT и VEGF/Notch — были повышены, дополнительно защищая раковые клетки от гибели.
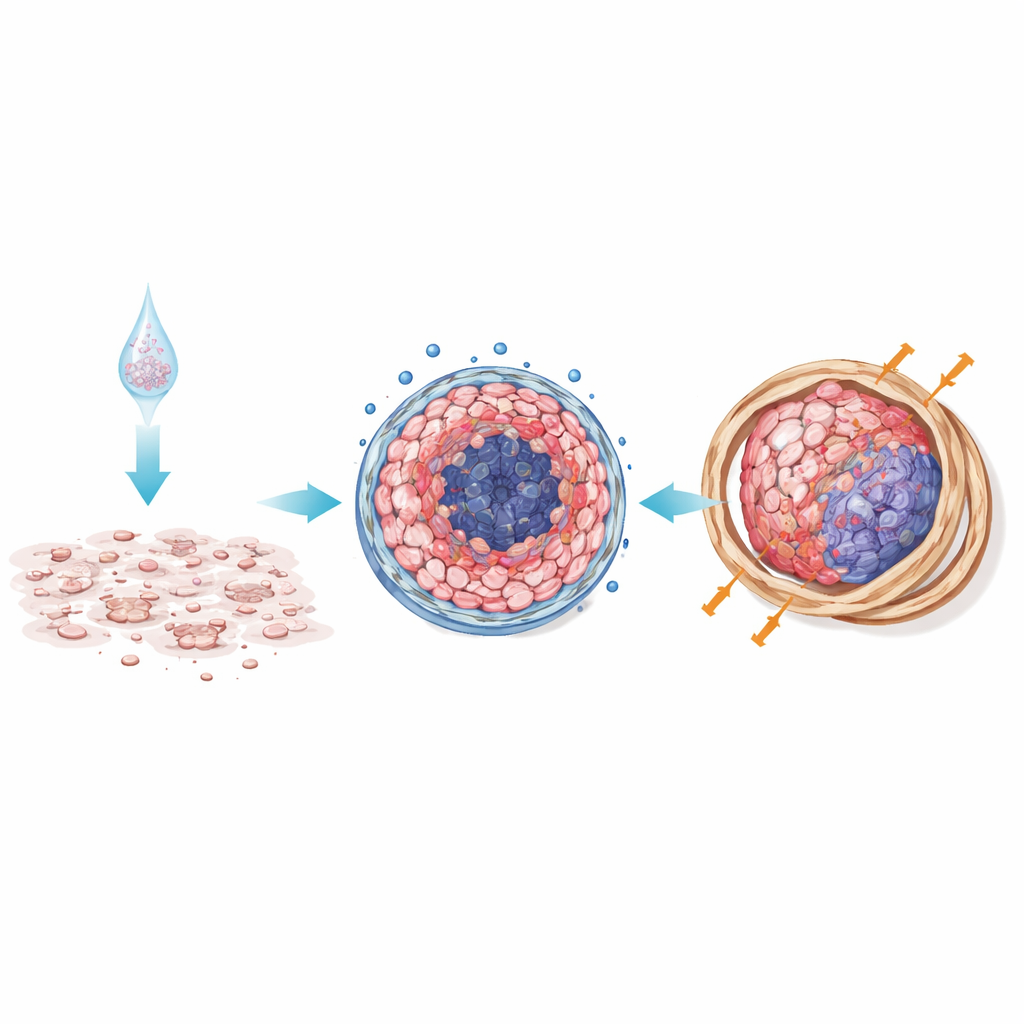
Опухоли у мышей подтверждают предсказания чашки Петри
Чтобы проверить, имеют ли эти различия значение в живом организме, учёные имплантировали клетки мезотелиомы мышам либо поодиночке (имитируя 2D‑культуру), либо в виде заранее сформированных 3D‑сфероидов. Опухоли, начавшиеся как сфероиды, росли больше и меньше реагировали на химиотерапию, чем те, что образовались из отдельных клеток. Под микроскопом опухоли, происходившие из 3D, демонстрировали плотные слои коллагена и волокнистой ткани, более организованные клеточные гнёзда и меньше мёртвых участков. Эта фиброзная «оболочка» скорее всего действует как физический и биохимический барьер, ограничивая проникновение препаратов и усиливая сигналы выживания — условия, которые очень близки тому, что наблюдается в стойких человеческих опухолях.
Что это значит для будущего лечения
Для непрофессионала главный вывод таков: способ выращивания раковых клеток в лаборатории может определить, насколько реалистичны тесты препаратов. Крошечные 3D‑опухолевые сфероиды воспроизводят ключевые черты мезотелиомы, которые упускают плоские слои клеток: кислородно‑бедные ядра, напряжённые, но трудно уничтожаемые клетки, защитная рубцовая ткань и активация путей выживания, блокирующих гибель клеток. Поскольку эти 3D‑модели ведут себя гораздо более похоже на настоящие опухоли у пациентов и у мышей, они предлагают более надёжную платформу для поиска препаратов и тестирования комбинаций, нацеленных как на раковые клетки, так и на их защитное окружение. В долгосрочной перспективе использование таких реалистичных моделей может помочь исследователям выявлять методы лечения, которые с большей вероятностью сработают в клинике, а не только в лаборатории.
Цитирование: Shi, H., Selvamani, S.P., Zelei, R. et al. Validation of chemoresistance phenotypes in pleural mesothelioma across 2D, 3D, and in vivo models. Sci Rep 16, 8396 (2026). https://doi.org/10.1038/s41598-026-38692-4
Ключевые слова: плевральный мезотелиома, устойчивость к химиотерапии, 3D опухолевые сфероиды, опухолевый микроокружение, модели тестирования противораковых препаратов