Clear Sky Science · ru
Фотоиндуцированный перенос протонов в воде с различной структурой: подход ЭПР к решению классической задачи
Почему скрытые перемещения протонов важны
Каждый раз, когда вы дышите, думаете или преобразуете солнечный свет в полезную энергию в солнечной ячейке, крошечные положительно заряженные частицы — протоны — находятся в движении. То, как эти протоны перемещаются через воду, — задача возрастом в несколько столетий, впервые сформулированная Теодором Гроттхуссом в 1806 году. В новом исследовании используется изящное сочетание света и магнитных измерений, чтобы наблюдать движение протонов в воде с разной структурой: от солёных и густонаселённых растворов до стекловидных замороженных смесей и даже внутри мембранного белка. Работа предлагает свежий способ проверить классические идеи о движении протонов и исследовать среды, которые трудно изучать другими методами.
Новый способ наблюдать за перемещением протонов
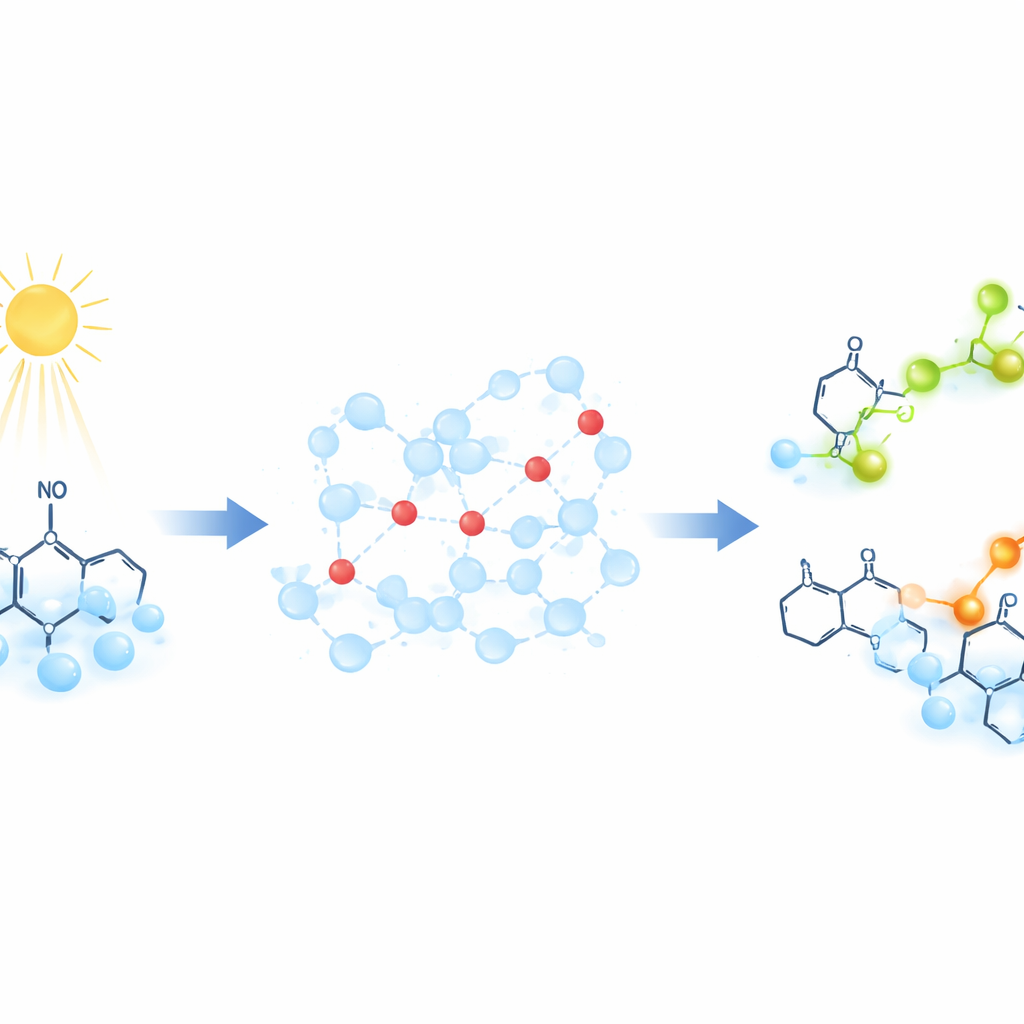
Вместо того чтобы следить за протонами напрямую, исследователи используют специальные «пробные» молекулы, которые изменяют свою магнитную подпись при захвате протона. Эти зонды — стабильные органические радикалы с неспаренным электроном, дающим чёткий сигнал в электронном парамагнитном резонансе (ЭПР), методе, фиксирующем ответ неспаренных электронов на магнитное поле. Чтобы запустить движение протонов по требованию, команда освещает соединение 2‑нитробензальдегидом. Эта фотохимическая реакция высвобождает вспышку протонов менее чем за миллиардную долю секунды, резко понижая pH раствора. По мере того как протоны распространяются по воде и присоединяются к зондами, ЭПР‑сигнал сдвигается во времени, что позволяет учёным отслеживать скорость переноса протонов.
Как окружение воды замедляет или ускоряет поток
Вода редко существует в одиночку; обычно она окружена растворёнными солями или другими молекулами, которые тонко перестраивают сеть водородных связей. Команда проверила, как такие добавки влияют на движение протонов, сравнив чистую воду с растворами, содержащими хлорид калия, мочевину или гуанидиний хлористый, все в высоких концентрациях. Подбирая изменения ЭПР к простым кинетическим моделям, они извлекли видимые скорости переноса протонов. Оказалось, что в 6‑молярном растворе гуанидиний хлористого перенос протонов был примерно в 40 раз медленнее, чем в чистой воде, тогда как 8‑молярная мочевина вызывала лишь умеренное замедление, а хлорид калия давал промежуточный эффект. Поскольку скорость, с которой протоны реагируют с зондами, ограничена их перемещением по сети водородных связей, эти различия указывают на существенные изменения в организации воды вокруг добавленных ионов и молекул.
Движение протонов в стекловидном льду и внутри белков
Метод не ограничивается обычной жидкой водой. Авторы также изучили смесь воды и глицерина, охлаждённую до 160 кельвинов, где она образует жёсткое стекло. Свободная диффузия молекул там фактически заморожена, но ЭПР‑сигнал всё равно показал, что зонды протонируются после облучения. Это указывает на то, что перенос протонов может происходить без классической диффузии, возможно посредством квантового туннелирования вдоль цепочки водородных связей, что перекликается с современными уточнениями идеи Гроттхусса. Чтобы исследовать биологическую релевантность, команда прикрепила pH‑чувствительный радикал к конкретному участку мембранного белка бактериородопсина, на границе между белком и окружающей водой. При запуске высвобождения протона светом они наблюдали временно‑зависимый ЭПР‑ответ с этого меченого участка, демонстрируя, что их подход может мониторить доставку протонов на определённую позицию на поверхности белка.
Связь структуры, воды и «протонных шоссе»
Чтобы лучше понять, почему зонд, связанный с белком, вёл себя почти так же, как в объёмной воде, исследователи провели компьютерное моделирование бактериородопсина в мембране и небольшого пептида в растворе. Они рассчитали, как молекулы воды окружают нитроксильную группу спин‑метки, и обнаружили почти идентичные локальные картины гидратации в обоих случаях, с лишь лёгким экранирующим эффектом со стороны мембранной среды. Это значит, что, по крайней мере для изученной позиции, протоны получают доступ через водный слой, очень похожий на обычную жидкую воду. Авторы также показывают, что их зонды можно применять в временно‑разрешённых экспериментах ЭПР, что открывает возможность одновременно отслеживать движение протонов и электронов в реакциях, где эти процессы тесно связаны.
Что это исследование говорит простыми словами
По сути, в этом исследовании свет служит чётким стартовым выстрелом для движения протонов, а затем чувствительные магнитные зонды позволяют наблюдать, как быстро эти протоны достигают разных целей. Сравнивая простые солевые растворы, плотные денатураты, стекловидные смеси и мембранный белок, исследователи демонстрируют, что поток протонов сильно определяется тем, как расположены молекулы воды и какое окружение их окружает. Их подход не только поддерживает идею о том, что протоны «перепрыгивают» по сетям водородных связей, но и показывает, что такое рывковое движение может сохраняться даже тогда, когда обычное молекулярное движение почти заморожено. Новый набор методов может помочь учёным разбирать механизмы переноса протонов в ферментах, системах преобразования энергии и новых материалах, приближая нас к управлению этими крошечными, но мощными носителями заряда.
Цитирование: Barbon, A., Savitsky, A., Grigoriev, I. et al. Photoinduced proton transfer in differently structured water: an EPR approach to solving a classic problem. Sci Rep 16, 7983 (2026). https://doi.org/10.1038/s41598-026-38650-0
Ключевые слова: перенос протонов, структура воды, электронный парамагнитный резонанс, сеть водородных связей, бактериородопсин