Clear Sky Science · ru
Длинная некодирующая РНК FTX усиливает миокардиальный фиброз, действуя как «губка» для miR-335-3p и регулируя сигналы TFEC/ILK
Почему важно рубцевание сердца
Сердечная недостаточность поражает десятки миллионов людей во всем мире и часто развивается незаметно годами. Главным фактором этого ухудшения является миокардиальный фиброз — медленное, прогрессирующее образование рубцовой ткани в сердце, которое делает его более жестким и менее способным перекачивать кровь. В этом исследовании вскрывают молекулярную «проводку», которая приказывает клеткам сердца откладывать слишком много рубцовой ткани, и выявляют новую цепочку молекул, нацеливание на которые может замедлить или даже обратить этот вредный процесс.
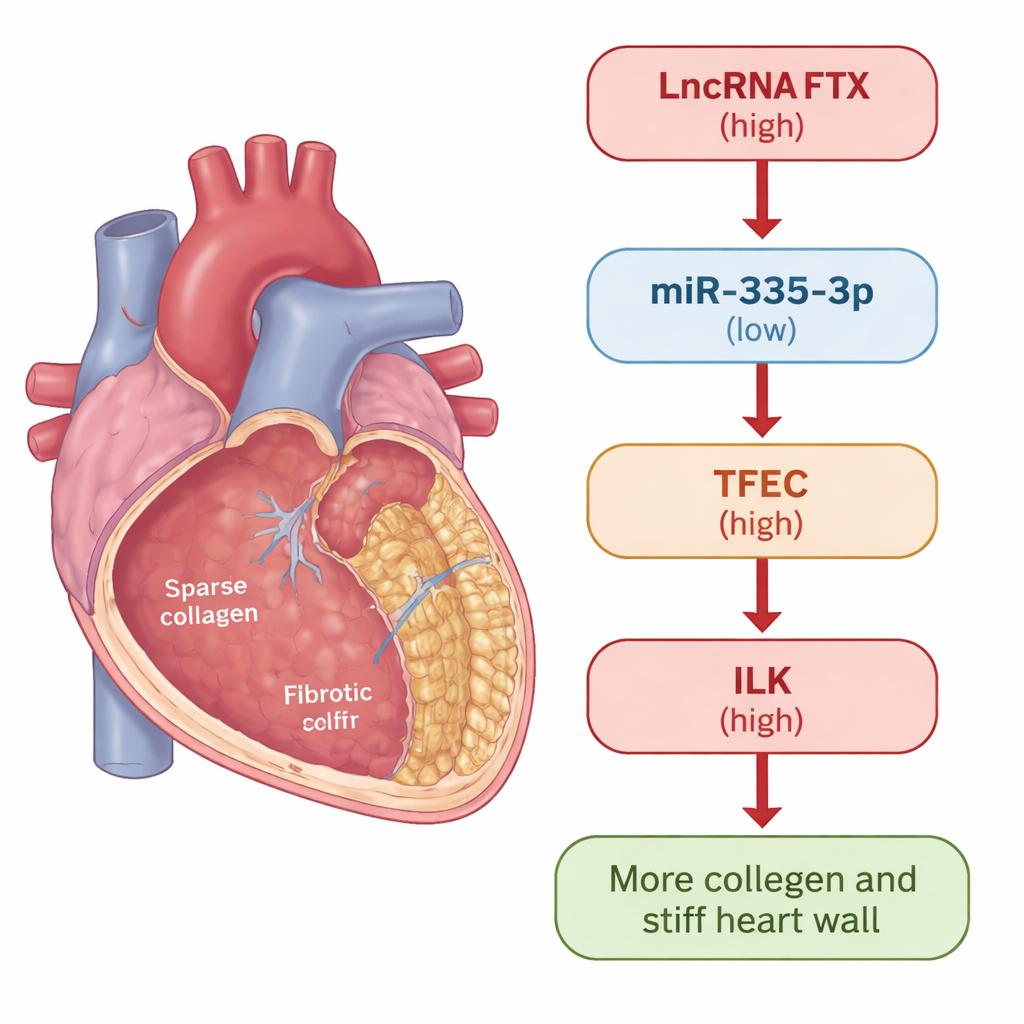
Более пристальный взгляд на рубцевание сердца
Когда сердце повреждено или испытывает стресс, в ответ включаются вспомогательные клетки — кардиальные фибробласты. При нормальном восстановлении они помогают заделывать повреждения. Но при хроническом заболевании они могут переключиться в гиперактивное состояние, вырабатывать избыток коллагена и других компонентов внеклеточного матрикса, в конечном итоге уплотняя стенку сердца. Исследователи использовали две модели для изучения этого процесса: мышей, обработанных изопротеренолом, который надежно индуцирует фиброз сердца, и человеческие кардиальные фибробласты, подвергнутые действию сигнальной молекулы TGF-β1, хорошо известного триггера рубцевания. В обоих моделях они измеряли, как меняется активность конкретных генов и белков по мере развития фиброза.
Вредная цепная реакция внутри клеток
Команда сосредоточилась на транскрипционном факторе TFEC — белке, находящемся в ядре клетки и включающем другие гены. Они обнаружили, что TFEC вместе с другим белком, интегрин-связанной киназой (ILK), постоянно увеличиваются, когда фибробласты переходят в фибротическое, рубцеобразующее состояние. Подавление TFEC или ILK резко снижало классические маркеры фиброза, такие как α-гладкомышечный актин и коллагены I и III, а также ослабляло путь контроля роста (Akt/GSK3β и сигналы Hippo), известный своей ролью в продвижении формирования рубцовой ткани. Эксперименты по картированию связывания с ДНК показали, что TFEC непосредственно прикрепляется к промотору гена ILK и усиливает его активность, что однозначно ставит TFEC выше ILK в про-фибротическом сигнальном каскаде.
РНК-переключатели, контролирующие главный регулятор
Чтобы понять, что регулирует сам TFEC, исследователи обратились к некодирующим РНК — молекулам РНК, которые не кодируют белки, но тонко регулируют активность генов. Они идентифицировали небольшую РНК, miR‑335‑3p, уровень которой снижался при фиброзе в сердце и клетках. Повышение уровня miR‑335‑3p понижало TFEC, тогда как блокирование miR‑335‑3p увеличивало TFEC; репортерные тесты подтвердили, что miR‑335‑3p напрямую связывается с сообщениями TFEC и сдерживает их. Затем они нашли длинную некодирующую РНК FTX, уровень которой повышался при фиброзе и которая физически взаимодействовала с miR‑335‑3p. FTX действовала как молекулярная губка: она «поглощала» miR‑335‑3p, не давая этой мелкой РНК сдерживать TFEC. В результате TFEC и ILK повышались, а фибробласты вырабатывали больше коллагена, образующего рубцы.
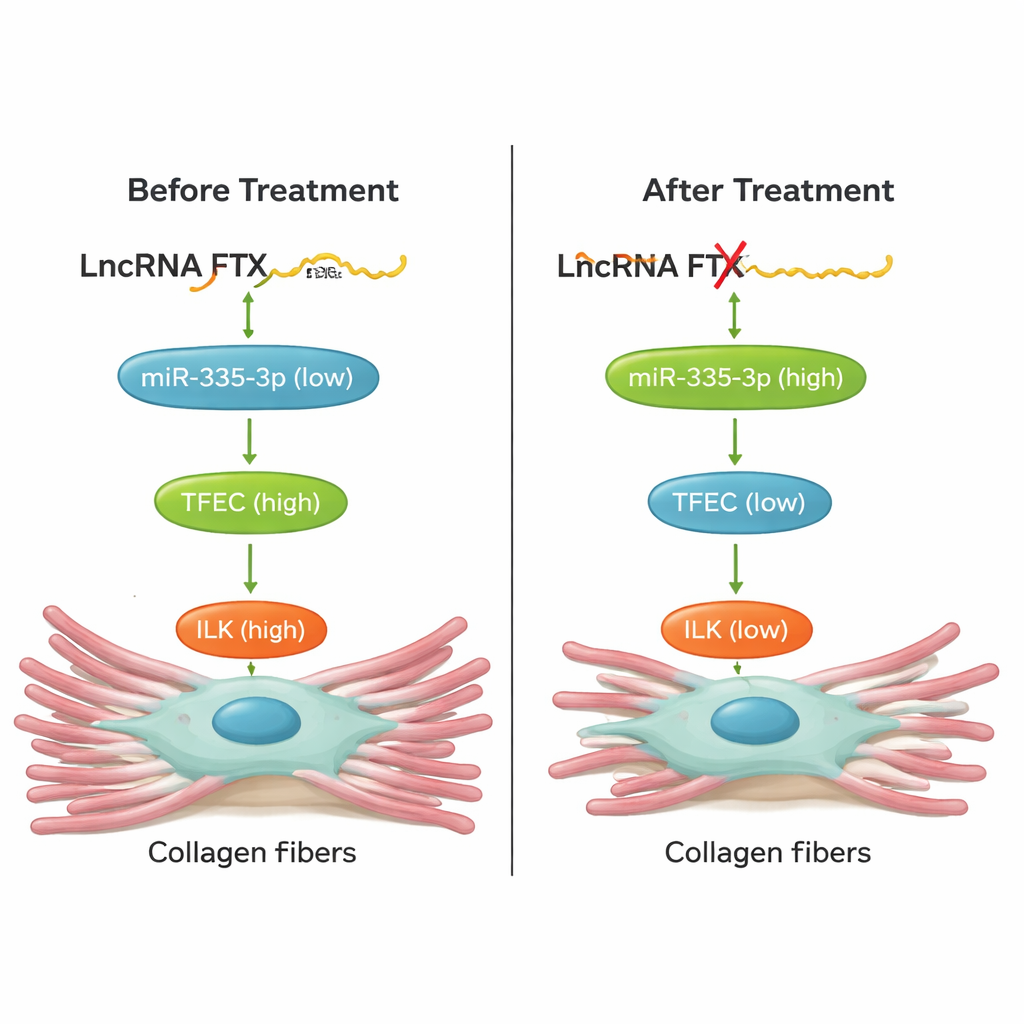
От клеточных культур к живым сердцам
Критически важно, что команда проверила, может ли разрыв этой цепочки реально защитить сердце у животных. У мышей, подвергнутых действию изопротеренола, подавление TFEC, снижение уровня FTX в сердце с помощью AAV9 векторной генетической терапии или повышение miR‑335‑3p с использованием химически стабилизированного «аго-мир» приводили к уменьшению накопления коллагена и снижению уровней маркеров фиброза в сердечной ткани. Эти вмешательства также улучшали функцию сердца: ударный объём и фракция выброса возвращались ближе к норме, а вредные повышения частоты сердечных сокращений ослаблялись. Эксперименты по спасению в клетках показали, что изменение одного компонента оси FTX/miR‑335‑3p/TFEC/ILK предсказуемо сдвигает другие, подтверждая, что это плотно связанный путь, а не случайная корреляция.
Что это значит для будущих терапий
Для неспециалиста главное: авторы выявили новый «рычаг управления» рубцеванием сердца. Длинная РНК FTX снимает тормоз (miR‑335‑3p) с главного переключателя (TFEC), который затем активирует ILK и нисходящие про-рубцовые сигналы, стимулируя чрезмерное отложение коллагена и уплотнение сердца. Сократив уровень FTX, восстановив miR‑335‑3p или прямо блокируя TFEC, в исследованиях на мышах удалось уменьшить образование рубцов и улучшить насосную функцию. Хотя требуется дополнительная работа, чтобы подтвердить этот путь у пациентов и разработать безопасные терапии, эта РНК-основанная регуляторная цепочка предоставляет несколько перспективных точек вмешательства при фиброз-опосредованной сердечной недостаточности.
Цитирование: Yao, F., He, Z., Zheng, C. et al. LncRNA FTX promotes myocardial fibrosis by sponging miR-335-3p to regulate TFEC/ILK signaling. Sci Rep 16, 7340 (2026). https://doi.org/10.1038/s41598-026-38615-3
Ключевые слова: миокардиальный фиброз, сердечная недостаточность, некодирующая РНК, кардиальные фибробласты, сигнализация фиброза