Clear Sky Science · ru
Пролиферация и антиапоптотические эффекты, обусловленные DNMT3A p.R882C, в клетках рака поджелудочной железы
Почему это исследование важно для рака поджелудочной железы
Рак поджелудочной железы печально известен поздним выявлением, быстрым распространением и слабой ответной реакцией на лечение. У большинства пациентов диагностируют аденокарциному протоков поджелудочной железы (PDAC) — особенно агрессивную форму заболевания. В этом исследовании рассматривается крошечное изменение в одном гене — DNMT3A — и ставится важный вопрос: может ли это небольшое изменение помочь объяснить, почему некоторые опухоли поджелудочной растут быстрее и сопротивляются гибели клеток? Понимание подобных изменений может открыть путь к более раннему выявлению и точным таргетным вмешательствам.
Более пристальный взгляд на смертоносный рак
PDAC составляет более 90% случаев рака поджелудочной железы и имеет пятилетнюю выживаемость ниже 13%. Как правило, его развитие обусловлено известными онкогенами, такими как KRAS и TP53, но многие пациенты по-прежнему не получают пользы от существующих таргетных методов лечения. Недавние работы указывают, что важную роль в этом раке играют не только мутации генов, но и «эпигенетические» изменения — химические метки на ДНК, которые регулируют включение и выключение генов. DNMT3A — один из ключевых ферментов, наносящих эти метки, и его дефекты уже связаны с опухолями крови, например с острым миелоидным лейкозом.
В поисках опасных изменений в ДНК
Исследователи собрали образцы опухоли и соседней некоперной ткани у трёх пациентов с умеренно- и плохо дифференцированным PDAC. Они провели секвенирование всех экзонов (whole‑exome sequencing) — метод, читающий все кодирующие белки участки генома — и затем применили строгие компьютерные фильтры, чтобы отделить безвредные варианты ДНК от тех, которые с высокой вероятностью нарушают поведение клеток. Из сотен изменений исследователи сузили список до 68 высокорисковых вариантов. Среди них выделялся редкий вариант в DNMT3A, известный как p.R882C, поскольку он почти не встречается в крупных популяционных базах и последовательно определяется как вредоносный несколькими предикторными инструментами.
Что делает эта мутация внутри клеток
DNMT3A — белок из 912 аминокислот, который помогает устанавливать шаблоны метилирования ДНК — химические метки, действующие как «включатели» или «выключатели» для генов. Замена p.R882C локализуется в важном функциональном участке DNMT3A, где она может нарушать активность фермента. С помощью 3D‑компьютерного моделирования команда обнаружила, что общая форма белка резко не изменилась, что указывает на то, что проблема может заключаться не в сворачивании, а в самой функции фермента. Чтобы проверить это, они создали линии клеток рака поджелудочной (PANC‑1 и PaTu 8988t), экспрессирующие либо нормальный DNMT3A, либо вариант p.R882C, и сравнили их с клетками, несущими пустой контрольный вектор.
Более быстрый рост, повышенная подвижность, сниженная гибель клеток
Удивительно, но мутация p.R882C не меняла уровни экспрессии DNMT3A на уровне РНК или белка; количество фермента оставалось примерно одинаковым. Тем не менее наличие этой мутации оказало заметное влияние на поведение клеток. В колониеобразующих и пролиферативных тестах клетки с мутантным DNMT3A образовывали больше колоний и демонстрировали повышенные показатели роста по сравнению с клетками с нормальной версией. Тесты заживления ран (wound‑healing) и Trans‑well, измеряющие скорость миграции клеток, показали, что клетки с мутацией перемещаются быстрее. При оценке программируемой гибели клеток (апоптоза) методом проточной цитометрии клетки с p.R882C имели значительно меньше умирающих клеток как на ранних, так и на поздних стадиях апоптоза, что указывает на выраженное преимущество в выживании.
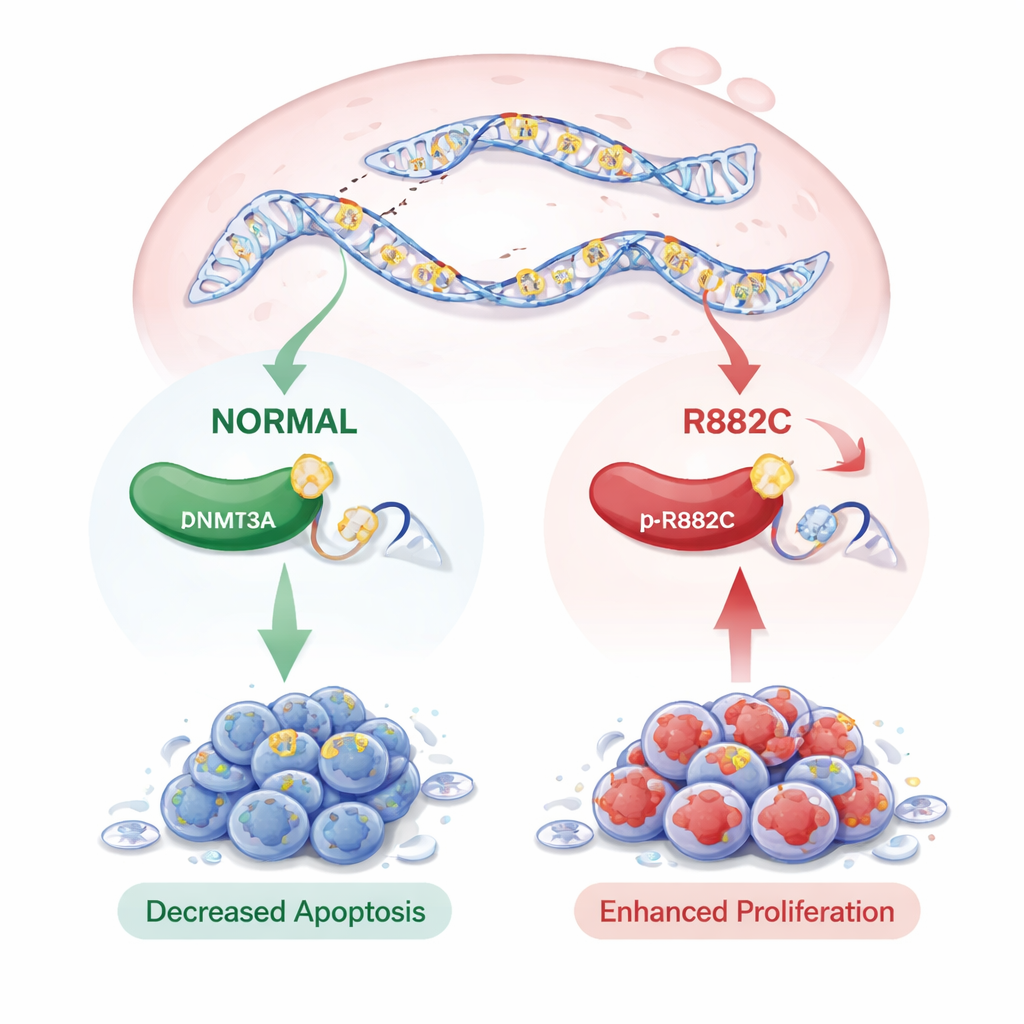
Что это может значить для будущего лечения
Вместе эти результаты дают основание полагать, что редкая мутация DNMT3A p.R882C способствует быстрому росту клеток рака поджелудочной, повышает их подвижность и делает их более устойчивыми к самоуничтожению — черты, которые могут способствовать прогрессированию опухоли. Хотя мутация не повышает уровни DNMT3A, она, вероятно, изменяет активность фермента и шаблоны метилирования ДНК по всему геному, повторяя наблюдения, сделанные в некоторых опухолях крови. Авторы отмечают, что это изменение встречается редко и пока не показало явной связи с выживаемостью пациентов в публичных наборах данных, отчасти потому, что доступные исследования малы и часто не включают DNMT3A. Тем не менее обнаружение этой мутации в PDAC подчёркивает потенциально важную новую мишень в болезни и создаёт предпосылки для того, что в будущем DNMT3A p.R882C может служить маркером риска или целью для более персонализированных терапий.
Цитирование: Qu, Z., Mao, J., Qian, Y. et al. DNMT3A p.R882C driven proliferation and anti-apoptotic effects in pancreatic cancer cells. Sci Rep 16, 7659 (2026). https://doi.org/10.1038/s41598-026-38613-5
Ключевые слова: рак поджелудочной железы, мутация DNMT3A, PDAC, метилирование ДНК, таргетная терапия