Clear Sky Science · ru
Редактирование генома в разных видах Dictyostelia открывает сравнительную функциональную генетику социальных амеб
Как одиночные клетки объединяются
Большую часть времени амебы — крошечные одиночки, ползающие в почве и поедающие бактерии. Однако некоторые из них, называемые социальными амебами, могут внезапно собираться в многоклеточное тело с примитивной «головкой» и «стеблем». Такой меняющийся образ жизни даёт учёным редкую возможность заглянуть в то, как простые клетки учатся сотрудничать и специализироваться — ключевые этапы на пути к возникновению сложной жизни. Новое исследование описывает набор инструментов для редактирования генома, который наконец позволяет изучать эти поведения не только на одной лабораторной модели, но и в нескольких отдалённых видах амеб.
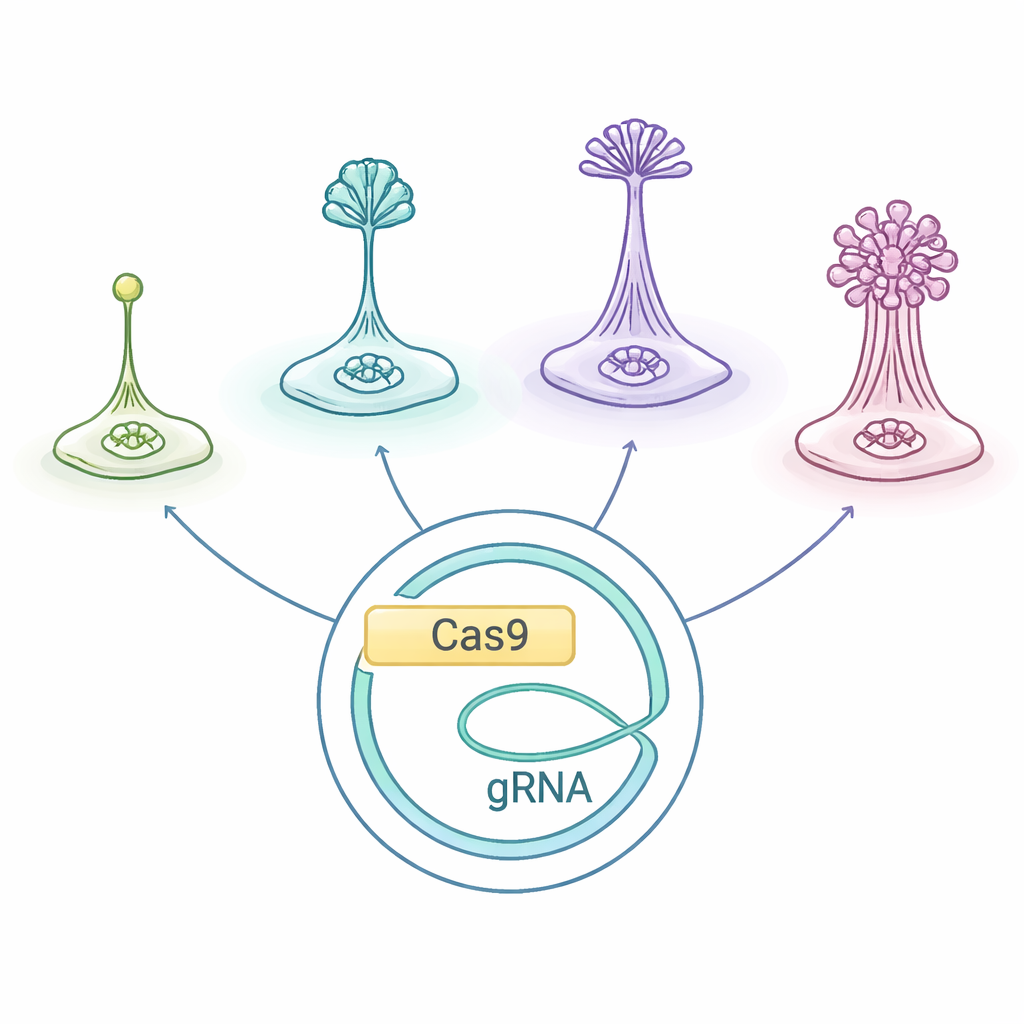
Малые существа с богатыми общественными связями
Социальные амебы, объединённые в группу Dictyostelia, живут поодиночке, пока пища в избытке. Когда они голодают, начинают посылать химические сигналы бедствия и собираться друг к другу, образуя насыпь, которая затем формирует миниатюрное «плодовое тело»: колонну жертвующихся клеток стебля, возносящих выносливые споры в воздух. Разные линии Dictyostelia строят эти структуры по-разному и используют разные типы клеток, что делает их естественной лабораторией для изучения того, как возникают многоклеточные тела и разделение труда.
Одного модельного вида было недостаточно
До сих пор почти все молекулярные исследования сосредотачивались на одном виде, Dictyostelium discoideum, потому что его гены относительно просто модифицировать. Это оставляло более ста других известных видов — в том числе представляющих более ранние ветви древа Dictyostelia — по сути неизученными. Эти упущенные виды имеют отличные жизненные истории, системы сигналинга и планы строения тела. Чтобы понять, как многоклеточность менялась со временем, учёным нужно уметь манипулировать одними и теми же генами в множестве таких видов и сравнивать результаты бок о бок.
Привнесение CRISPR в разнородную семью амеб
Исследователи адаптировали систему редактирования генома CRISPR/Cas9, изначально оптимизированную для D. discoideum, и проверили, работает ли она по всему дереву Dictyostelia, включая как ранние, так и более производные виды. Они использовали плазмиду — дополнительный круговой фрагмент ДНК — которая несёт инструкции для «молекулярных ножниц» Cas9, направляющую РНК, указывающую Cas9 на выбранный ген, и маркер устойчивости к препарату. Введение этой плазмиды в разные амебы позволило команде разрезать два хорошо изученных гена — stlA и pkaC — важные для сигналов, координирующих агрегацию и формирование плодового тела. У почвенной амебы Polysphondylium violaceum эта стратегия надёжно давала мутанты с явными нарушениями развития, показав, что заимствованная система может работать и за пределами привычной модели.
Проверка генов в разных видах
Далее команда перешла к более отдалённо связанным видам, включая Heterostelium pallidum из Группы 2 и Cavenderia fasciculata из Группы 1 — линиям, разошедшимся раньше в ходе эволюции. Используя ту же конструкцию плазмиды, они разрушили ген pkaC в обоих видах и обнаружили, что мутанты не смогли агрегироваться и сформировать нормальные плодовые тела, что отражает тяжёлые дефекты, наблюдаемые в D. discoideum. Поскольку мутации CRISPR, созданные этим методом, не оставляют громоздких селекционных кассет, полученные штаммы были «безмаркерными». Это облегчило ввод обратно версии гена из D. discoideum и проверку, может ли она заменить местный вариант. Во всех случаях чужой pkaC смог восстановить начальный этап агрегации, но не позднее формирование зрелого плодового тела — свидетельство того, что базовый сигнальный набор разделяется между видами, тогда как тонкая настройка времени и расположения эволюционировала в видовоспецифичных направлениях.
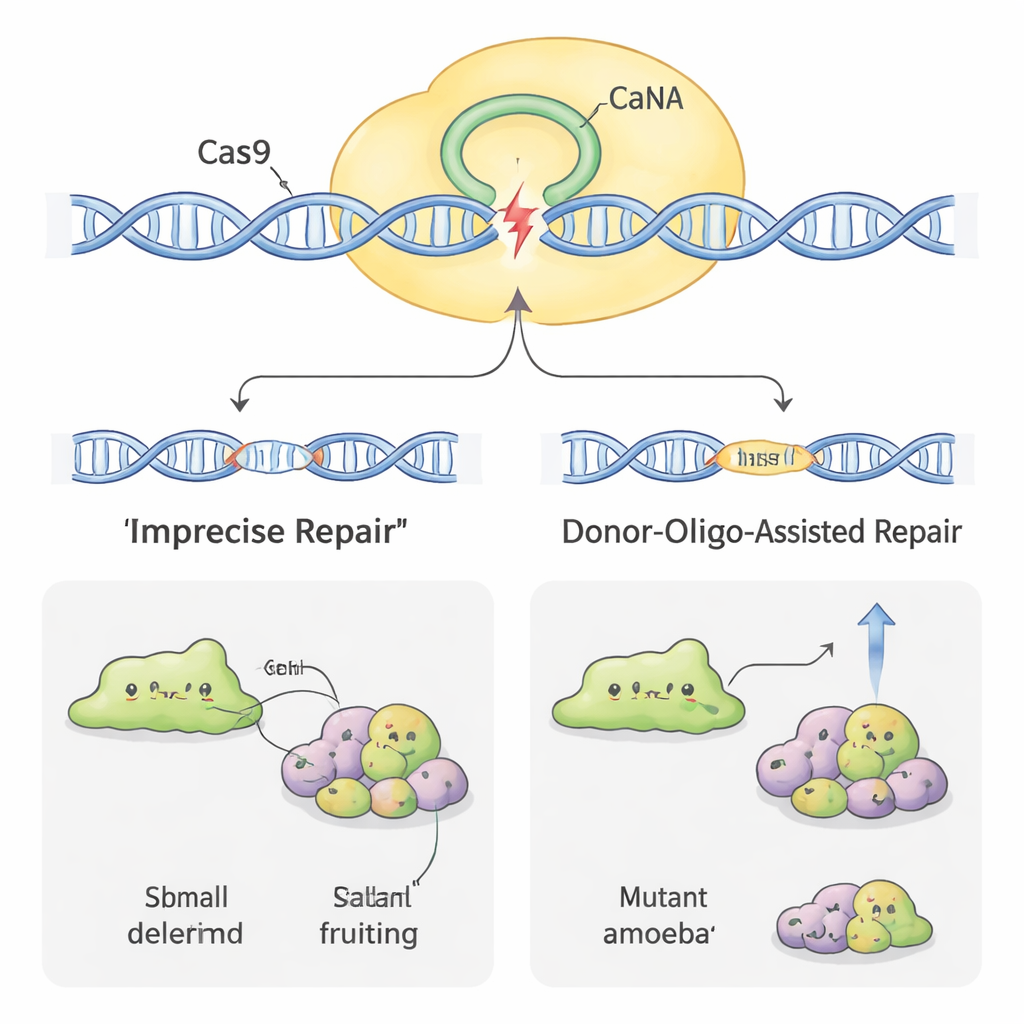
Повышение эффективности редактирования
Не все амебы одинаково легко поддавались редактированию генома. В некоторых видах, например в H. pallidum, первоначальный процент успеха был очень низким. Чтобы повысить эффективность, учёные позаимствовали ещё одну хитрость: добавление коротких «донорных» участков ДНК вместе с CRISPR-плазмидой. Эти доноры несут небольшой тег и стоп-сигнал, окружённые короткими участками, совпадающими с целевым геном. Когда клетка ремонтирует разрез Cas9, используя донора как шаблон, ген надёжно разрушается узнаваемым образом. В D. discoideum это увеличивало долю дефектных клонов и даже позволило получить мутанты без непрерывной селекции лекарством. В более упорном H. pallidum комбинирование донорной ДНК с несколькодневной лекарственной обработкой подняло частоту мутаций почти на порядок, превращая ранее редкие события в нечто близкое к рутине.
Открывая окно в происхождение сложности
Для неспециалиста детали конструкции плазмид и шаблонов ремонта звучат технично, но отдача широка: гибкий набор CRISPR-инструментов, работающий в нескольких ветвях семейства социальных амеб. С его помощью учёные теперь могут сравнивать, как один и тот же ген формирует развитие в разных видах и как тонкие изменения в регуляции генов или структуре белков помогают появляться новым типам клеток и планам строения тела. Иными словами, эта работа даёт исследователям генетические инструменты, необходимые, чтобы в живом виде наблюдать, как эволюция перестраивала одноклеточные организмы для построения кооперативных многоклеточных сообществ.
Цитирование: Oishi, S., Doi, S., Sekida, T. et al. Genome editing across Dictyostelia species enables comparative functional genetics of social amoebas. Sci Rep 16, 7457 (2026). https://doi.org/10.1038/s41598-026-38605-5
Ключевые слова: социальные амебы, редактирование генома CRISPR, эволюция многоклеточности, Dictyostelium, клеточная дифференциация