Clear Sky Science · ru
Изофлуран усугубляет ранее существующую протеотоксичность у взрослых нематод, подавляя функциональную способность митохондрий
Почему это важно для хирургии и здоровья мозга
У многих пожилых людей после операции возникают спутанность сознания и проблемы с памятью — состояние, известное как постоперативный делирий. В этом исследовании поставлен простой, но актуальный вопрос: может ли анестетический газ, используемый для поддержания бессознательного состояния пациента, сделать уже уязвимый мозг ещё более хрупким? На модельных крошечных червях исследователи показали, что широко применяемый анестетик изофлуран может усиливать ранее возникшие повреждения белков в нервных и мышечных клетках, подрывая здоровье митохондрий — генераторов энергии клетки. Полученные данные указывают на новые подходы по защите пациентов из группы риска до операции.
Анестетик, который действует только при уже напряжённом состоянии клеток
Не все мозги одинаково реагируют на анестезию. Команда работала с нематодой C. elegans, микроскопическим червём, биология которого во многом совпадает с человеческой. Часть червей была обычной, часть — генетически модифицирована для производства липких, связанных с болезнями белков, склонных к слипанию, имитируя такие состояния, как болезнь Хантингтона. Когда нормальные черви вдыхали изофлуран несколько часов, их двигательная активность и белковый гомеостаз в основном сохранялись через несколько дней. Но у червей, уже перегруженных аггрегирующимися белками, та же экспозиция анестетика вызывала заметное и длительное ухудшение подвижности — признак того, что клетки не справляются с нагрузкой. Иными словами, изофлуран действовал как дополнительный толчок для системы, находившейся близко к критическому порогу.
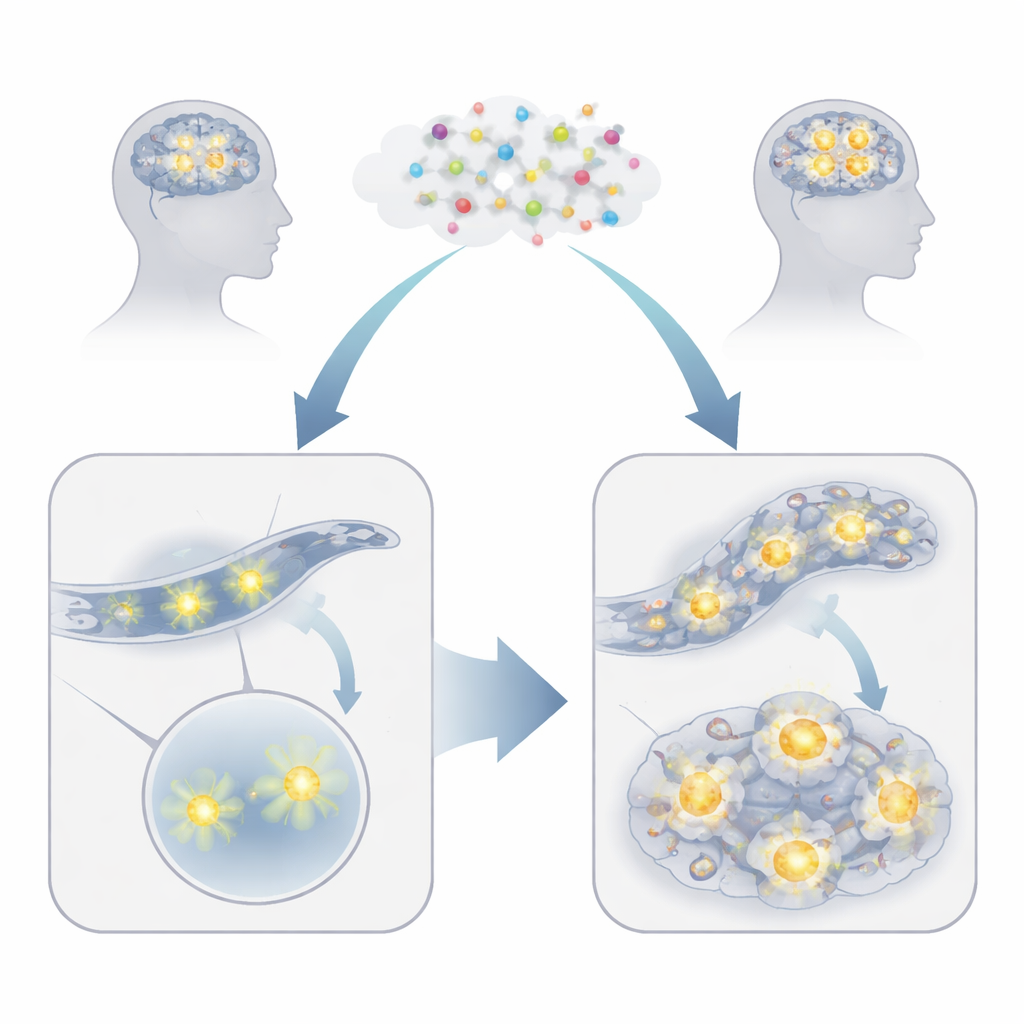
Скрытые изменения в белковых скаплениях и активности генов
При более тщательном рассмотрении исследователи обнаружили, что у анестезированных уязвимых червей формировалось больше видимых белковых фокусов — ярких участков скопления липких белков, — но парадоксально уменьшалось количество крупных, детергент-резистентных агрегатов. Такая картина указывает на сдвиг в сторону меньших, более токсичных собирательств белков, а не в пользу безвредных плотных комков. Одновременно клетки червей перенастроили активность генов: сотни генов, вовлечённых в стресс‑ответы, метаболизм и утилизацию белков, оказались либо включены, либо выключены после воздействия изофлурана, вне зависимости от наличия рискованных белков. Некоторые помощники, например шапероны, участвующие в сворачивании белков, увеличивали свою экспрессию — признак того, что клетки замечали проблему и пытались отреагировать. Тем не менее по крайней мере один шаперон, HSP‑16.41, в присутствии изофлурана усугублял ситуацию, что подчёркивает, как защитная система может стать вредной при неблагоприятных условиях.
Митохондрии в прицеле
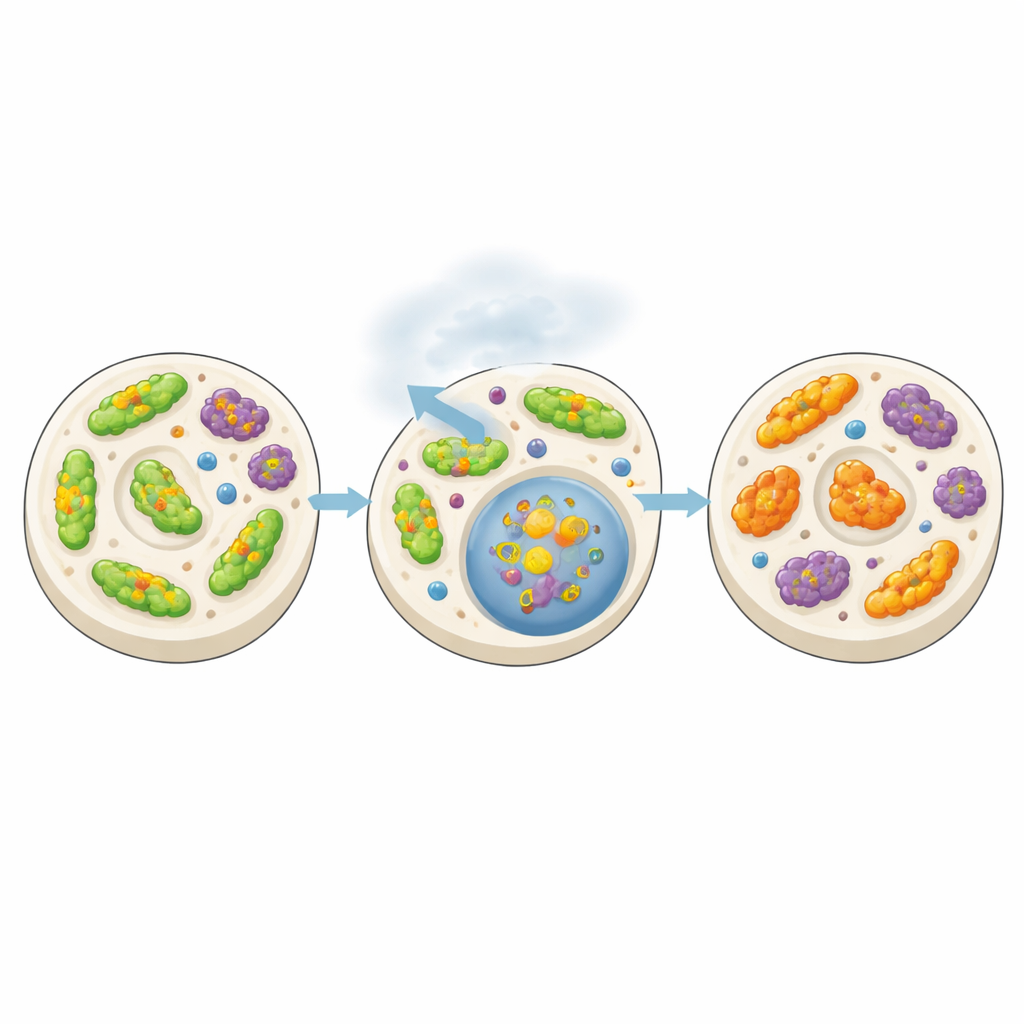
Наиболее заметные изменения проявились, когда команда проанализировала, какие белки фактически попадали в нерастворимые сгустки. У червей с предшествующим белковым стрессом многие из вновь агрегировавших белков происходили из митохондрий, особенно из их внутренней аппаратуры и каналов импорта белков. Когда исследователи ослабляли экспрессию tomm‑20 — ключевого «дверного» белка, помогающего транспортировать другие белки в митохондрии — изофлуран больше не усугублял проблемы с движением ни в мышечных, ни в нервных клетках. Другие компоненты митохондрий, такие как субъединица комплекса I GAS‑1, также влияли на чувствительность червей к анестетику. В совокупности эти результаты указывают на митохондрии как на центральную сцену, на которой разворачивается токсичное взаимодействие между анестезией и повреждением белков.
Когда клеточная уборка заходит слишком далеко
Клетки поддерживают митохондрии через путь утилизации под названием митофагия, который маркирует повреждённые органеллы для удаления. Команда обнаружила, что этот процесс, обычно защитный, может превратиться в палку о двух концах. Воздействие изофлурана усиливало активность нескольких генов, связанных с общей клеточной очисткой и митофагией. Тем не менее подавление отдельных участников митофагии, особенно киназы PINK‑1 и рецепторов груза SQST‑1, SQST‑2 и LGG‑1, фактически защищало червей от вредных эффектов анестетика. У червей, перегруженных липкими белками, изофлуран, по-видимому, сдвигал баланс в сторону избыточного удаления митохондрий при недостаточной их замене, оставляя клетки с меньшим числом здоровых «энергетических станций». Подкрепляя эту идею, малое молекулярное соединение, известное как VL‑004 и улучшающее функцию митохондрий, помогло восстановить их численность и частично вернуть подвижность анестезированных червей с белковым стрессом.
Что это может значить для пациентов после операции
Проще говоря, работа показывает, что изофлуран может углублять повреждение белков и функциональный упадок, но главным образом в тех клетках, которые уже находятся на грани из‑за возрастных или наследственных уязвимостей. Путём чрезмерной активации митохондриальной очистки и несоответствующего стимулирования роста новых митохондрий анестетик делает эти клетки бедными по энергии и менее способными справляться с токсичными формами белков. Хотя черви не равны людям, основные исследованные процессы хорошо консервативны между видами, и результаты предлагают механистическую связь между летучими анестетиками, митохондриальным стрессом и длительными когнитивными проблемами после операции. Исследование ставит вопрос, что точная настройка митохондриальной функциональности — возможно, с препаратами вроде VL‑004 или посредством модуляции путей митофагии — могла бы помочь снизить риск постоперативного делирия у пациентов с предсуществующими нарушениями когнитивной функции или обработки белков.
Цитирование: Elami, T., Zhu, H., Bruck-Haimson, R. et al. Isoflurane aggravates pre-existing proteotoxicity in adult nematodes by suppressing mitochondrial fitness. Sci Rep 16, 8098 (2026). https://doi.org/10.1038/s41598-026-38591-8
Ключевые слова: постоперативное делирий, изофлуран, митохондрии, агрегация белков, C. elegans