Clear Sky Science · ru
Активированные Т-клетки индуцируют апоптоз в клетках аденокарциномы легкого A549 через вход кальция, опосредованный TRPV4
Почему это исследование важно для рака легкого
Рак легкого по-прежнему остаётся одним из наиболее смертоносных видов рака, отчасти потому, что опухоли часто вырабатывают устойчивость к стандартным методам лечения, таким как химио- и лучевая терапии. В последние годы использование собственной иммунной системы организма вселило новую надежду. В этом исследовании рассматривается новый поворот в этой идее: показано, как определённый тип иммунных клеток — активированные Т-клетки — может подтолкнуть раковые клетки легкого к самоуничтожению, заставляя их пропускать кальций через молекулярные «ворота» TRPV4. Понимание этого пути может помочь учёным разработать более мощные и точные иммунотерапии.
Воины иммунной системы встречаются с опухолевыми клетками легкого
Исследователи сосредоточились на человеческих клетках аденокарциномы легкого, известных как клетки A549, широко используемой модели немелкоклеточного рака легкого. Они сочетали эти раковые клетки с клетками Jurkat, которые служат замещающим моделем для киллерных Т-клеток организма, которые обычно обнаруживают и уничтожают инфицированные или злокачественные клетки. Химической активацией клеток Jurkat команда имитировала состояние повышенной готовности Т-клеток, характерное для реального иммунного ответа. Затем активированные или неактивированные Т-клетки смешивали с раковыми клетками легкого в разных соотношениях и наблюдали в течение одного-трёх дней, особенно отслеживая выживаемость раковых клеток и долю клеток, подвергшихся программируемой клеточной смерти — апоптозу.
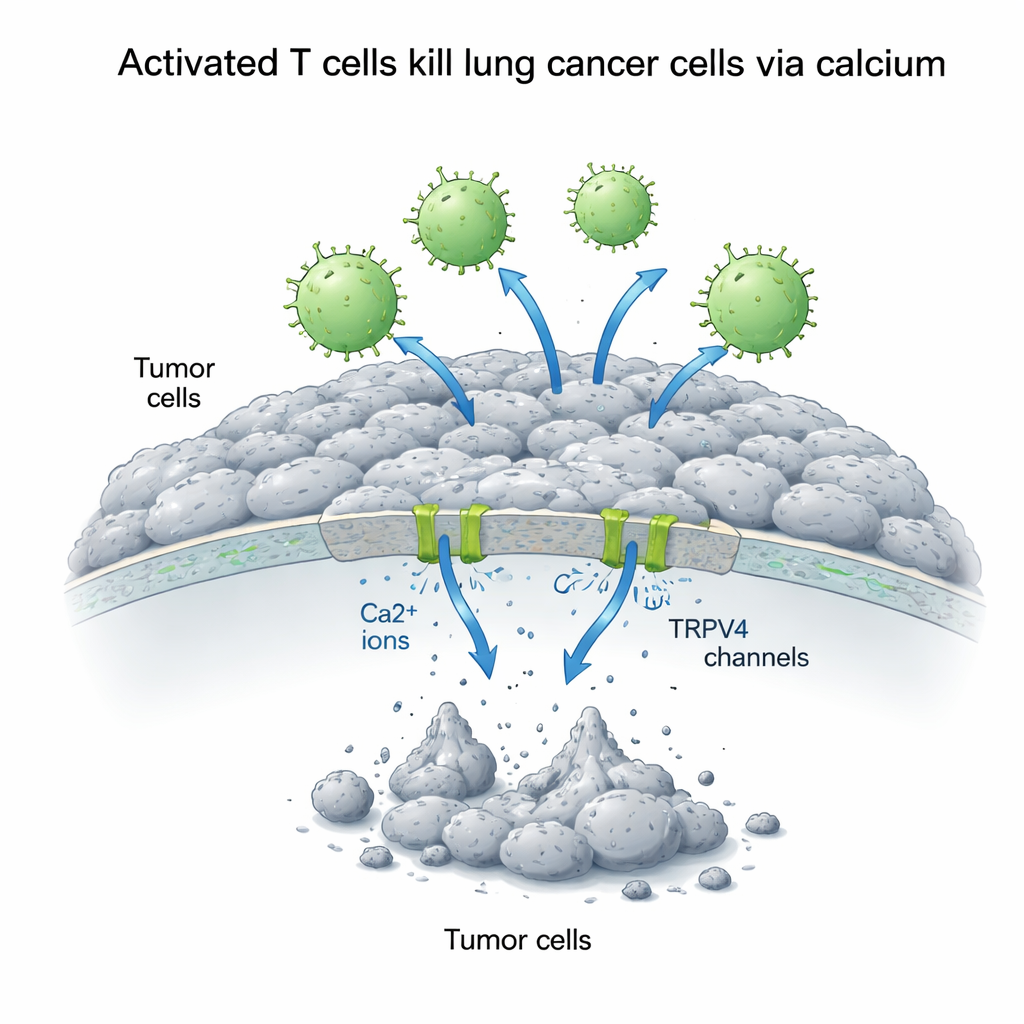
Кальций как двусторонний сигнал для раковых клеток
Внутриклеточный кальций действует как универсальный переключатель сигналов: он может либо стимулировать рост, либо запускать гибель, в зависимости от того, как он регулируется. Учёные увеличили концентрацию кальция вне клеток A549 и измеряли, как это влияет на противостояние между Т-клетками и опухолевыми клетками. Удивительно, но дополнительный кальций сам по себе улучшал рост раковых клеток легкого, что говорит о том, что в спокойных условиях кальций подпитывает пути выживания. Но в присутствии активированных Т-клеток картина изменилась: повышенный внешний кальций существенно усиливал убивающее действие Т-клеток. В течение 72 часов выживаемость раковых клеток упала до менее чем трети нормы при сочетании активированных Т-клеток и дополнительного кальция, тогда как неактивные Т-клетки почти не влияли или даже могли поддерживать рост при добавлении кальция.
Кальциевые «ворота», связанные со стрессом и гибелью клеток
Чтобы понять, как происходит этот переход от роста к гибели, команда изучила TRPV4 — белковый канал в клеточной мембране, пропускающий кальций внутрь клетки. С помощью белкового анализа они обнаружили, что уровень TRPV4 резко повышается при воздействии добавленного кальция на клетки A549, независимо от присутствия Т-клеток, и достигает максимума при сочетании кальция и активированных Т-клеток. Одновременно раковые клетки демонстрировали явные признаки оксидативного стресса: баланс смещался в сторону вредных окислителей (повышался общий оксидантный статус) и от защитных антиоксидантов (снижалась общая антиоксидантная ёмкость). Проточная цитометрия — метод, маркирующий клетки флуоресцентными красителями — подтвердила, что активированные Т-клетки вызывали всплеск как ранних, так и поздних стадий апоптоза, особенно при избытке кальция. В совокупности эти наблюдения указывают на цепочку событий, в которой каналы TRPV4 пропускают больше кальция, что затем вызывает химический стресс внутри клетки и толкает её к гибели.
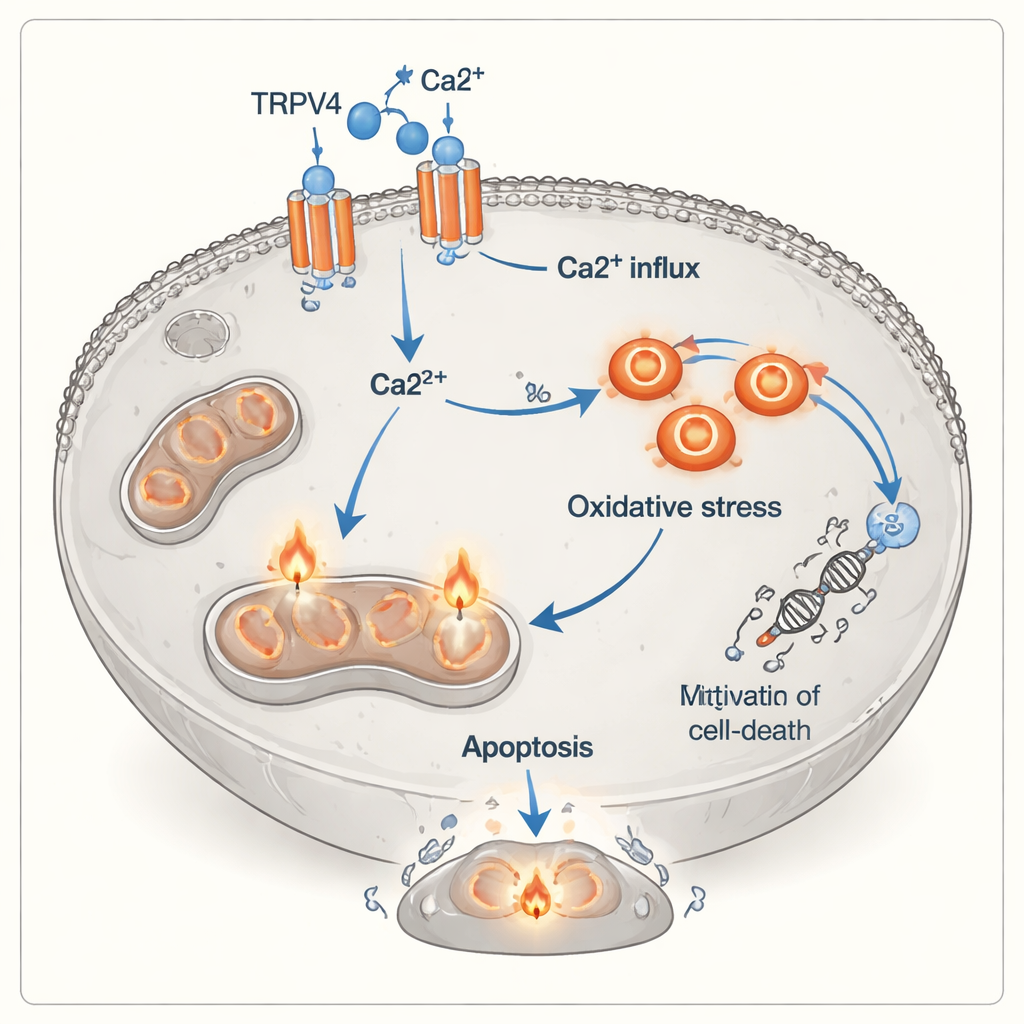
Новый уровень понимания, как иммунные клетки убивают опухоли
Классически киллерные Т-клетки уничтожают свои цели, выделяя токсические белки или активируя рецепторы смерти на поверхности раковой клетки. Это исследование предлагает ещё один, более косвенный путь: сигналы от активированных Т-клеток — включая воспалительные молекулы и тесный контакт клетка-к-клетке — по-видимому делают раковые клетки легкого более зависимыми от TRPV4 и более уязвимыми к перегрузке кальцием и оксидативному повреждению. В этой интерпретации TRPV4 действует как переключатель чувствительности, который превращает кальций, обычно стимулирующий рост, в летальный сигнал. Хотя эксперименты проводилиcь в культурах клеток и на одной линии раковых клеток, они подчеркивают потенциально важный мост между иммунной атакой, ионными каналами и внутренними механизмами стресса опухолевых клеток.
Что это может означать для будущих методов лечения
Для неспециалистов ключевое сообщение таково: успех иммунотерапии может зависеть не только от усиления Т-клеток, но и от повышения уязвимости самих раковых клеток. Нацеливание на TRPV4 или связанные кальциевые каналы может в будущем повысить способность Т-клеток ликвидировать опухоли легкого или позволить точнее настраивать лечение, чтобы избежать повреждения здоровых тканей. Работа находится на ранней стадии, и авторы подчёркивают необходимость дальнейших экспериментов на животных и в более сложных моделях. Тем не менее открытие оси TRPV4–кальций–оксидативный стресс добавляет перспективную новую цель в набор инструментов для улучшения иммуно-ориентированных методов лечения рака легкого.
Цитирование: Alavi, F., Kazemi-Lomedasht, F., Eftekhari, Z. et al. Activated T cells induce apoptosis in A549 lung adenocarcinoma cells via TRPV4-mediated calcium influx. Sci Rep 16, 7155 (2026). https://doi.org/10.1038/s41598-026-38589-2
Ключевые слова: иммунотерапия рака легкого, Т-клетки, кальциевые сигналы, канал TRPV4, оксидативный стресс