Clear Sky Science · ru
Оптимизация агентов, связывающихся с галектином‑3, с помощью синтеза множества соединений in situ и нативной масс-спектрометрии
Почему это важно для будущих лекарств
Многие современные лекарства действуют, присоединяясь к белкам в организме, но найти малую молекулу, которая прочно и селективно связалась бы с нужным участком, сложно, дорого и часто разочаровывающе. В этом исследовании предложен более быстрый способ доводить такие молекулы непосредственно в присутствии целевого белка и затем выявлять победителей при помощи очень чувствительного метода взвешивания. Авторы демонстрируют подход на галектине‑3, белке, связанном с ростом рака, и получают перспективный кандидат, похожий по силе связывания на лучшие существующие соединения, но связывающийся в неожиданном кармане на поверхности белка.

Переосмысление поиска лучших лидов для лекарств
Традиционная оптимизация лекарств напоминает дорогую игру в угадайку. Химики изменяют исходное соединение шаг за шагом, тестируют каждую версию и надеются улучшить прочность связывания с белком-мишенью. Но поверхности белков гибкие, молекулы воды мешают, а само связывание может перестроить белок, из‑за чего компьютерные прогнозы ненадёжны. Даже при наличии высокоразрешающей структуры нет гарантии, что предлагаемое изменение поможет. Существующие «целеподдержанные» методы пытаются позволить белку выбирать партнёров из набора строительных блоков, но эти подходы всё ещё зависят от сложного анализа и косвенных сигналов, чтобы вывести, какое соединение действительно связывается лучше всего.
Пусть белок выберет, а затем взвесьте победителей
Исследователи объединили две идеи в единый упрощённый рабочий процесс. Сначала они использовали обратимую химическую реакцию, которая связывает общий сахаро‑подобный сердечник с множеством различных боковых фрагментов в одной пробирке, формируя смесь родственных молекул. Тщательная регулировка исходных соотношений позволяет продуктам прийти к равновесному распределению, управляемому простыми законами концентрации, что выравнивает их количества несмотря на различия в реакционной способности. Затем они подвергали эту смесь действию галектина‑3 и исследовали её нативной масс‑спектрометрией — вариантом масс‑спектрометрии, который сохраняет пары белок–молекула в целостности в мягком, водоподобном растворе. Поскольку у каждого кандидата своя масса, прибор может прямо обнаружить, какие молекулы действительно связаны с белком, без меток или эталонов.
От переполненных смесей к выдающемуся связывающему агенту
С помощью этой схемы команда создала десятки связывающих галектин‑3 соединений, присоединяя разные боковые группы к сахаро‑ядру, вдохновлённому известным ингибитором GB1107. Они разбили 35 различных гидразидных фрагментов на управляемые группы, сформировали все комбинации in situ и затем добавили галектин‑3. Нативная масс‑спектрометрия выявила те соединения, которые чаще всего «путешествовали» вместе с белком, отмечая их как основные попадания. Последующий тест термической стабильности, измеряющий, как соединение стабилизирует белок при нагревании, отсеял ложноположительные результаты, вызванные артефактами газовой фазы измерения. Остались три ведущих кандидата, и детальные измерения связывания по тепловым изменениям показали, что один из них, названный GalAldBZ20, связывается с галектином‑3 особенно прочно — в субмикромолярном диапазоне.
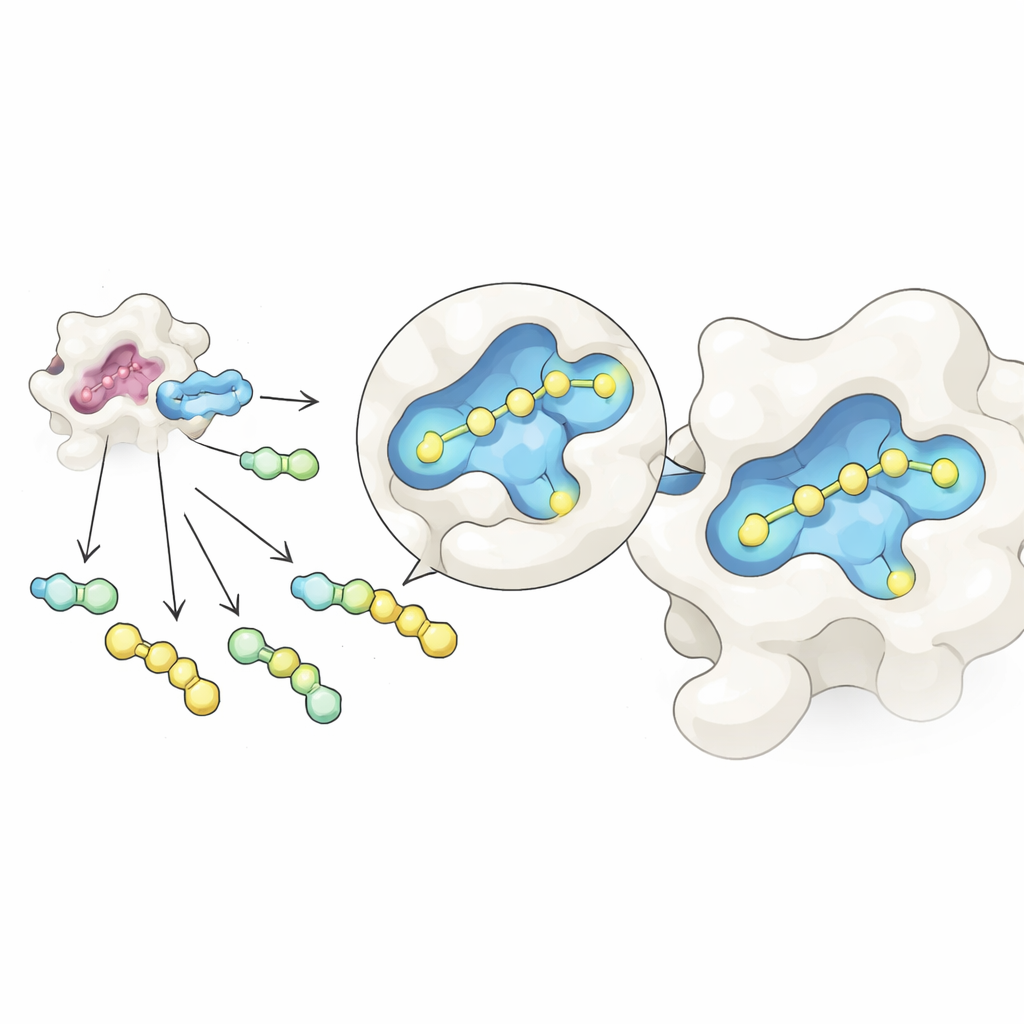
Открытие скрытого кармана и его укрепление
Следующий сюрприз произошёл, когда команда рассмотрела, как GalAldBZ20 располагается на поверхности галектина‑3. Большинство известных связывающих используют «альфа» карман рядом с сахаросвязывающим участком, но структурные методы и компьютерные симуляции показали, что GalAldBZ20 предпочитает соседний «бета» карман. Рентгеновская кристаллография дала наводки на это, ядерный магнитный резонанс в растворе выявил множественные локальные конформации рядом с этим карманом, а молекулярно‑динамические симуляции поддержали модель, в которой нитросодержащий ароматический фрагмент молекулы разместился в бета‑сайте. Рассуждая, что можно закрепить такое расположение прочнее, химики переработали химический звено между сахаром и нитро‑кольцом, чтобы поощрить новые полярные контакты с белком и уменьшить гибкость.
Преобразование умного скрининга в мощный кандидат
Имея это понимание, команда синтезировала небольшой набор более жёстких последующих молекул, сохранив сахар и нитро‑кольцо, но изменив связующее между ними. Одна версия, N‑галактозид (соединение 5), выделилась: она связывалась с галектином‑3 примерно в десять раз прочнее, чем исходный хит, достигая силы связывания, сопоставимой с GB1107, при этом всё ещё предпочитая бета‑карман. Ультра‑высокое разрешение кристаллографической структуры показало чёткую электронную плотность для нитро‑кольца в этом кармане, поддерживаемую несколькими водородными связями и катион‑π контактом с ключевыми аминокислотами. Удаление нитро‑группы или замена её на простой метил существенно ослабляло связывание, подчёркивая её значимость. Поскольку галектин‑1, родственный белок, лишён этого бета‑кармана, новое соединение потенциально обеспечивает лучшую селективность — важное свойство при разработке лекарств.
Что это значит для будущих исследований лекарств
Говоря доступным языком, эта работа показывает: можно смешать множество родственных молекул, позволить релевантному заболеванию белку «выбрать» фаворитов и затем прямо «взвесить» пары белок–молекула, чтобы увидеть, что лучше прилипает. Применённый к галектину‑3, этот подход неожиданно обнаружил и затем усилил связывание с менее изученным карманом, получив соединение, сопоставимое с лучшими существующими ингибиторами и пригодное в качестве лида для новых противораковых препаратов. Более широко, сочетание in situ химии с нативной масс‑спектрометрией предлагает общий кратчайший путь для оптимизации лидов против белков с несколькими возможными участками связывания, что может сэкономить время, материалы и усилия на ранних этапах разработки лекарств.
Цитирование: Hoshi, K., Konuma, T., Taguchi, R. et al. Optimization of galectin-3 binding agents by in situ multiple compound synthesis and native mass spectrometry. Sci Rep 16, 8453 (2026). https://doi.org/10.1038/s41598-026-38570-z
Ключевые слова: ингибиторы галектина‑3, нативная масс-спектрометрия, фрагментно-ориентированное обнаружение препаратов, целеподдержанный синтез, лиды противораковых препаратов