Clear Sky Science · ru
Сравнение и комбинирование ксевинапанта с ингибированием ATR и PARP для радиосенсибилизации клеток HPV‑негативного ПНКОР
Почему усиление действия радиации важно
Лучевая терапия — основной метод лечения опухолей ротовой полости и глотки, но многие опухоли ей сопротивляются, что вынуждает врачей применять высокие дозы, способные повредить нормальные ткани. В этом исследовании поставлен практический вопрос с большим значением для пациентов: какие из современных противоопухолевых препаратов, задуманных чтобы делать раковые клетки более уязвимыми, действительно лучше всего работают в сочетании с радиацией против трудноподдающихся HPV‑негативных опухолей головы и шеи, выращенных в лаборатории?
Текущее лечение и его ограничения
Пациентов с местно‑распространенным плоскоклеточным раком головы и шеи часто лечат сочетанием лучевой терапии и химиопрепарата цисплатина или проводят операцию с последующей лучевой терапией. Хотя такой подход может контролировать болезнь, он нередко оставляет пациентов с серьезными долгосрочными побочными эффектами — затруднениями при глотании, сухостью во рту, нарушениями слуха и повреждением почек. Многие пожилые или медицински хрупкие пациенты вовсе не переносят цисплатин. Это стимулировало повышенный интерес к «радиосенсибилизаторам» — препаратам, которые делают опухолевые клетки легче уничтожаемыми радиацией, так что лечение может стать результативнее или, возможно, менее токсичным.
Многообещающий препарат, который подвел
Один из таких препаратов, ксевинапант, поначалу воспринимали как прорыв. Он имитирует природный белок SMAC и блокирует молекулы, помогающие раковым клеткам избегать запрограммированной гибели. В предыдущих исследованиях добавление ксевинапанта к стандартной хеморадиотерапии улучшало исходы в фазе 2 клинического испытания при раке головы и шеи, что породило надежды на новый стандарт лечения. Однако гораздо крупное фазовое исследование 3‑й фазы TrilynX было остановлено досрочно: промежуточный анализ показал не только отсутствие пользы, но и худшую выживаемость и больше побочных эффектов в группе с ксевинапантом. Это неожиданное поражение создало острую необходимость переоценить, насколько ксевинапант действительно усиливает радиацию, и сравнить его с другими, более новыми стратегиями.
Три стратегии в прямом сравнении
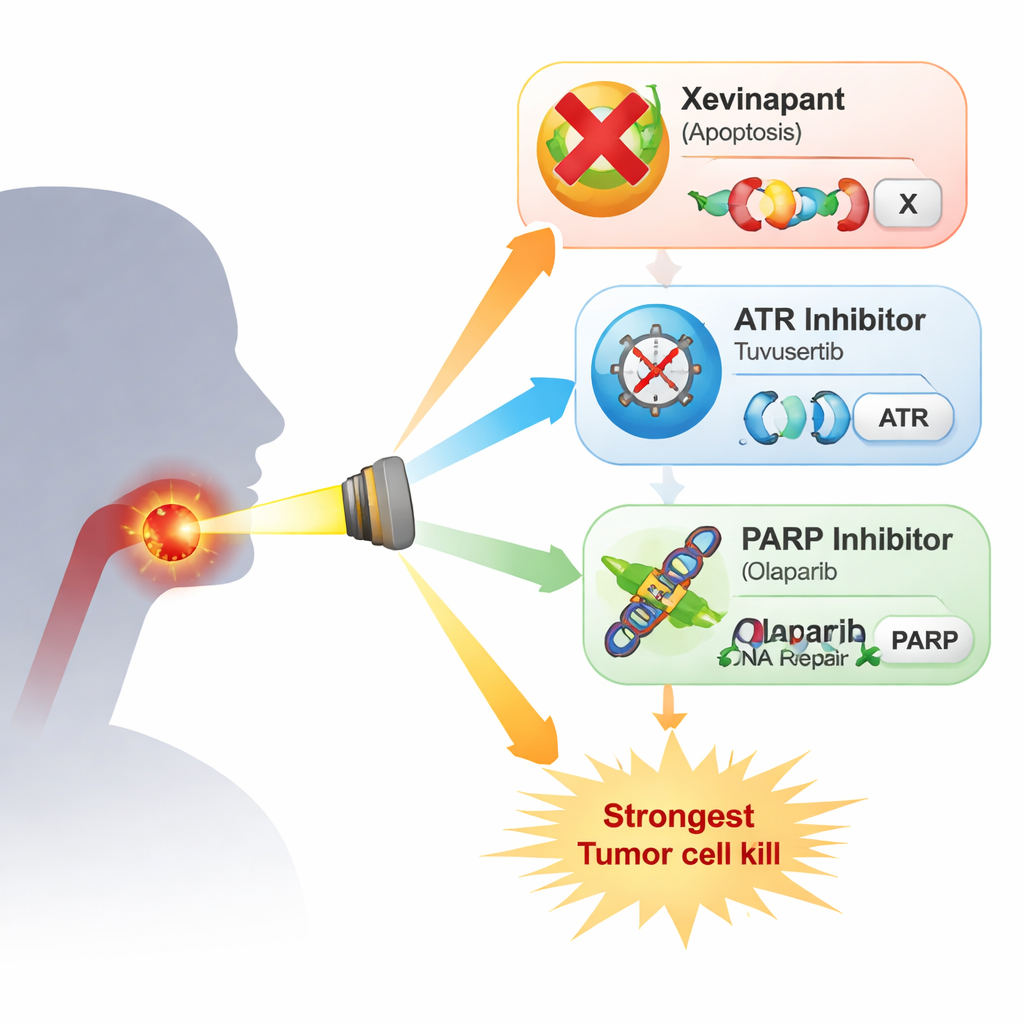
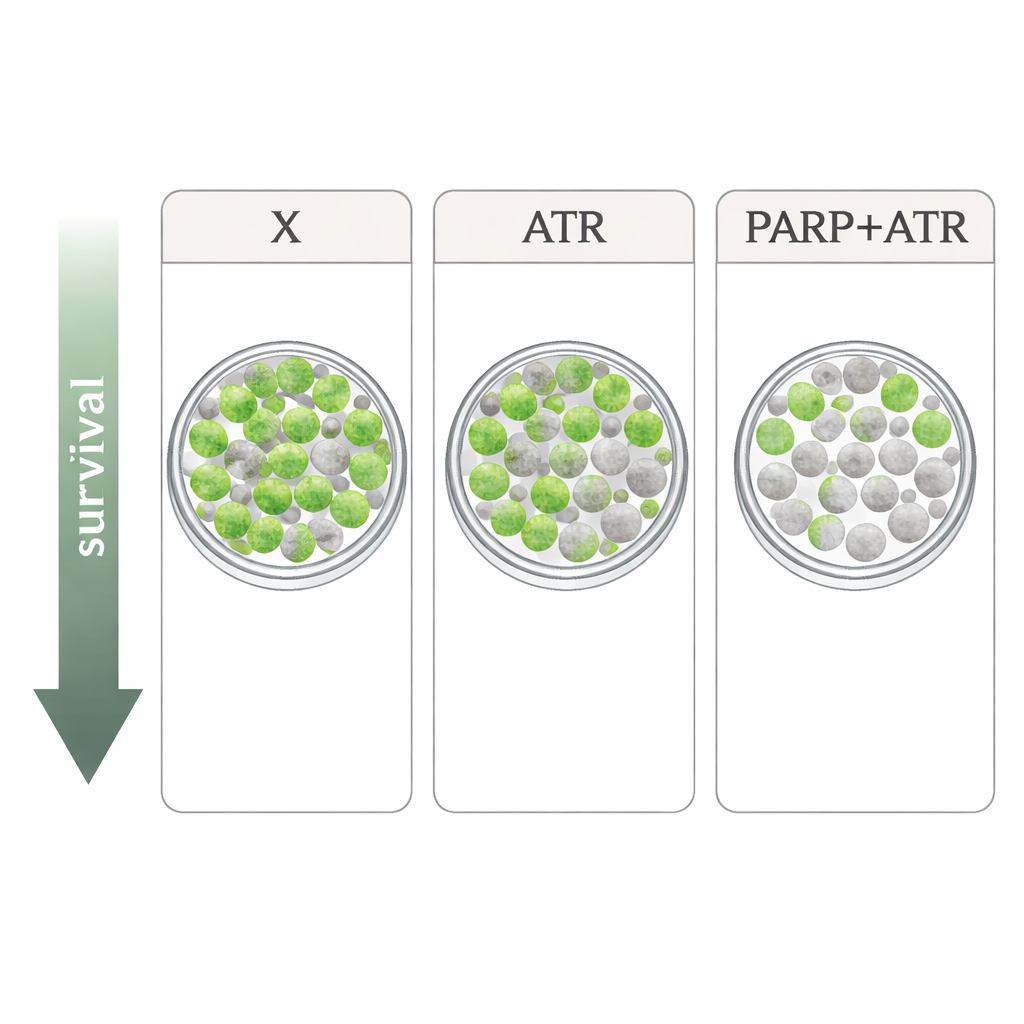
Исследователи изучили четыре радиационно‑устойчивые HPV‑негативные клеточные линии рака головы и шеи. Они сравнили ксевинапант с двумя препаратами, нацеленными на ответ клетки на повреждение ДНК: ингибитором ATR тухусертрибом и ингибитором PARP олапараибом, оба применяли в дозах, сопоставимых с достижимыми у пациентов. ATR и PARP — ключевые факторы, помогающие клеткам приостанавливать клеточный цикл и восстанавливать ДНК после повреждения, например, вызванного рентгеновскими лучами. В простых тестах роста каждый препарат по‑отдельности лишь умеренно замедлял пролиферацию, и эффект варьировал между линиями. В сочетании с радиацией в самом строгом варианте — учете способности отдельных клеток формировать колонии — картина прояснилась: ксевинапант давал лишь слабый или вовсе отсутствующий дополнительный радиационный эффект в нескольких линиях, тогда как и тухусертиб, и олапараиб последовательно делали радиацию более летальной. Наибольший эффект наблюдали при комбинированном ингибировании ATR и PARP, что приводило к особенно сильному падению выживаемости колоний в трех из четырех клеточных линий.
Сигналы клеточной гибели — не вся история
Поскольку ксевинапант нацелен на запуск клеточной гибели, команда также измеряла долю клеток, ставших апоптотическими или лизированными после лечения с радиацией и без нее. Эти маркеры гибели заметно увеличивались в некоторых условиях — особенно в одной клеточной линии HSC4 и при сочетании препаратов — но не коррелировали надежно с тем, насколько эффективно радиация подавляла длительную выживаемость. Иными словами, краткосрочные показатели гибели плохо предсказывали истинную радиосенсибилизацию. Это несоответствие подчеркивает ключевой урок для разработки лекарств: лишь тесты, отслеживающие клетки достаточно долго, чтобы увидеть, могут ли они восстановиться — такие как тесты на образование колоний — адекватно оценивают эффективность радиосенсибилизатора.
Что это значит для будущего лечения
Из лабораторных экспериментов видно, что ксевинапант имеет некоторое способность усиливать действие радиации в HPV‑негативных клетках рака головы и шеи, но его эффект был слабее и менее стабильным по сравнению со стратегиями, которые непосредственно нарушают обработку повреждений ДНК через ATR и PARP. Сочетание ингибиторов ATR и PARP давало самый мощный результат, что указывает на то, что тщательно дозированные комбинации этих препаратов с радиотерапией могут представлять более перспективный путь, чем дальнейшее продвижение ксевинапанта, по крайней мере для этого типа рака. Перенос этих результатов в клинику будет непростым, поскольку такие препараты также могут повреждать нормальные быстро делящиеся ткани и в ранних испытаниях уже требовали снижения доз. Тем не менее работа нацеливает клиницистов и исследователей на стратегии, ориентированные на репарацию ДНК, как на более убедительные кандидаты для повышения эффективности лучевой терапии и, возможно, повышения ее безопасности для пациентов, которые не могут получать стандартную химиотерапию.
Цитирование: Roehrle, J., Perugachi-Heinsohn, A., Gatzemeier, F. et al. Comparing and combining xevinapant with ATR and PARP inhibition for the radiosensitization of HPV-negative HNSCC cells. Sci Rep 16, 5882 (2026). https://doi.org/10.1038/s41598-026-38550-3
Ключевые слова: рак головы и шеи, лучевая терапия, ингибиторы репарации ДНК, ксевинапант, радиосенсибилизация