Clear Sky Science · ru
Исследование токсического механизма, посредством которого циперметрин вызывает нейродегенеративные заболевания, с помощью сетевой токсикологии и молекулярного докинга
Повседневные спреи от насекомых и стареющий мозг
От ферм до кухонь в домах — инсектициды помогают бороться с вредителями, но некоторые из этих химикатов не просто исчезают после использования. В этом исследовании рассматривают циперметрин, широко применяемый инсектицид, и задают вопрос с реальными последствиями: может ли долгосрочное воздействие незаметно повышать риск развития заболеваний мозга, таких как болезнь Альцгеймера и Паркинсона? С помощью современных компьютерных методов исследователи строят карту возможных взаимодействий этого вещества с организмом и мозгом, давая раннее предупреждение о загрязнителе, с которым многие сталкиваются, не подозревая об этом.
Почему нейроны так трудно защитить
Нейродегенеративные заболевания, включая болезни Альцгеймера, Паркинсона и другие формы деменции, — это состояния, при которых нервные клетки мозга постепенно погибают и не восстанавливаются. По мере их утраты люди теряют память, способности к мышлению и контроль над движениями. В то же время в современном мире растёт использование пестицидов, и несколько долгосрочных популяционных исследований показали, что в сообществах с более интенсивным применением пестицидов выше уровни этих заболеваний мозга. Эксперименты на животных и клетках указывают, что пиретроидные инсектициды, такие как циперметрин, могут повреждать клетки мозга через окислительный стресс (химическое «ржавение») и длительное воспаление. Но до настоящего времени учёные не имели ясной картины того, как именно это конкретное химическое соединение на молекулярном уровне связано с человеческой нейродегенерацией.
Построение цифровой карты химического вреда
Для решения этой задачи команда обратилась к «сетевой токсикологии» — подходу больших данных, который объединяет информацию из множества биологических баз данных. Сначала они предсказали, с какими человеческими белками циперметрин мог бы потенциально связываться, сравнивая его структуру с тысячами известных соединений. Затем собрали сотни генов и белков, уже связанных с нейродегенеративными заболеваниями, из основных медицинских и генетических ресурсов. Перекрыв эти два списка, они обнаружили 108 общих мишеней — белков, которые и взаимодействуют с циперметрином, и ассоциированы с дегенерацией мозга. После этого они построили большую карту взаимодействий, показывающую, как эти белки «общаются» внутри клеток, и с её помощью выделили 19 «хабовых» белков, которые кажутся особенно центральными для потенциальных токсических эффектов циперметрина.
Ключевые белки в центре проблемы
Некоторые из наиболее важных хабовых белков играют хорошо известные роли в здоровье мозга. Например, APOE помогает управлять жирами в мозге и тесно связан с риском развития болезни Альцгеймера, а A2M участвует в удалении вредных агрегатов белков. Другие, такие как AKT1 и SRC, находятся в крупных сигнальных путях, контролирующих выживание или гибель клеток. Исследователи сосредоточились на трёх конкретных белках: CREBBP, который помогает включать и выключать гены и поддерживает формирование памяти; GSK3B, сигнальном ферменте, давно связанном с аномальными белковыми отложениями в мозге и воспалением; и ALB, основном белке крови, переносящем химикаты по организму и способном попадать в мозг при повреждении гематоэнцефалического барьера. При проведении подробных компьютерных симуляций «докинга» циперметрин плотно размещался в карманах каждого из этих белков, что указывает на то, что он может реально связываться и изменять их поведение.
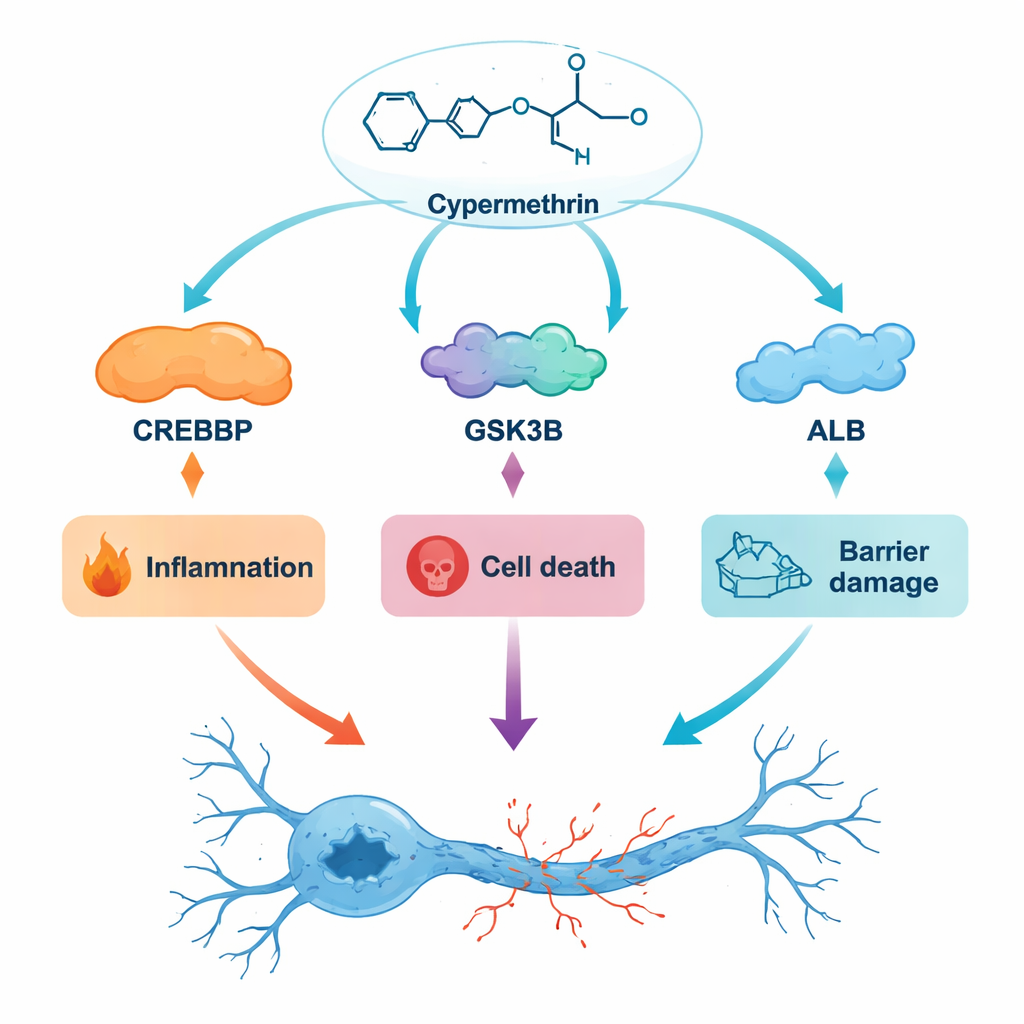
Моделирование повреждений на молекулярном уровне
Чтобы выяснить, были ли эти соответствия стабильными или мимолётными, команда провела виртуальные «фильмы» взаимодействия белков и циперметрина в течение 100 наносекунд, отслеживая, насколько структуры колеблются. Во всех трёх случаях комплексы стабилизировались в устойчивые формы, что подтверждает идею о том, что циперметрин может прочно закрепляться за этими белками достаточно долго, чтобы иметь биологическое значение. Наблюдаемые шаблоны согласуются с известными механизмами заболеваний: участие GSK3B указывает на усиление воспаления и неправильную укладку белков в мозге; вмешательство CREBBP может нарушать генетические программы, защищающие нейроны; а сильное связывание с ALB поддерживает идею, что циперметрин может «путешествовать» по крови и влиять на то, какое количество вещества достигает мозга.
Что это значит для людей и общественного здравоохранения
Проще говоря, исследование показывает, что циперметрин действует не на один «выключатель» в мозге, а смещает целую сеть белков в сторону стресса, воспаления и гибели клеток — условий, благоприятных для развития нейродегенеративных заболеваний. Работа не доказывает, что циперметрин вызывает болезнь Альцгеймера или Паркинсона у людей, поскольку опирается на компьютерные модели, а не клинические испытания. Тем не менее она выделяет правдоподобные биологические пути, через которые повседневное воздействие пестицидов может способствовать долгосрочному повреждению мозга, и определяет конкретные белки, которые можно проверить в будущих лабораторных и клинических исследованиях. По мере того как регуляторы и врачи оценивают безопасность распространённых инсектицидов, этот сетевой взгляд даёт важную научную основу для более осторожного использования и разработки ранних диагностических инструментов для людей, находящихся в группе риска.
Цитирование: Li, S., Ding, W., Yu, Y. et al. Exploring the toxic mechanism of cypermethrin-induced neurodegeneration diseases via network toxicology and molecular docking. Sci Rep 16, 7293 (2026). https://doi.org/10.1038/s41598-026-38547-y
Ключевые слова: циперметрин, нейротоксичность пестицидов, нейродегенеративные заболевания, воспаление мозга, загрязнители окружающей среды