Clear Sky Science · ru
Целевая ингибиция HDAC8 с помощью не-гидроксаматных соединений [1,2,4]триазоло[4,3-а]хинолина
Новая надежда при детском раке
Нейробластома — агрессивный детский рак, развивающийся из нервных клеток и часто трудно поддающийся лечению после распространения. В этом исследовании изучается новый подход к замедлению или уничтожению нейробластомных клеток путем выключения ключевого клеточного переключателя — HDAC8. Создавая новую семью молекул, похожих на лекарства и действующих очень селективно на этот переключатель, исследователи стремятся получить препараты, которые будут одновременно более эффективны против опухолей и менее вредны для остального организма.
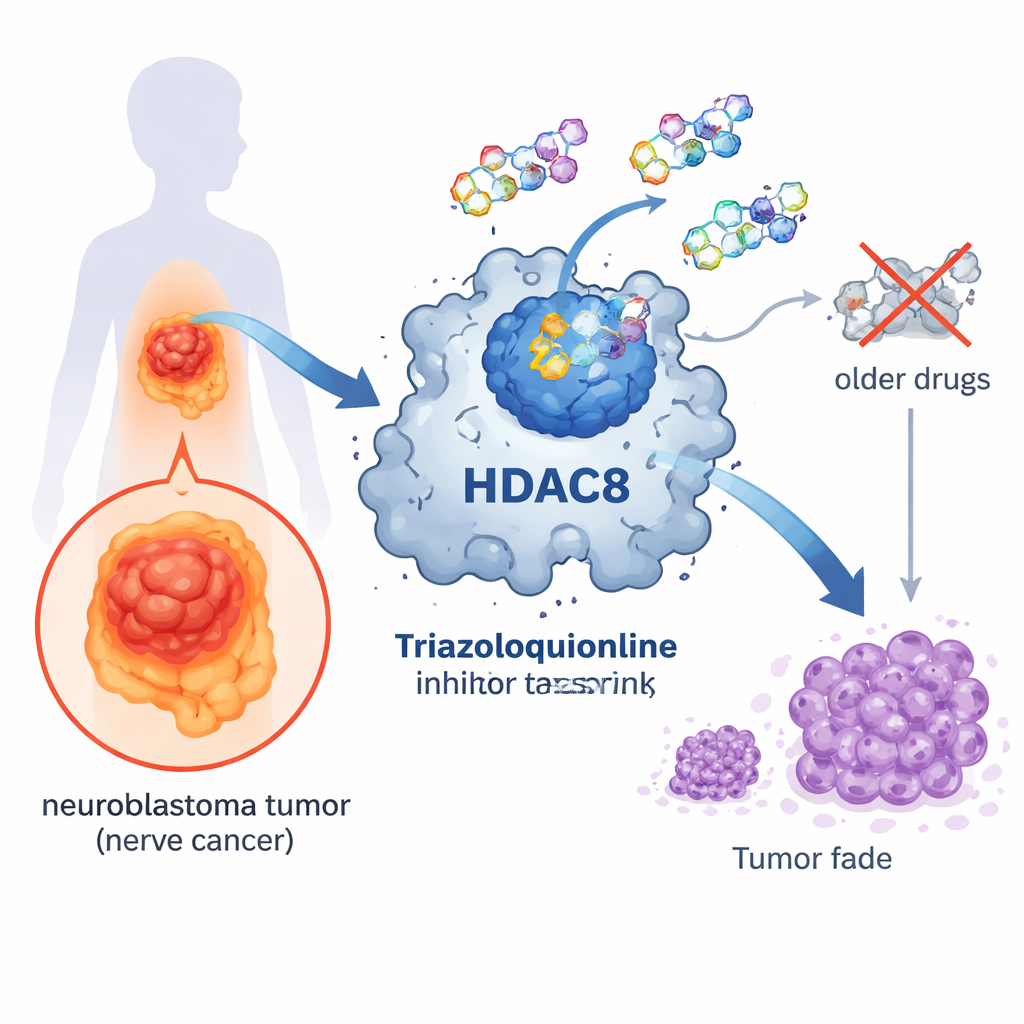
Молекулярный переключатель в центре рака
Внутри наших клеток гены постоянно включаются и выключаются. Одна важная система контроля опирается на крошечные химические метки — ацетильные группы, присоединяющиеся к белкам, связанным с ДНК. Ферменты, называемые гистоновыми деацетилазами (HDAC), снимают эти метки, уплотняя упаковку ДНК и обычно снижая активность генов. HDAC8 — один из членов этого семейства ферментов и связан с несколькими видами рака, включая нейробластому. При избыточной активности HDAC8 раковые клетки легче растут, выживают и распространяются, что делает этот фермент привлекательной мишенью для новых препаратов.
Ограничения старых HDAC-препаратов
Некоторые препараты, блокирующие HDAC, уже одобрены для лечения некоторых заболеваний крови, но они обычно воздействуют на множество типов HDAC одновременно. Большинство таких лекарств используют гидроксаматную химическую группу для захвата иона металла в активном центре фермента. Хотя это эффективно, гидроксамат связывает металлы настолько прочно, что может вызывать побочные эффекты и ограничивать точность различения между разными HDAC. В результате пациенты могут испытывать токсичность, а нормальные клетки страдать наряду с раковыми. Поэтому исследователи ищут альтернативные химические конструкции, сохраняющие антиопухолевый эффект, но уменьшающие нежелательный вред.
Проектирование нового класса таргетных ингибиторов
В этой работе команда спроектировала и синтезировала 21 новое соединение, построенное вокруг скелета триазолохинолина, связанного через гибкий линкер с областью «α-амин амида», способной связывать атом цинка в активном центре HDAC8. Используя компьютерное моделирование, они выбрали такую архитектуру, чтобы втиснуться в узкий «канал выхода ацетата», уникальный для HDAC8 — структурную особенность, способствующую высокой селективности. Подробные докинг-исследования и молекулярно-динамические симуляции показали, что несколько новых молекул — особенно 9m и 9r — формируют стабильные, долговременные взаимодействия в кармане HDAC8 и связываются так же прочно или даже прочнее, чем известный эталонный ингибитор. Важно, что биохимические тесты подтвердили: лучшие соединения сильно блокируют HDAC8, почти не затрагивая другие члены семейства HDAC.
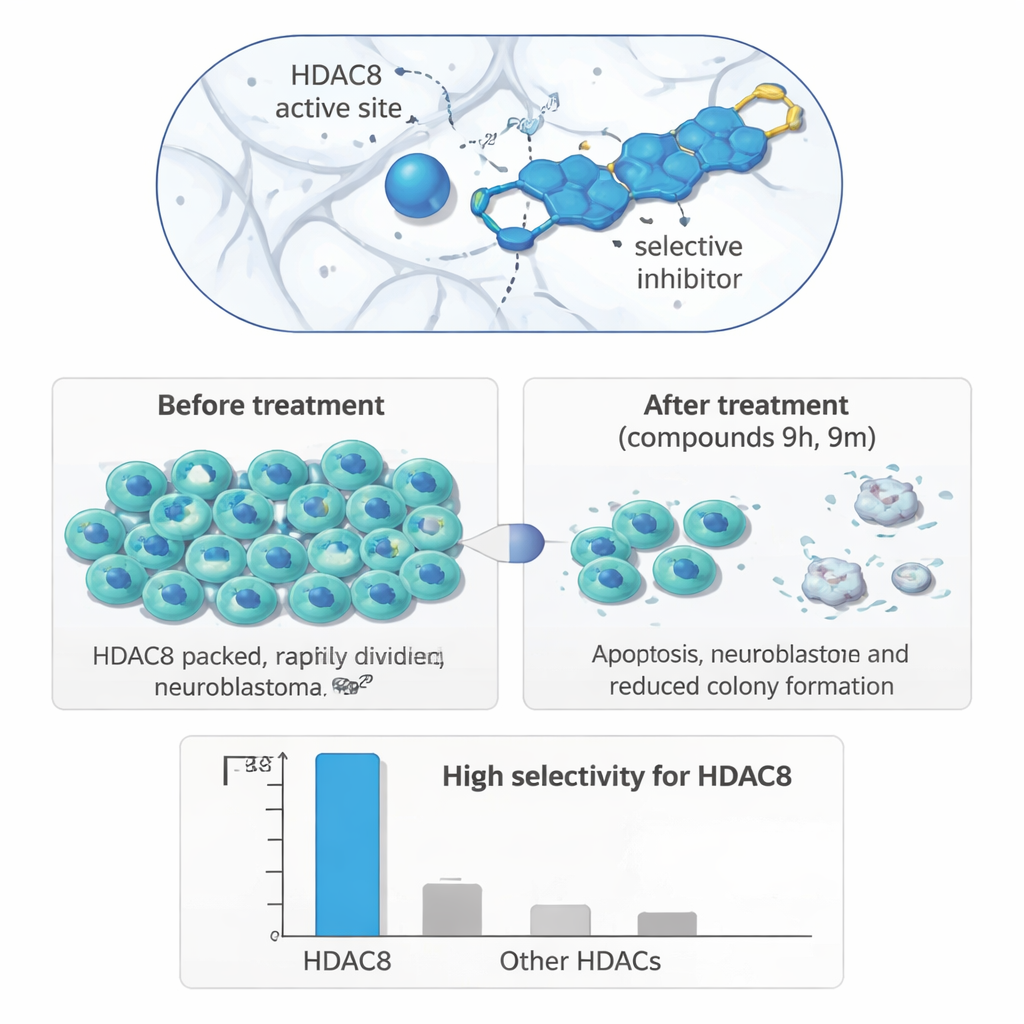
От пробирки к опухолевым клеткам
Чтобы проверить, переносится ли такая точная нацеленность на фермент в полезные биологические эффекты, исследователи опробовали свои соединения на панели человеческих клеточных линий. В клетках нейробластомы (IMR‑32) отчетливо выделялись две молекулы, 9h и 9m: они снижали рост клеток при микромолярных концентрациях и действовали сильнее в нейробластоме, чем в клетках рака молочной или толстой кишки или в незлокачественных почечных клетках. Долговременные эксперименты по формированию колоний показали, что обработанные нейробластомные клетки значительно утратили способность восстанавливаться после воздействия препарата. В тесте на заживление раны, который отслеживает, как быстро клетки мигрируют, чтобы закрыть царапину в слое клеток, оба соединения замедляли движение нейробластомных клеток, что указывает на снижение метастатического потенциала.
Как эти соединения убивают раковые клетки
Эксперименты с проточной цитометрией показали, что 9h и 9m вызывают программируемую гибель клеток (апоптоз) в нейробластомных клетках и приводят к накоплению клеток в фазе клеточного цикла, связанной с повреждением ДНК или гибелью (Sub‑G1). Чтобы подтвердить, что эти эффекты действительно обусловлены блокадой HDAC8, команда измеряла степень ацетилирования белка SMC3, известной мишени HDAC8, участвующей в сохранении сцепления сестринских хромосом во время деления клетки. При ингибировании HDAC8 ацетилированный SMC3 накапливается. После обработки 9h или 9m уровни ацетилированного SMC3 резко возросли, в то время как общий уровень белка SMC3 оставался без изменений — убедительное свидетельство того, что эти соединения непосредственно поражают HDAC8 в живых клетках и нарушают его нормальную функцию в контроле хромосом.
Что это может значить для будущего лечения
В совокупности химия, компьютерное моделирование, ферментные тесты и клеточные эксперименты рисуют согласованную картину: недавно разработанные триазолохинолиновые соединения являются мощными, высокоселективными блокирами HDAC8, способными ограничивать рост и распространение нейробластомных клеток, щадя при этом другие ферменты семейства HDAC. Поскольку они обходятся без обычной гидроксаматной группы, они могут предложить более безопасный путь для использования HDAC8 в качестве терапевтической мишени. Хотя предстоит еще много работы — особенно исследования на животных и клинические испытания в будущем — это исследование закладывает прочную основу для разработки более точных препаратов против детской нейробластомы и, возможно, других заболеваний, связанных с активностью HDAC8.
Цитирование: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
Ключевые слова: ингибиторы HDAC8, нейробластома, эпигенетическая терапия, триазолохинолин, таргетные противораковые препараты