Clear Sky Science · ru
Интерпретируемая модель машинного обучения, использующая рутинные клинические данные для прогнозирования раннего рецидива при гепатоцеллюлярной карциноме
Почему это важно для пациентов и их семей
Для людей, перенесших операцию по удалению рака печени, один из самых насущных вопросов — «Вернётся ли рак в ближайшее время?» Сегодня врачи могут дать лишь приблизительные оценки, часто основанные на широких стадийных системах, которые рассматривают многих разных пациентов как одинаковых. В этом исследовании предложен новый подход, использующий информацию, которую больницы уже собирают — рутинные анализы крови и данные сканирования — вместе с интерпретируемым искусственным интеллектом, чтобы дать каждому пациенту более ясную и персонализированную картину краткосрочного риска рецидива.
Распространённый рак с упорной частотой возврата
Гепатоцеллюлярная карцинома — самый частый тип первичного рака печени и одна из основных причин онкологических смертей в мире. Даже при полном удалении видимых опухолей более 70% пациентов сталкиваются с возвращением болезни в течение пяти лет. Ранний рецидив — примерно в течение двух лет после операции — вызывает особую тревогу, так как обычно свидетельствует об агрессивных клетках, уже распространившихся в пределах печени, и резко ухудшает прогноз выживаемости. Существующие клинические системы стадирования, такие как TNM или Barcelona Clinic Liver Cancer (BCLC), позволяют грубо разделить пациентов на широкие категории, но часто не в состоянии точно определить, кто действительно находится в высокой группе риска раннего рецидива.
Преобразование повседневных результатов тестов в шкалу риска
Исследователи использовали записи 1 120 пациентов, которым в двух крупных больницах Китая в 2014–2024 годах была выполнена, по виду, радикальная резекция печени. Они сосредоточились только на информации, доступной до операции: возраст и пол, признаки визуализации, такие как диаметр наибольшей опухоли и наличие множественных очагов, а также широкий набор стандартных лабораторных тестов, проведённых в дни перед операцией. Из этих данных отобрали девять ключевых предикторов, связанных с вероятностью рецидива. Вместо того чтобы полагаться на одну математическую формулу, авторы комбинировали три различные методы машинного обучения и усредняли их прогнозы в единый скор риска от 0 до 1. Пациентов затем разделили на группы низкого, умеренного и высокого риска на основе этого показателя. 
Превосходство над стандартными системами стадирования
Чтобы проверить эффективность модели, команда сначала оценила её на «отложенной» выборке пациентов из той же больницы, а затем на независимой группе из второй больницы. В обоих случаях новая модель явно превосходила традиционные системы стадирования в умении отличать тех, кто останется свободным от опухоли, от тех, у кого произойдёт рецидив в течение 24 месяцев. В внутренней тестовой группе показатель точности во времени, измеряемый стандартной метрикой «площадь под кривой», составлял около 0,76, по сравнению примерно с 0,55–0,64 для распространённых методов стадирования. Пациенты в группе высокого риска имели наихудшую безрецидивную выживаемость, в группе умеренного риска риск рецидива снижался примерно на 60%, а в группе низкого риска — примерно на 90% по сравнению с группой высокого риска. Эти выраженные различия сохранялись и в внешней больнице и оставались согласованными в большинстве подгрупп, таких как молодые и пожилые пациенты, мужчины и женщины, а также пациенты с большими или маленькими опухолями.
Открытие «чёрного ящика» искусственного интеллекта
Частая критика применения машинного обучения в медицине заключается в том, что оно ведёт себя как «чёрный ящик»: модель может хорошо предсказывать, но даже специалисты не всегда понимают, почему. Чтобы решить эту проблему, авторы применили метод SHapley Additive exPlanations (SHAP), который разлагает каждое предсказание на вклад отдельных входных факторов. Анализ показал, что размер опухоли был единственным самым сильным фактором, повышающим риск во всех трёх алгоритмах, за ним следовали такие признаки, как число опухолей и показатели крови, отражающие функцию печени и воспаление. Интересно, что уровень хлора в крови, как правило, смещал риск в противоположную сторону, выступая в этой базе данных как фактор, снижающий риск. Для отдельных пациентов модель может генерировать простые графики в виде полос, показывающие, например, как большой диаметр опухоли и неблагоприятные показатели крови повышают скор, тогда как лучшая функция печени снижает его. 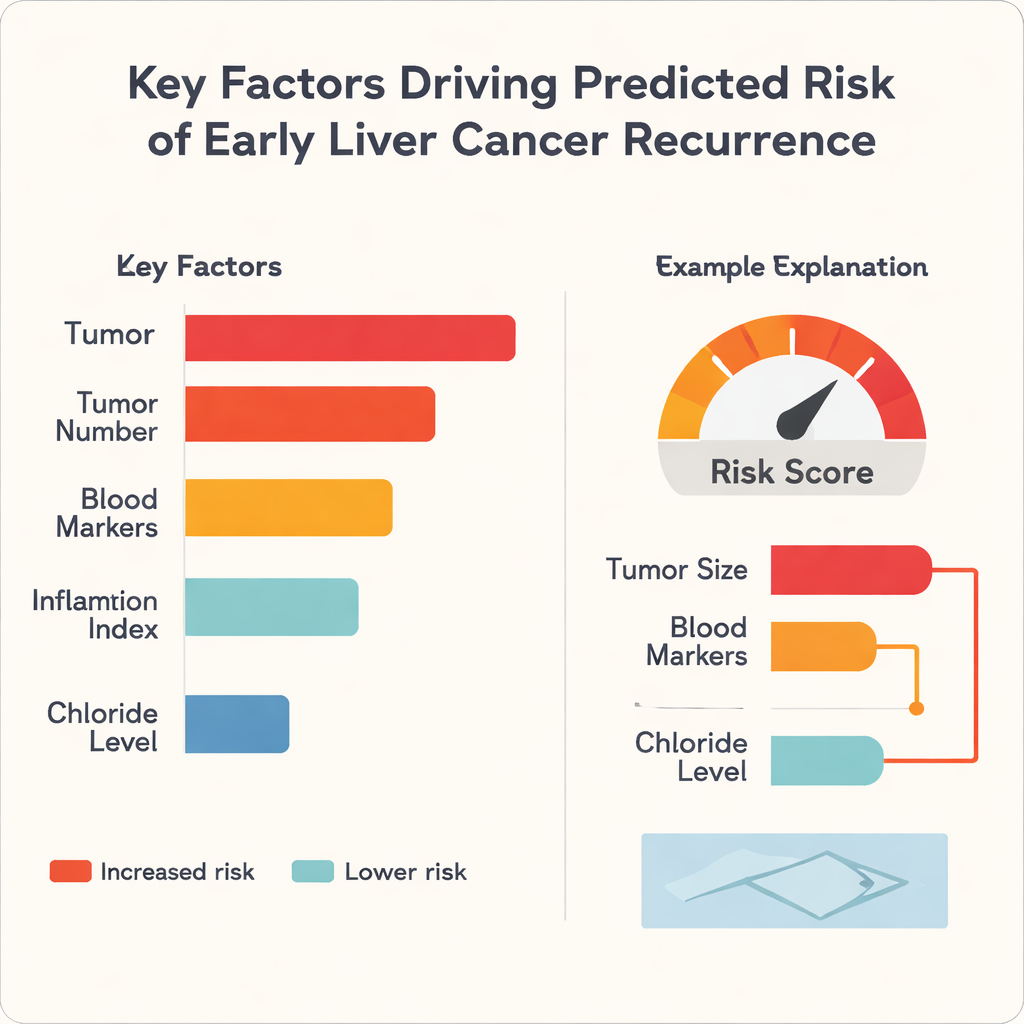
Что это может значить в клинической практике
Поскольку модель работает на данных, которые больницы уже собирают, и не требует специальных сканирований или дорогих генетических тестов, её можно внедрить в различных условиях оказания помощи, включая ресурсоограниченные. До операции врачи могли бы использовать её для выявления людей, нуждающихся в более интенсивном наблюдении или потенциально получающих дополнительные послеоперационные терапии, при этом освобождая действительно низкорисковых пациентов от ненужных обследований и тревоги. Авторы отмечают, что их исследование носит ретроспективный характер и основано на специфической популяции пациентов, поэтому требуются проспективные испытания в более разнообразных условиях. Тем не менее, их работа демонстрирует, как прозрачный, объяснимый ИИ может превращать привычные лабораторные показатели и результаты сканирования в значимые персонализированные прогнозы, поддерживающие совместное принятие решений между пациентами и их лечащими командами.
Цитирование: Guo, DF., Wen, Q., Zhang, X. et al. An interpretable machine learning model using routine clinical data for early recurrence prediction in hepatocellular carcinoma. Sci Rep 16, 7520 (2026). https://doi.org/10.1038/s41598-026-38484-w
Ключевые слова: рецидив рака печени, модель машинного обучения, клиническое прогнозирование риска, интерпретируемый ИИ, гепатоцеллюлярная карцинома