Clear Sky Science · ru
Двойной ингибитор G9a и антагонист гистаминового рецептора H3 A-366 улучшает повторяющееся и социальное поведение и ослабляет нейровоспаление у мышей BTBR T + tf/J
Почему это исследование на мышах важно для аутизма
Семьи, живущие с расстройством аутистического спектра (РАС), часто сталкиваются с набором лечебных подходов, которые облегчают лишь отдельные симптомы. В этом исследовании изучается новый экспериментальный препарат A-366, разработанный для одновременного воздействия на две разные биологические системы. В широко применяемой модельной линии мышей с аутипо́подобным поведением A-366 снижал повторяющиеся действия, улучшал социальное взаимодействие и уменьшал воспаление в мозге, что намекает на возможность создания одного лекарства, способного одновременно влиять на несколько ключевых признаков РАС.
Состояние с множеством взаимосвязанных факторов
РАС — это не единое заболевание с одной причиной. Оно включает трудности в социальной коммуникации, повторяющееся поведение и часто сопутствующие проблемы, такие как тревога или нарушения внимания. За внешними проявлениями скрывается сложный узел изменений в химии мозга и регуляции генов. Существующие препараты, например антипсихотик арипипразол, в основном воздействуют на нейромедиаторные системы, такие как дофамин и серотонин, и одобрены только для сопутствующих симптомов, например раздражительности. Одновременно исследования показали, что упаковка ДНК и её химические метки внутри нейронов — эпигенетика — также изменяются при РАС, как и активность иммунных и воспалительных ответов мозга. Эти множественные уровни указывают, что подход «по одной мишени за раз» может быть слишком узким.
Воздействие и на «переключатели генов», и на нейромедиаторы
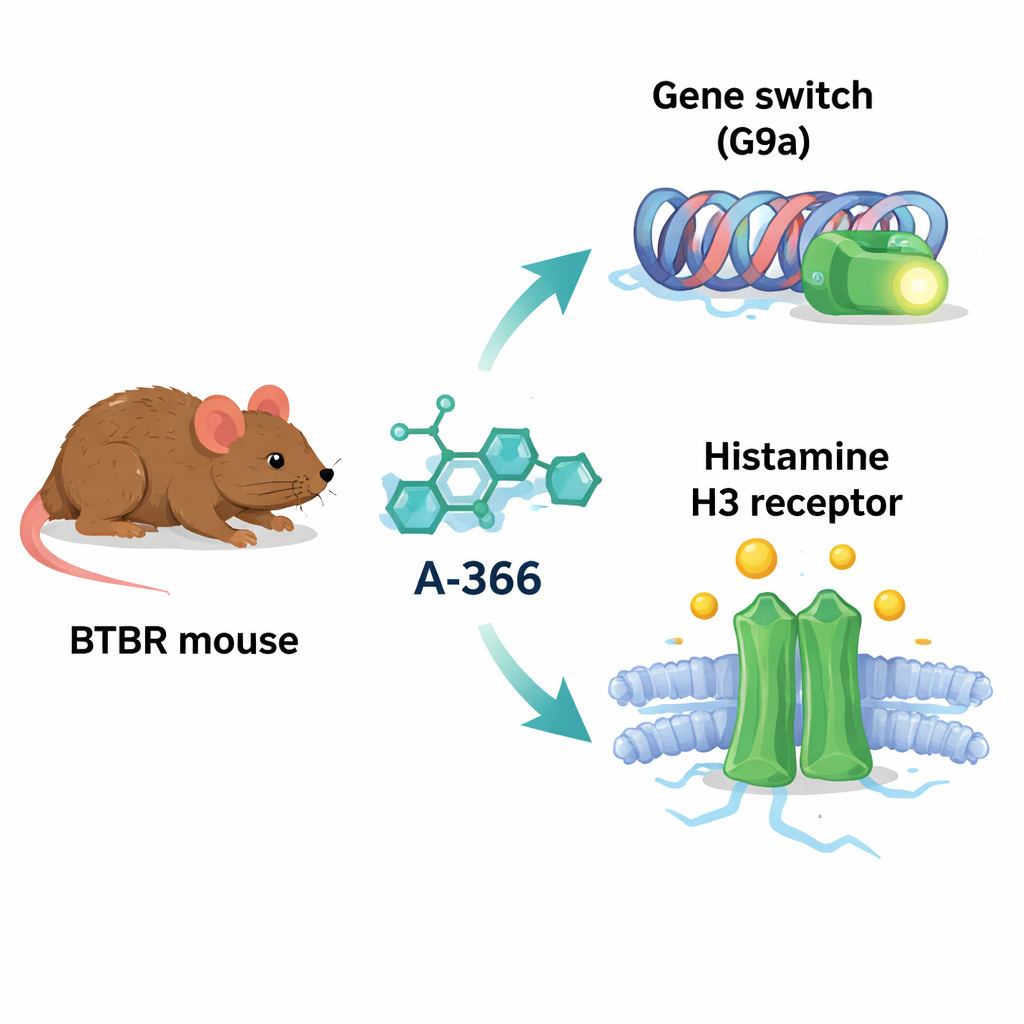
A-366 изначально разрабатывали как блокатор белка G9a — фермента, который добавляет химические метки на гистоны и, как правило, подавляет активность генов. При ряде заболеваний мозга активность G9a и отмечаемые им метки повышены, что может приводить к выключению генов, важных для обучения, памяти и нормального развития нейронных связей. Любопытно, что молекулярная форма A-366 также напоминает структуру веществ, блокирующих гистаминовый рецептор H3 — «переключатель», контролирующий высвобождение гистамина и других нейромедиаторов и связанный с вниманием, бодрствованием и социальным поведением. Из-за этого сходства авторы предположили, что A-366 может выступать как «двойной агент»: ослаблять вредное эпигенетическое подавление через ингибирование G9a и одновременно усиливать гистаминовую сигнализацию блокадой H3-рецепторов.
Испытание A-366 на мышах с аутипоподобным поведением
Исследователи работали с мышами линии BTBR T+tf/J, у которых природно наблюдаются низкая социальность, выраженное повторяющееся вылизывание и копание, а также повышенное воспаление в мозге — признаки, созвучные ключевым чертам РАС. Самцы BTBR получали ежедневные инъекции A-366 в течение трёх недель в трёх разных дозах; их поведение сравнивали с типичными мышами C57 и с BTBR, леченными либо питолизантом (стандартный блокатор H3), либо арипипразолом. В ряде тестов A-366 в дозозависимом режиме снижал повторяющееся копание, разрывание материалов и вылизывание, а также улучшал показатели в Y-лабиринте, тесте на пространственную рабочую память. В трёхкамерном социальном тесте A-366 не только восстановил предпочтение мышей проводить время с другой мышью по сравнению с пустой клеткой, но и при максимальной дозе довёл социальные показатели до уровня типичных мышей, превзойдя эффект питолизанта и арипипразола.
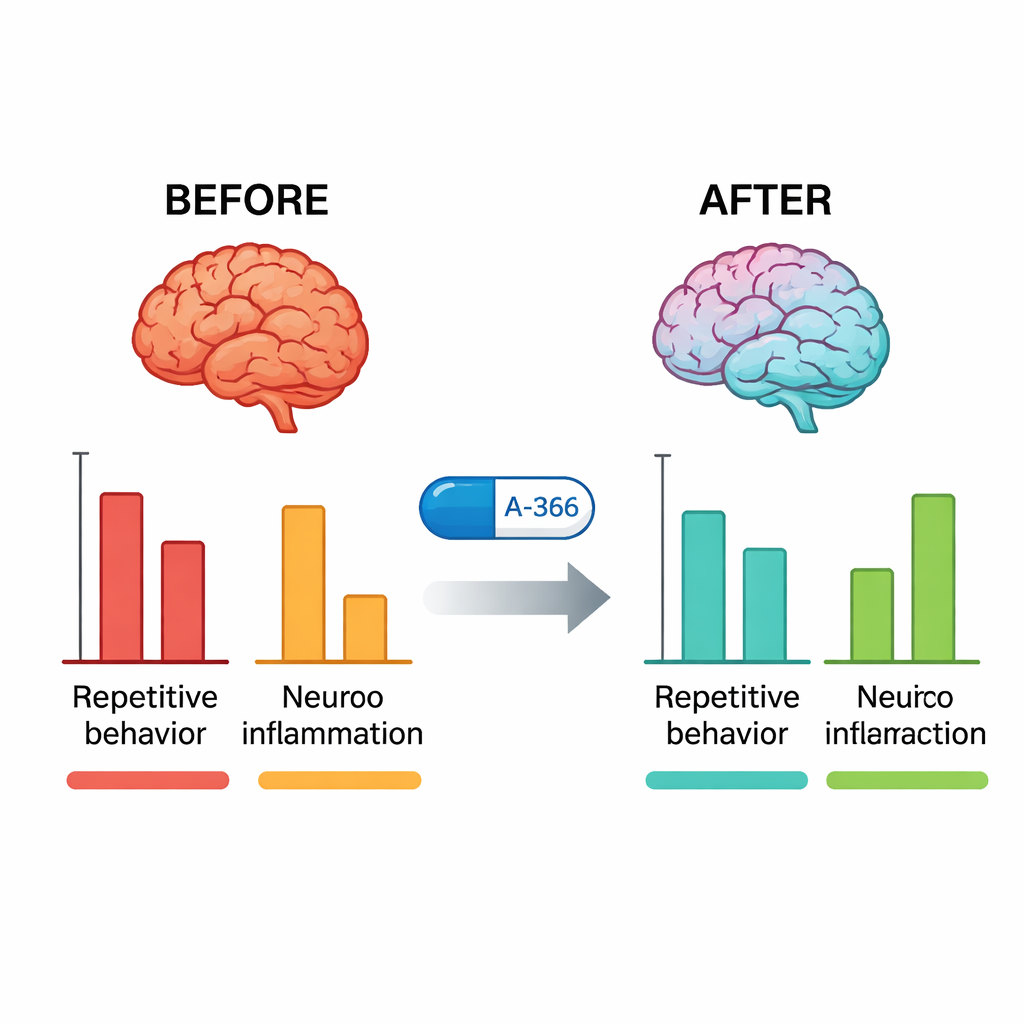
Угомонение воспаления и подтверждение мишеней
После поведенческих тестов исследователи изучили мозг мышей. У нелеченных BTBR активность G9a в гиппокампе и мозжечке была заметно выше, чем у типичных мышей. Лечение A-366 резко снизило эту активность в сторону нормы, тогда как питолизант сам по себе этого не сделал, что подтверждает взаимодействие A-366 с его эпигенетической мишенью. Одновременно ключевые провоспалительные молекулы — TNF-α, IL-6 и IL-1β — были значительно повышены у BTBR и заметно снижались под воздействием A-366, в большей степени, чем при арипипразоле. Когда учёные добавили к A-366 препарат, активирующий H3-рецепторы (RAMH), поведенческие и противовоспалительные эффекты лишь частично обращались назад, а снижение активности G9a сохранялось. Эта картина поддерживает комбинированный механизм: стабильное эпигенетическое ослабление через ингибирование G9a в сочетании с гистамин-опосредованным вкладом через блокаду H3-рецептора.
Что это может означать для будущих лечений
Для неспециалиста эти результаты свидетельствуют о том, что возможно проектировать препараты, воздействующие одновременно и на «программное обеспечение», и на «систему сообщений» мозга. В этой мышиной модели аутипоподобного поведения A-366 ослаблял повторяющиеся действия, улучшал социальную вовлечённость и снижал признаки хронического воспаления в мозге, одновременно ослабляя вредное генное выключение и регулируя гистаминовую сигнализацию. Сам A-366 был создан для других заболеваний и потребует оптимизации и обширной проверки безопасности перед применением у людей. Тем не менее он служит ориентиром для нового класса многомишенных препаратов, направленных на сложную биологию РАС, где поочередная работа с одной путём за раз до сих пор давала ограниченный эффект.
Цитирование: Hajar, M., Jayaprakash, P., Stark, H. et al. The dual G9a inhibitor and histamine H3 receptor antagonist A-366 improves repetitive and social behaviors and attenuates neuroinflammation in BTBR T + tf/J mice. Sci Rep 16, 7105 (2026). https://doi.org/10.1038/s41598-026-38481-z
Ключевые слова: расстройство спектра аутизма, эпигенетическая терапия, гистаминовый рецептор H3, нейровоспаление, модель на мышах