Clear Sky Science · ru
aFGF спасает фибробласты, подвергшиеся старению под действием высокого уровня глюкозы, и улучшает заживление диабетических ран, регулируя путь SIRT1/STAT3
Почему медленно заживающие раны имеют значение
Для многих людей с диабетом даже небольшая царапина на стопе или ноге может перерасти в упрямую рану, которая тлеет месяцами, иногда приводя к инфекции или даже ампутации. Эти хронические язвы — не просто поверхностная проблема: клетки кожи, которые должны восстанавливать поврежденную ткань, часто стареют преждевременно и перестают работать должным образом. В этом исследовании изучают перспективный способ «омоложения» части таких клеток с помощью природного сигнала восстановления, чтобы помочь диабетическим ранам закрываться быстрее и более полно.
Клетки, стареющие слишком рано
Здоровая кожа зависит от фибробластов — опорных клеток, живущих в глубоких слоях кожи, — которые должны размножаться, мигрировать в рану и откладывать новый каркас для ткани. При диабете длительно высокий уровень сахара и продукты гликирования толкают эти фибробласты в состояние, называемое клеточным старением или сенесценцией. Сенесцентные фибробласты уже не делятся эффективно, производят меньше структурных белков, необходимых для ремонта, и вместо этого выделяют набор факторов, усиливающих воспаление. Авторы показывают, что у диабетических крыс кожа вокруг раны содержит больше таких стареющих фибробластов и меньше полезных матричных белков, что коррелирует с заметно замедленным заживлением.
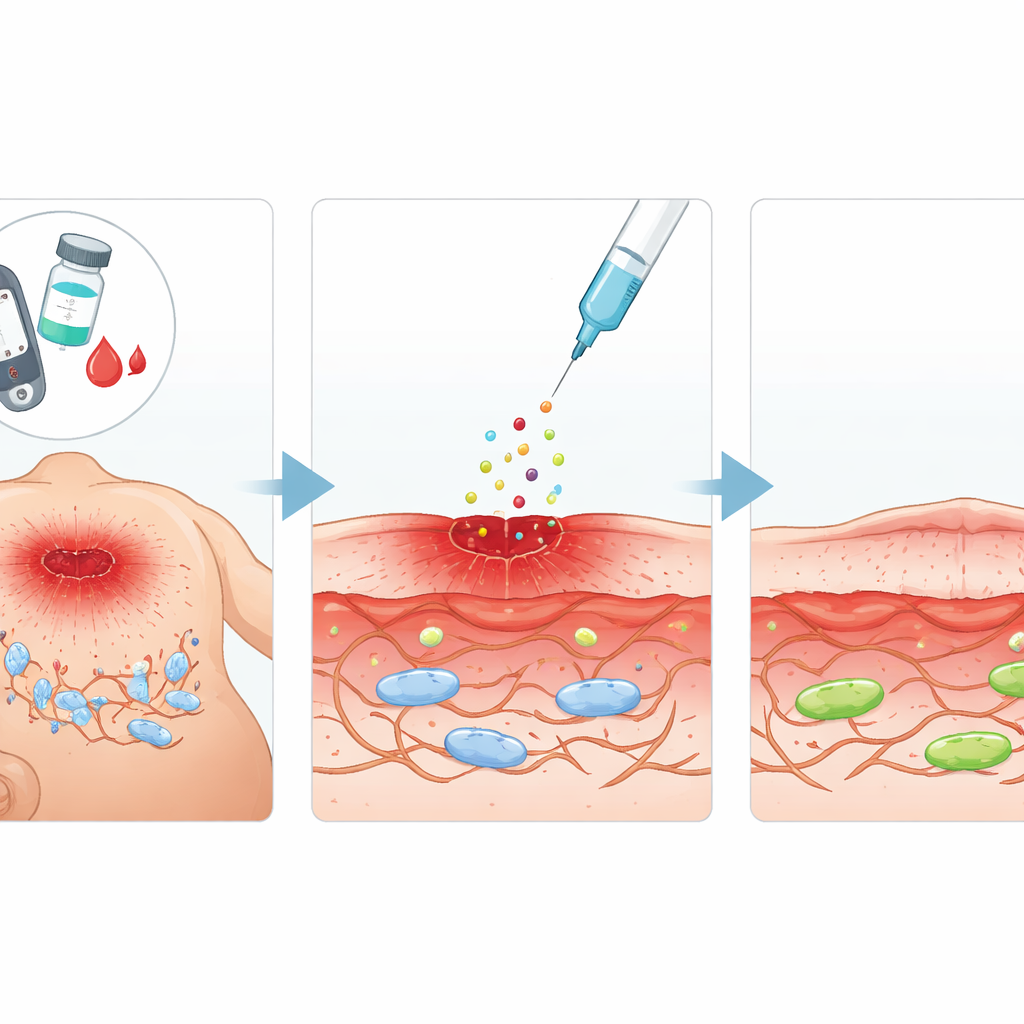
Сигнал восстановления с потенциалом
Исследователи сосредоточились на кислой фибробластной факторе роста (aFGF) — природном белке, известном способностью стимулировать рост клеток и регенерацию тканей. Они задались вопросом, сможет ли aFGF не только повысить активность фибробластов, но и обратить изменения, похожие на старение, вызванные высоким уровнем сахара. У диабетических крыс учёные создали стандартизированные кожные раны и вводили aFGF вокруг поврежденной области каждые несколько дней. По сравнению с нелечеными диабетическими животными, крысы, получавшие aFGF, демонстрировали более быстрое сокращение поверхности раны, лучшее восстановление подлежащей ткани и более низкие уровни маркёров клеточного старения. В параллельных лабораторных экспериментах на клеточной линии мышиных фибробластов, подвергнутых очень высокому уровню глюкозы, aFGF восстанавливала способность клеток к делению и миграции — два поведения, необходимые для закрытия раны.
Успокоение оксидативного стресса внутри клеток
Высокий уровень сахара делает не только избыток топлива для клеток: он также стимулирует чрезмерное образование реактивных кислородных видов — нестабильных молекул, которые повреждают белки, липиды и ДНК. Этот оксидативный стресс является важным триггером перехода фибробластов в состояние сенесценции. Исследователи измеряли несколько стандартных индикаторов этого стресса в своей клеточной модели, включая продукты повреждения и активность собственных антиоксидантных ферментов клетки. При высоком уровне глюкозы фибробласты демонстрировали больше повреждений и ослабленные антиоксидантные защиты. После добавления aFGF баланс сместился: вредные маркеры снизились, а активность защитных ферментов возросла. Это говорит о том, что aFGF способствует восстановлению более здоровой внутренней среды, снижая вероятность того, что фибробласты перейдут в необратимо старое состояние.
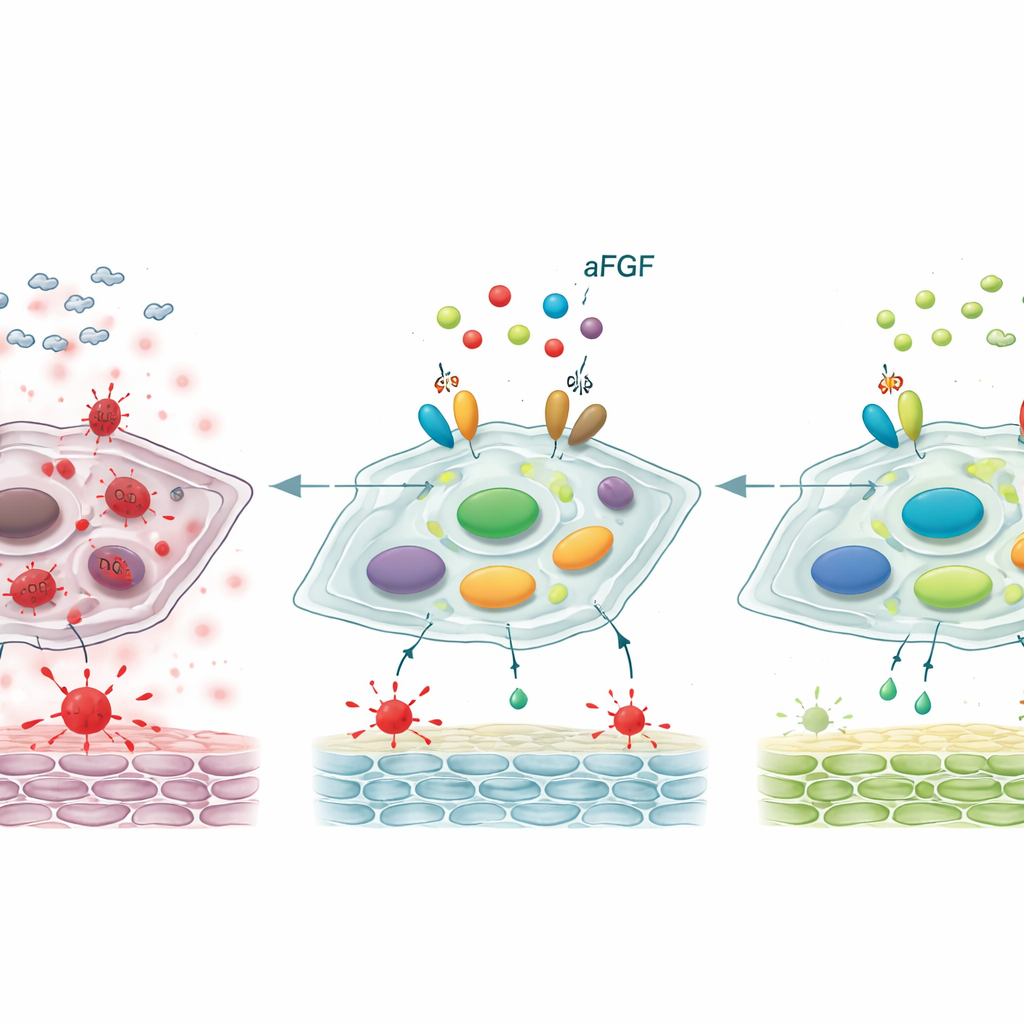
Перенастройка ключевого контрольного переключателя
Углубляясь, учёные изучили молекулярную ось контроля, включающую два белка — SIRT1 и STAT3 — которые совместно влияют на то, останутся ли фибробласты юными или станут сенесцентными. В диабетических ранах и в клетках, обработанных высоким уровнем глюкозы, уровни SIRT1, белка-стража, связанного с устойчивостью к стрессу, были снижены, тогда как активированная форма STAT3 — драйвер старения и провоспалительного поведения — была повышена. Лечение aFGF изменяло этот паттерн: SIRT1 повышался, а активированная STAT3 снижалась. Когда команда блокировала SIRT1 с помощью специфического ингибитора, aFGF в значительной степени терял способность уменьшать оксидативный стресс, подавлять маркёры старения и ускорять заживление ран у крыс. Это указывает на то, что благоприятные эффекты aFGF в значительной степени зависят от пробуждения SIRT1, который, в свою очередь, сдерживает STAT3 и вредную программу старения, которую он контролирует.
Что это может значить для пациентов
В совокупности результаты показывают, что aFGF делает не просто толчок к росту клеток. Похоже, он спасает перегруженные фибробласты в диабетических ранах от разрушительного цикла старения, снижая оксидативный стресс и перенастраивая ключевой молекулярный переключатель, чтобы эти клетки снова могли помогать в восстановлении ткани. Хотя работа проводилась на крысах и в культурах клеток, а реальные диабетические раны ещё сложнее, чем использованные модели, данные указывают на aFGF как на перспективного кандидата для будущих терапий. Если аналогичные преимущества подтвердятся у людей, целенаправленная терапия aFGF однажды может помочь хроническим диабетическим язвам заживать быстрее, снижая боль, риск инфекции и вероятность серьёзных осложнений.
Цитирование: Wang, X., Lu, M., Jia, S. et al. aFGF rescues high glucose-induced senescent fibroblasts and improves diabetic wound healing by regulating SIRT1/STAT3 pathway. Sci Rep 16, 7856 (2026). https://doi.org/10.1038/s41598-026-38480-0
Ключевые слова: заживление диабетических ран, старение фибробластов, окислительный стресс, терапия факторами роста, путь SIRT1 STAT3