Clear Sky Science · ru
In silico-открытие многоцелевого ингибитора на основе природного соединения для терапии болезни Хантингтона
Новый взгляд на разрушительное заболевание мозга
Болезнь Хантингтона — редкое, но разрушительное расстройство мозга, которое постепенно лишает людей двигательных навыков, мышления и независимости. Современные лекарства могут смягчить некоторые симптомы, но они не останавливают и не обращают процесс болезни. В этом исследовании изучается новый, управляемый компьютером подход к поиску лечения: поиск одного природного соединения, которое одновременно воздействовало бы на несколько уязвимых звеньев патологии — подход, который может быть эффективнее, чем препараты, направленные на одну цель.
Почему болезнь Хантингтона так трудно лечить
Болезнь Хантингтона вызвана дефектным геном, который приводит к постепенному разрушению нервных клеток, обычно начинаясь в среднем возрасте. На ранних стадиях люди могут заметить неявные изменения настроения, мелкие непроизвольные движения или лёгкие трудности с планированием и концентрацией. В течение 10–12 лет это может прогрессировать до тяжёлых двигательных нарушений, утраты речи, деменции и полной зависимости от опекунов. Учёные знают, что в клетках мозга при Хантингтоне нарушается множество процессов: падает выработка энергии, вредные белки скапливаются в агрегаты, а химические сигналы между клетками становятся токсичными. Поскольку одновременно нарушены многие пути, стратегия «один белок — один препарат» испытывает трудности с достижением реальных прорывов.
Три критические точки давления в мозге
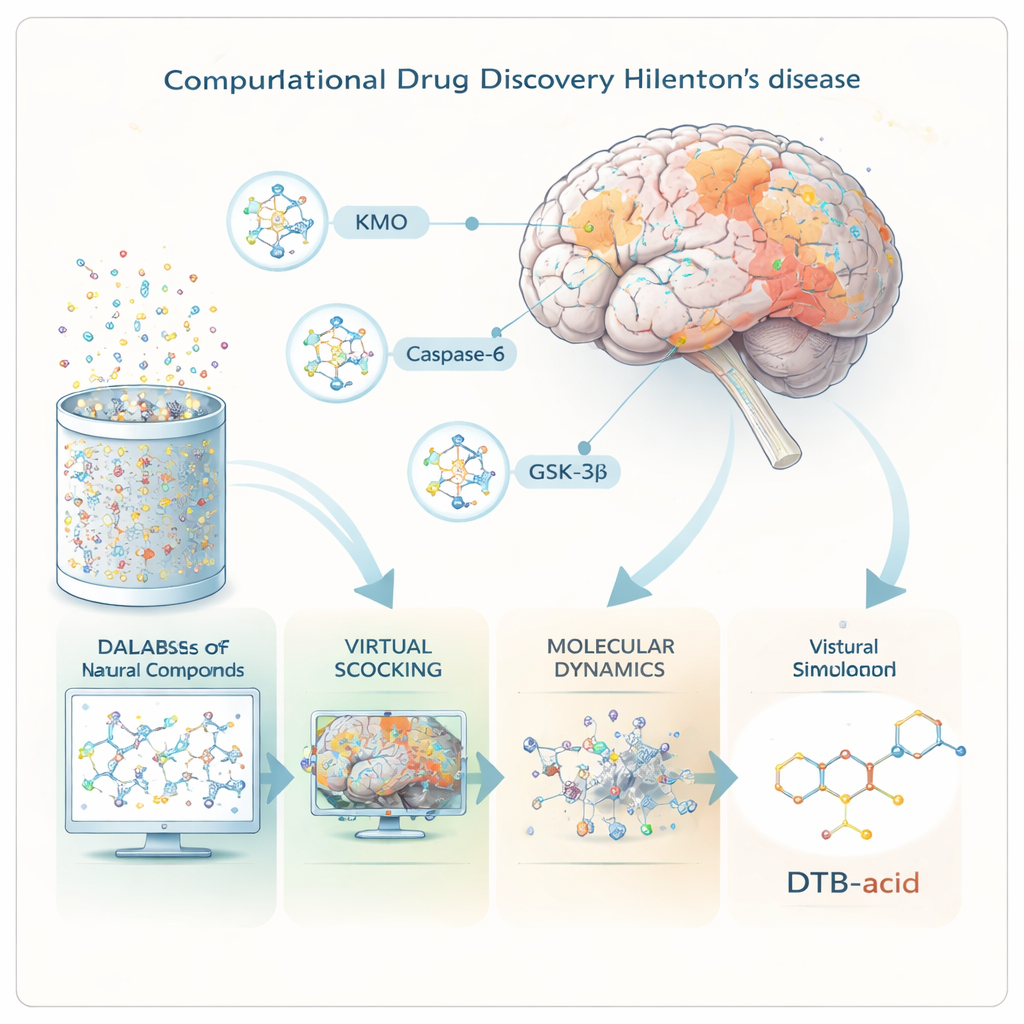
Исследователи сосредоточились на трёх белках, которые занимают ключевые регуляторные позиции при болезни Хантингтона. Первый, KMO, направляет распад аминокислоты триптофана либо в токсичные, либо в защитные метаболиты; когда баланс смещается в сторону токсинов, клетки мозга страдают. Второй, Caspase-6, режет мутантный белок huntingtin на более мелкие, сильно токсичные фрагменты, которые накапливаются на ранних стадиях болезни. Третий, GSK-3β, — сигнальная киназа, связанная с аномальными белковыми клубками и гибелью клеток при нескольких заболеваний мозга. Найдя одну молекулу, способную ослабить вредную активность всех трёх белков одновременно, команда надеялась разработать терапию, лучше соответствующую сложности болезни.
Скрининг природной библиотеки на суперкомпьютерах
Вместо того чтобы смешивать вещества в пробирках, учёные работали полностью «in silico», используя продвинутое программное обеспечение для моделирования поведения молекул. Они начали с более чем 695 000 природных соединений из публичной базы данных, подготавливая каждое в трёхмерном виде. Мощные инструменты виртуального скрининга затем предсказали, какие соединения, вероятно, смогут проникнуть через гематоэнцефалический барьер, вести себя как реальные лекарства в организме и избегать серьёзных проблем с безопасностью. Примерно 60 000 прошли эти фильтры и были протестированы, уже на компьютере, на предмет того, насколько плотно они могут встать в сайты связывания трёх целевых белков.
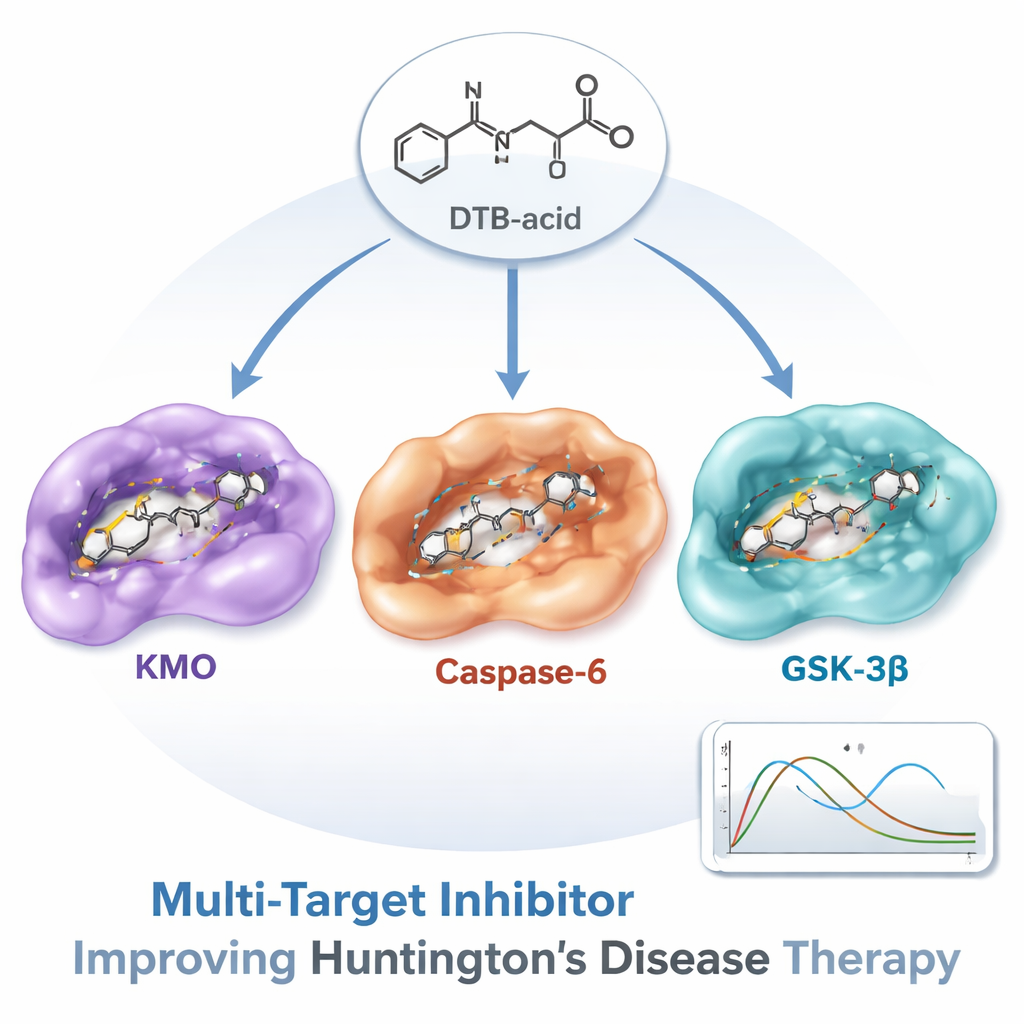
Одна выдающаяся молекула: DTB-кислота
Из этого огромного поиска одна молекула — названная DTB-кислота, природный алкалоид, родственный матриничной кислоте — вышла в лидеры. Подробные докинг-исследования показали, что DTB-кислота может образовывать сильные, точные контакты во всех трёх белках. Затем команда провела длительные молекулярно-динамические симуляции, которые имитируют движение атомов в воде со временем, чтобы проверить, удержится ли соединение на месте, а не уйдёт прочь. В течение 100 миллиардных долей секунды смоделированного движения комплексы белок–лигант оставались стабильными. Дополнительные расчёты энергии показали, что связывание с KMO особенно сильно, а отдельный анализ молекул воды в сайтах связывания указал, что взаимодействия с GSK-3β также термодинамически благоприятны.
От компьютерного «хита» к потенциальному лекарству
Разумеется, молекула, многообещающая на экране, — это только первый шаг. Авторы подчёркивают, что DTB-кислота всё ещё должна быть проверена в клеточных и животных моделях, чтобы подтвердить, что она достигает мозга, бьёт по намеченным целям и действительно защищает нейроны без вредных побочных эффектов. Тем не менее эта работа демонстрирует мощный и эффективный путь к открытию многоцелевых препаратов для сложных заболеваний мозга. Для неспециалистов главный посыл таков: вместо лечения болезни Хантингтона серией отдельных, узконаправленных препаратов может оказаться возможным спроектировать одну тщательно подобранную молекулу, подобную DTB-кислоте, которая одновременно борется с несколькими факторами повреждения — давая новую надежду на замедление или изменение течения этого неумолимого расстройства.
Цитирование: Zheng, B., Banday, M., Gangwar, S. et al. In silico discovery of natural compound-derived multi-target inhibitor for Huntington’s disease therapy. Sci Rep 16, 7716 (2026). https://doi.org/10.1038/s41598-026-38430-w
Ключевые слова: болезнь Хантингтона, многоцелевой препарат, вычислительное открытие лекарств, природные соединения, нейродегенерация