Clear Sky Science · ru
Интегрированный многонаборный скрининг для прогнозирования исхода и выявления генов-мишеней иммунотерапии у пациентов с гепатоцеллюлярной карциномой
Почему это важно для людей с раком печени
Гепатоцеллюлярная карцинома, самая распространённая форма первичного рака печени, уносит сотни тысяч жизней каждый год. У многих пациентов с одинаковой стадией заболевания ответ на лечение сильно различается, особенно в случае современных иммунотерапий, которые пытаются мобилизовать собственную иммунную систему организма. В этом исследовании поставлен простой, но ключевой вопрос: можно ли «прочитать» активность генов опухоли как отпечаток пальца, чтобы предсказать, у кого прогноз будет неблагоприятным, кто ответит на иммунно-ориентированные препараты и какие гены могут стать лучшими новыми мишенями для лечения?
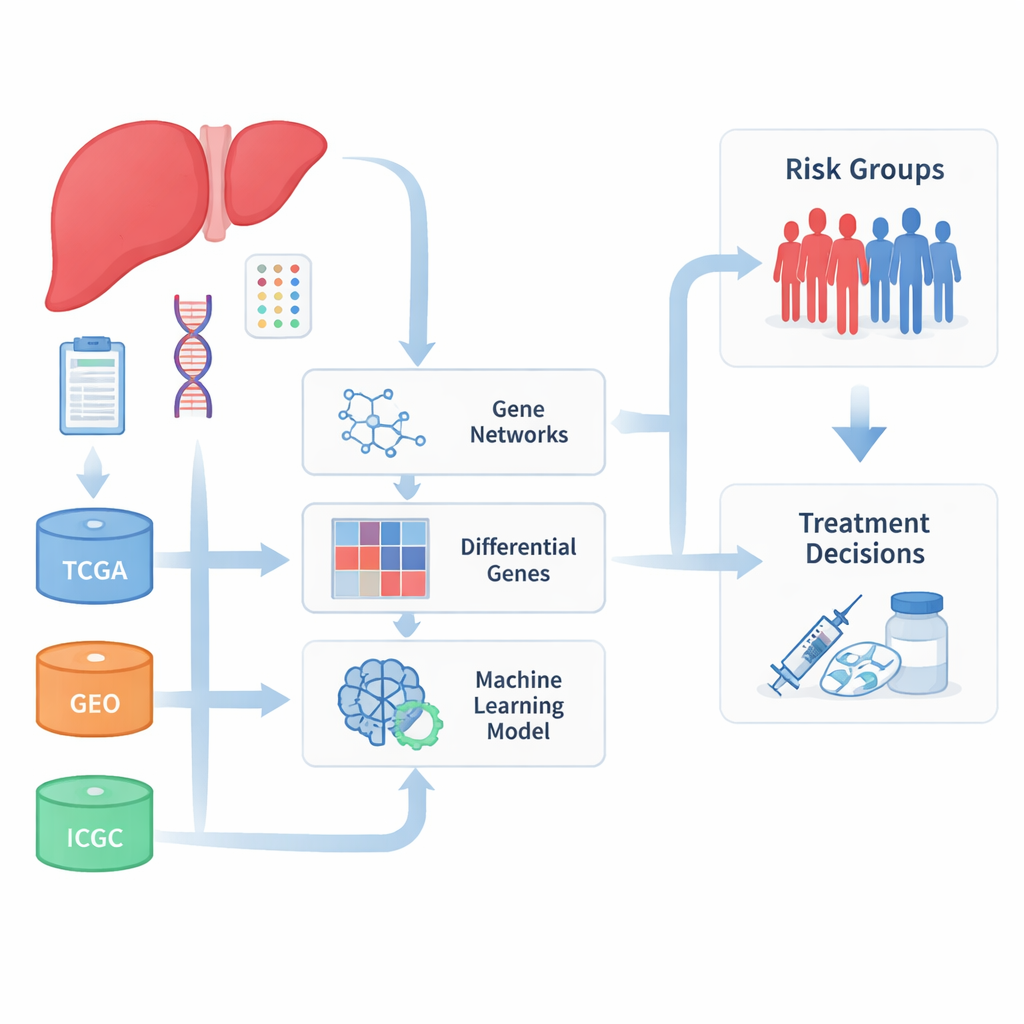
Объединение множества наборов данных
Исследователи начали с объединения больших коллекций образцов рака печени из нескольких международных баз данных, где хранятся данные об активности генов опухолей и клинические исходы. Комбинируя данные из The Cancer Genome Atlas, International Cancer Genome Consortium и ряда исследований Gene Expression Omnibus, они сформировали гораздо большую и более разнородную когорту пациентов, чем могла бы дать любая отдельная больница или проект. Поскольку эти наборы данных были получены в разных лабораториях и разными методами, команда вначале приложила существенные усилия для коррекции технических различий, чтобы результаты отражали биологические сигналы, а не лабораторный шум.
Поиск генетических паттернов, связанных с исходом
С очищенными данными в распоряжении команда искала группы генов, которые склонны включаться и выключаться совместно и которые коррелируют с клиническим исходом пациентов. Используя сетевой подход, они сгруппировали тысячи генов в модули и затем сосредоточились на тех модулях, которые наиболее тесно связаны с поведением опухоли и выживаемостью пациентов. Также сравнивали опухолевую и неопухолевую ткань, чтобы выявить гены, чья активность явно повышена или снижена при раке. Пересечение этих двух подходов дало набор из 93 генов, которые были изменены при раке печени и тесно связаны с ключевыми чертами заболевания, многие из них — вовлечены в метаболизм лекарств и детоксикацию.
Создание риск-скоринга на основе десяти генов
Чтобы превратить эти списки генов во что-то, что врачи могли бы в будущем использовать, авторы обратились к машинному обучению. Они протестировали более ста комбинаций алгоритмов выбора признаков и прогнозирования выживаемости, оценивая их по тому, насколько точно они разделяли пациентов на группы с более благоприятным и более неблагоприятным исходом в нескольких независимых когортах. В результате большого поиска им удалось выделить компактную сигнатуру из десяти генов, которые в сумме образовали риск-скор. Пациенты с высокими баллами последовательно демонстрировали меньшую общую, безрецидивную и безпрогрессную выживаемость как в основных наборах данных, так и в валидационных группах. Среди этих генов TYMS выделялся как сильный маркер плохого прогноза, тогда как APOL3 и FBXO2 были связаны с более благоприятными исходами.
Подсказки из иммунного окружения опухоли
Исследование вышло за рамки простого прогнозирования и попыталось понять, почему эти гены важны. С помощью нескольких вычислительных инструментов команда оценивала, какие типы иммунных клеток присутствуют в каждой опухоли и как сильно десятигенный скор коррелировал с этим иммунным ландшафтом. Опухоли высокого риска обычно демонстрировали иммунные паттерны и генетические изменения, связанные с большим количеством мутаций и признаками иммунного уклонения, включая связи с известными контрольными молекулами, такими как PD-1 и CTLA-4. Также были проанализированы профили мутаций: в опухолях высокого риска чаще встречались изменения в классических драйверах рака, например TP53. Наконец, анализ крови пациентов и здоровых добровольцев подтвердил, что TYMS повышен, а FBXO2 снижен у людей с раком печени, что поддерживает идею о биологической активности этих генов при заболевании, а не об их статистическом происхождении.
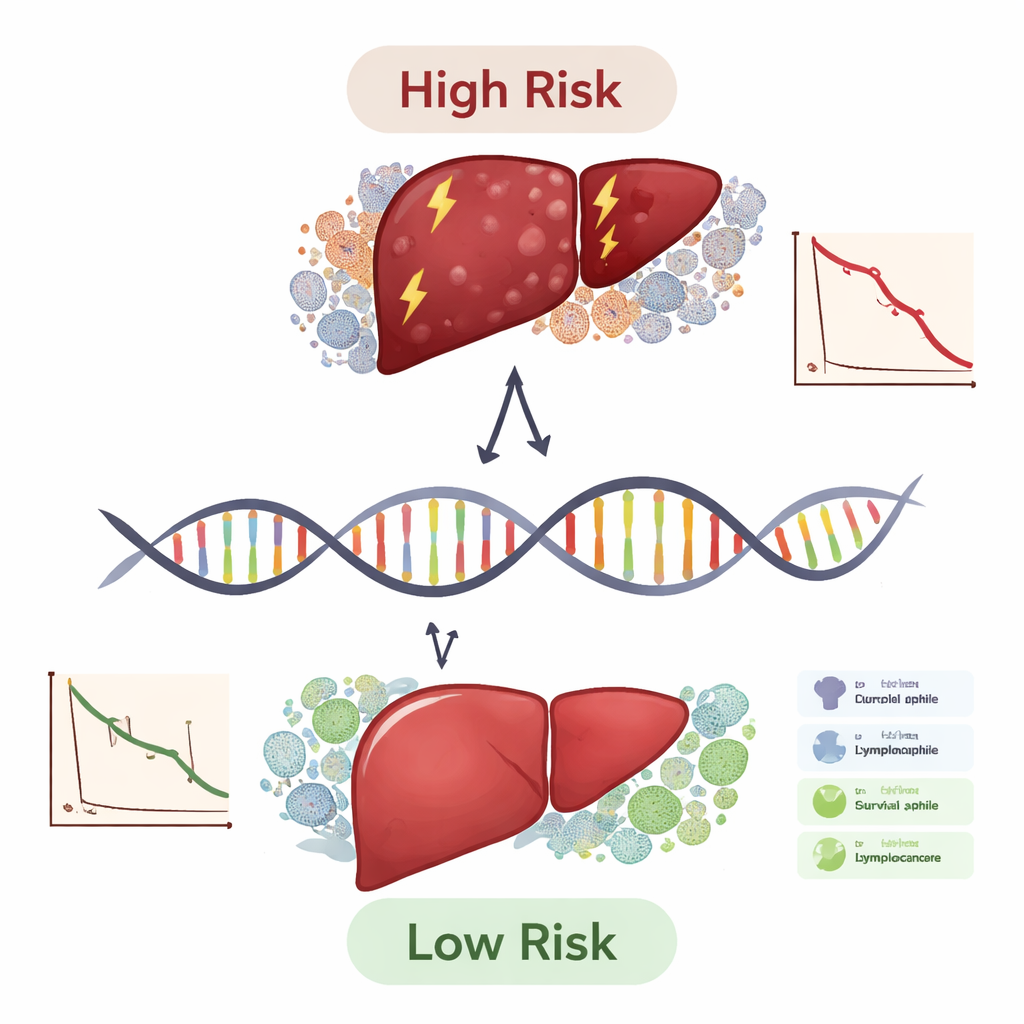
Что это значит для пациентов и врачей
В практическом смысле эта работа предлагает план использования небольшой панели генов для разделения пациентов с раком печени на группы риска и для определения тех, кто может получить наибольшую пользу от иммунотерапии. Десятигенный скор ещё не готов для клиники, но он показал себя лучше, чем одни лишь стандартные системы стадирования, и оставался информативным в различных подгруппах пациентов. Подобно тому, как панели холестерина направляют профилактику сердечных заболеваний, генетическая панель такого рода могла бы однажды помочь онкологам выбирать более агрессивную терапию для пациентов высокого риска, избавлять пациентов с низким риском от ненужных побочных эффектов и указывать разработчикам лекарств на новые мишени, такие как TYMS, APOL3 и FBXO2. Потребуются более крупные проспективные исследования и лабораторные эксперименты, но этот интегрированный анализ стал значительным шагом к более персонализированному, биологически обоснованному лечению рака печени.
Цитирование: Zhou, L., Zhang, W., Liu, Z. et al. Integrated multi-dataset screening to predict prognosis and identify immunotherapy gene targets in hepatocellular carcinoma patients. Sci Rep 16, 7014 (2026). https://doi.org/10.1038/s41598-026-38424-8
Ключевые слова: гепатоцеллюлярная карцинома, генный сигнатур, иммунотерапия, прогноз, опухолевая микроокружение