Clear Sky Science · ru
Сигнальный путь CNOT2 / c-Myc / STAT3 критически вовлечён в гликолиз-опосредованную апоптозу, вызванную бензил-изотиоцианатом, при гепатоцеллюлярной карциноме
Противораковый ингредиент на вашей тарелке
Бензил-изотиоцианат, или BITC, — это природное соединение, встречающееся в таких привычных овощах, как брокколи, капуста и капуста кейл. Врачи давно заметили, что люди, которые чаще едят эти продукты, в среднем реже болеют раком, но точные механизмы, с помощью которых отдельные растительные компоненты замедляют или убивают раковые клетки, всё ещё изучаются. Это исследование рассматривает действие BITC на клетки рака печени в лаборатории и обнаруживает неожиданный механизм, связывающий способ, которым раковые клетки утилизируют сахар, с активацией их самоубийства — апоптоза.
Почему раку печени нужны лучшие варианты лечения
Рак печени — один из самых смертельных видов рака в мире, а гепатоцеллюлярная карцинома является его самой распространённой формой. Даже при наличии хирургии, химиотерапии и таргетных препаратов многие опухоли рецидивируют или перестают отвечать на лечение. Одна из причин — перенастройка энергетического обмена в раковых клетках: вместо опоры в основном на митохондрии и кислород они интенсивно сжигают сахар в процессе, часто называемом «эффектом Варбурга». Такое искажённое использование глюкозы помогает опухолевым клеткам быстрее расти и сопротивляться гибели. Поиск безопасных способов вмешательства в эту энергетическую подпитку, в том числе с помощью молекул, получаемых из пищи, выглядит привлекательной стратегией.
Испытание растительного соединения на клетках рака печени
Исследователи обработали две линии человеческих клеток рака печени, SK-Hep1 и Huh7, возрастающими дозами BITC. По мере увеличения дозы выживаемость клеток снижалась, что показало токсичность BITC для клеток рака печени в этих условиях. При внимательном изучении внутриклеточных процессов были обнаружены классические признаки программируемой клеточной смерти, или апоптоза. Ключевые белки, которые в норме существуют в «неактивной» форме до расщепления при апоптозе, такие как PARP и каспаза-3, уменьшились в своих интактных, «про‑» формах. Анализ методом проточной цитометрии также показал увеличение доли клеток в суб-G1 фрагменте клеточного цикла и рост числа клеток, положительных по Annexin V, оба признака того, что раковые клетки активно проходят апоптоз, а не просто получили повреждение.
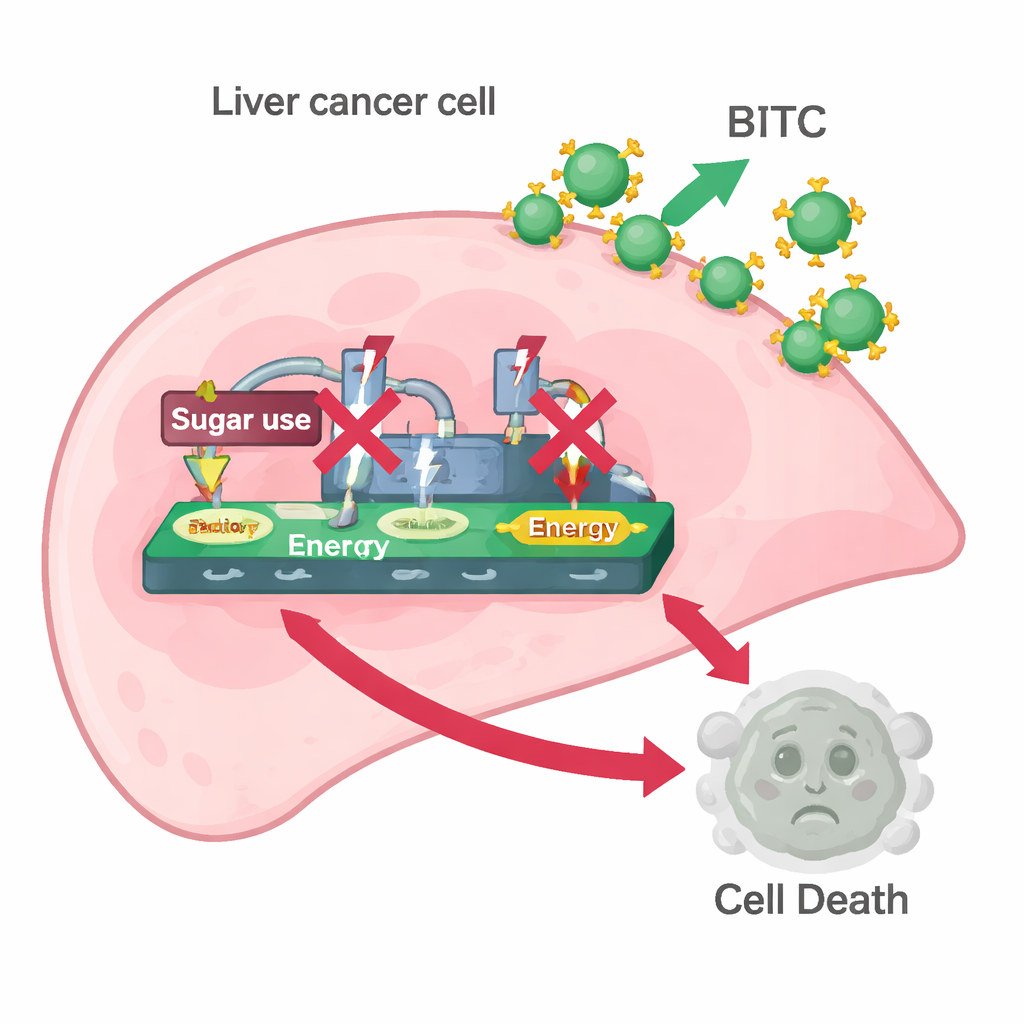
Отключение «сахарной» жажды рака
Затем команда исследовала, влияет ли BITC на эффект Варбурга. Они измерили уровни белков, помогающих раковым клеткам утилизировать глюкозу и превращать её в энергию и лактат — в частности HK2, PKM2 и LDH. Лечение BITC снизило уровни всех трёх белков в обеих линиях и уменьшило количество лактата, выделяемого клетками, а также поглощение глюкозы из среды. Другими словами, BITC делал клетки рака печени менее способными поддерживать свой ускоренный «сахарный» обмен. Когда учёные добавили пируват — продукт распада сахара, который всё ещё может подпитывать метаболизм клеток — многие эффекты BITC были обращены: уровни PARP, каспазы-3 и ферментов гликолиза восстановились. Эта «спасительная» реакция указывает на то, что вмешательство в переработку сахара является ключевой составляющей механизма, с помощью которого BITC вызывает гибель клеток.
Распутывая внутриклеточные переключатели управления
Чтобы понять более глубокие уровни контроля, исследователи сосредоточились на сигнальном трио: CNOT2, c-Myc и STAT3. Эти белки способствуют росту, выживанию и метаболической перенастройке во многих опухолях. Данные у больных раком печени показали, что уровень CNOT2, как правило, выше у пациентов с худшим прогнозом. В лабораторных экспериментах лечение BITC снижало активную, фосфорилированную форму STAT3, его верхний активатор JAK1, провоцирующий рост белок c-Myc и сам CNOT2. Генетическое снижение уровней CNOT2 или STAT3 усиливало цитотоксический эффект BITC, ещё сильнее снижая PARP и каспазу-3. Эксперименты по выявлению белковых взаимодействий показали, что BITC также нарушает физические взаимодействия между CNOT2 и STAT3 и между CNOT2 и c-Myc. Когда CNOT2 или c-Myc искусственно повышали, BITC терял большую часть своей способности подавлять ферменты гликолиза и вызывать апоптоз, что подчёркивает, что эта сигнальная ось функционирует как главный переключатель, связывающий сахарный обмен и выживание.
Что это может значить для будущих терапий
В совокупности результаты рисуют последовательную картину: BITC атакует клетки рака печени, перекрывая их предпочтительную «сахарную» топливную линию и активируя механизмы гибели клетки, зависящие от оси CNOT2/c-Myc/STAT3. Блокируя как сигналы роста, так и использование глюкозы, BITC толкает раковые клетки через метаболическую точку перегиба к апоптозу. Эти данные получены в экспериментах на культурах клеток, а не у пациентов, и исследованы всего две линии рака печени, поэтому необходимы дальнейшие работы на животных и в клинических условиях. Тем не менее исследование укрепляет идею о том, что определённые соединения из повседневных овощей могут быть доработаны или использованы в сочетании с другими методами для более точного истощения опухолей печени и стимулирования их саморазрушения.
Цитирование: Koh, W., Park, SY., Kim, B. et al. CNOT2 /c-Myc/STAT3 signaling is critically involved in glycolysis mediated apoptosis of benzyl isothiocyanate in hepatocellular carcinoma. Sci Rep 16, 7000 (2026). https://doi.org/10.1038/s41598-026-38416-8
Ключевые слова: рак печени, бензил-изотиоцианат, метаболизм рака, апоптоз, крестоцветные овощи