Clear Sky Science · ru
Влияние усечённого мутантного фактора V на гемостатическую функцию и эмбриональное развитие у мышей
Почему это важно для крови и развития плода
Большинство из нас думает о свёртывании крови только при порезе, но та же система, которая останавливает кровотечение из содранного колена, также участвует в формировании и защите сосудов в утробе. В этом исследовании рассматривается один ключевой участник этой системы — белок фактор V — и задаётся на вид простым вопросом: что происходит с развивающейся мышью, если этот помощник сильно повреждён? Ответ проливает свет на редкое кровоточивое заболевание у людей и на скрытую роль, которую свёртывание играет в обеспечении выживания и роста эмбрионов.
Скрытый участник жизни и смерти
Фактор V находится на пересечении процессов свёртывания, помогая крови превращаться из жидкости в стабильную пробку при повреждении сосуда. Люди, рождающиеся с недостатком функционального фактора V, могут страдать от тяжёлых, иногда опасных для жизни кровотечений. Предыдущие работы показали, что полное удаление фактора V у мышей обычно смертельно до или вскоре после рождения, но было неясно, как именно этот белок поддерживает растущие сосуды. Авторы решили изучить эту связь, используя штамм мышей, созданный с помощью инструментов редактирования генома, который неожиданно дал усечённую версию фактора V вместо планируемого мягкого дефекта.
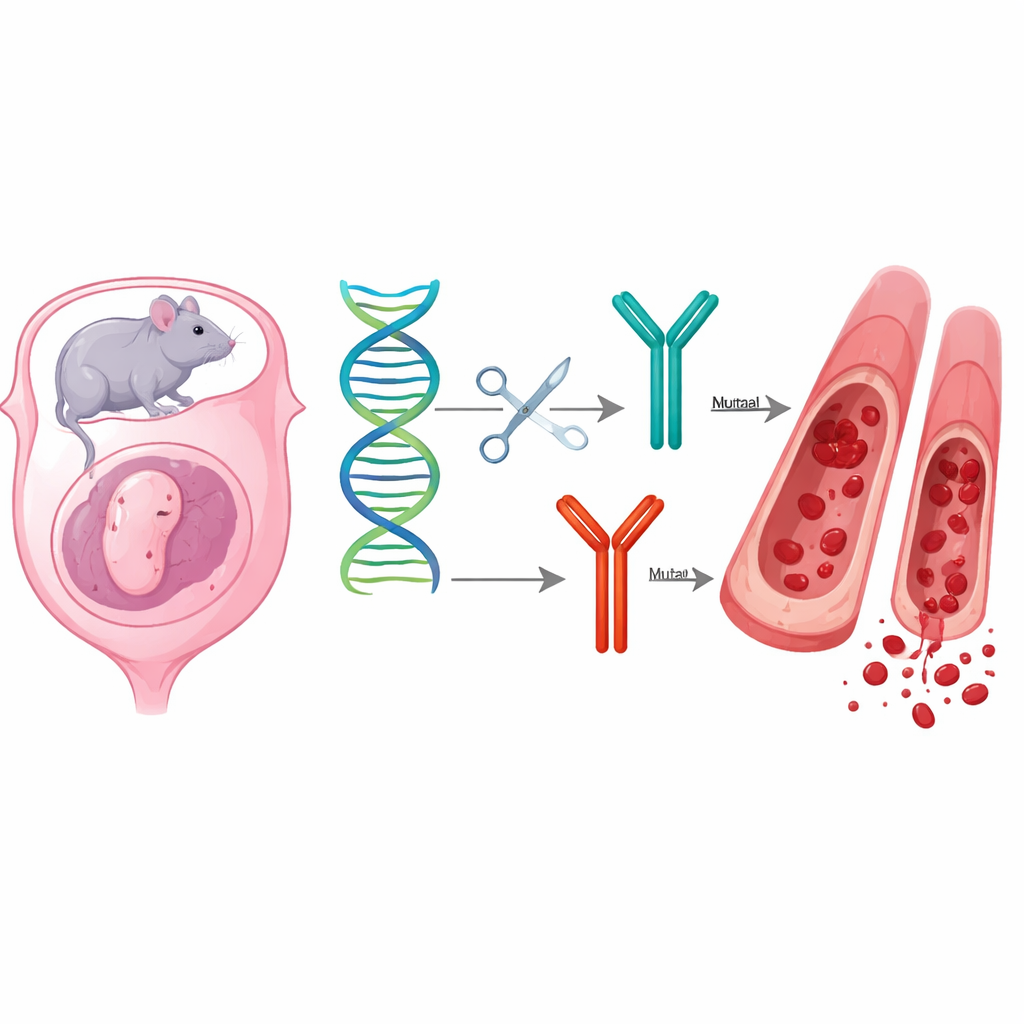
Случайная мутация с тяжёлыми последствиями
С помощью редактирования генов CRISPR команда изменила ген фактора V в эмбрионах мышей. Наряду с запланированным мягким изменением возник второй вариант: небольшое удаление, сдвинувшее рамку считывания и прервавшее белок близко к его концу. Мыши с одной нормальной и одной мутантной копией гена (гетерозиготы) рождались живыми, но их анализы крови показали, что активность фактора V упала примерно до одной пятой от обычной, а время свертывания было явно удлинено. При скрещивании двух носителей ожидаемое соотношение потомства было искажено. Намного меньше животных оказалось с двумя мутантными копиями, и большинство из них умирали около рождения с распространёнными кровоизлияниями в кожу и органы или выживали всего несколько недель, погибая без очевидных внешних кровотечений.
Что показывают ткани
Чтобы понять, что шло не так, исследователи изучили органы поражённых и нормальных животных под микроскопом и использовали методы окрашивания для отслеживания трёх ключевых молекул: самого фактора V, тромбина (фермента, который фактически образует сгустки) и структурного белка альфа-гладкомышечного актина, который укрепляет стенки сосудов. У новорождённых мышей с двумя мутантными копиями наблюдалась застой кровеносных сосудов и мелкие утечки во многих тканях. В их мозге и печени сигналы тромбина были значительно слабее, чем у нормальных детёнышей, что отражает низкую свертывающую активность. Сигналы фактора V также были снижены или отсутствовали вне печени, что указывает на то, что усечённый белок вырабатывался плохо, был нестабилен или не распознавался окраской. В печени и сердце слой гладкой мускулатуры вокруг сосудов окрашивался слабо и выглядел тоньше, что предполагает недоразвитие стенок сосудов и их повышенную хрупкость.
Когда и где включается фактор V
Команда также измеряла активность гена фактора V на разных стадиях эмбрионального развития мыши. Они выяснили, что активность гена постепенно возрастает от ранних стадий до поздней гестации, а затем резко увеличивается в печёночной ткани взрослых животных, подтверждая эту роль печени как основного источника. В разных тканях ранние эмбрионы демонстрировали относительно высокую активность гена фактора V в желточном мешке, временном, высоко васкуляризированном органе, который питает эмбрион до того, как плацента возьмёт на себя эту функцию. По мере развития печень и область, дающая начало будущим кровеносным и сосудистым клеткам, становились основными источниками продукции фактора V. Эти закономерности согласуются с идеей, что фактор V поддерживает раннее формирование сосудов в желточном мешке и позже помогает созреванию растущей сосудистой системы.
Что это значит для кровотечивых заболеваний
В совокупности результаты рисуют картину, в которой серьёзно повреждённый белок фактора V подрывает как способность крови свёртываться, так и нормальное формирование стенок кровеносных сосудов во время развития. У мутантных мышей снижение фактора V приводит к плохой генерации тромбина и ослаблению гладкомышечной поддержки вокруг сосудов, что делает их склонными к протечкам и разрывам. Многие эмбрионы, вероятно, погибают и резорбируются до рождения, а те, кто рождается, сталкиваются с высоким риском фатальных кровотечений, особенно в мозге. Для людей с наследственным дефицитом фактора V эти результаты помогают объяснить, почему в некоторых семьях наблюдаются выкидыши и почему очень низкий уровень белка вызывает такое тяжёлое заболевание. В более широком смысле работа подчёркивает, что система свёртывания — это не просто аварийная ремонтная бригада, но активный партнёр в формировании и стабилизации сосудистой сети, от которой зависит каждый эмбрион.
Цитирование: Miguel-Batuecas, A., De Pablo-Moreno, J.A., Porras, N. et al. Effect of a truncated mutant factor V on hemostatic function and embryonic development in mice. Sci Rep 16, 8460 (2026). https://doi.org/10.1038/s41598-026-38387-w
Ключевые слова: дефицит фактора V, свёртывание крови, эмбриональное развитие, сосудистая биология, модель мыши с помощью CRISPR