Clear Sky Science · ru
Прогностическая модель на основе машинного обучения, объединяющая гены, связанные со стволовостью и ангиогенезом, для прогнозирования выживаемости и иммунной инфильтрации у пациентов с ГЦК
Почему это исследование важно для пациентов с раком печени
Гепатоцеллюлярная карцинома — наиболее распространённая форма рака печени — часто рецидивирует или метастазирует даже после лечения. В этом исследовании изучают причины таких исходов и способы более точного прогнозирования пациентов с высоким риском. Комбинируя большие генетические наборы данных с современными методами машинного обучения, авторы создали инструмент, связывающий два ключевых свойства рака — «стволовость» (клетки, ведущие себя как устойчивые «семена») и ангиогенез (образование новых сосудов) — с прогнозом выживания и вероятной реакцией на иммунотерапию.
Раковые «семена» и новые кровеносные сосуды
Во многих опухолях есть небольшая популяция клеток, действующих как семена. Эти раковые стволовые клетки способны к самоподдержанию, устойчивы к лечению и могут возобновлять рост опухоли после операции или химиотерапии. Одновременно опухоли нуждаются в формировании новых сосудов, чтобы получать кислород и питательные вещества для роста и метастазирования. Последние данные показывают, что эти процессы взаимосвязаны: стволоподобные клетки выделяют сигналы, стимулирующие ангиогенез, а сосудистая среда, в свою очередь, поддерживает выживание таких клеток. Понимание и совместная блокада этого взаимодействия особенно важны при раке печени, который отличается высокой сосудистостью и склонностью к рецидивам.
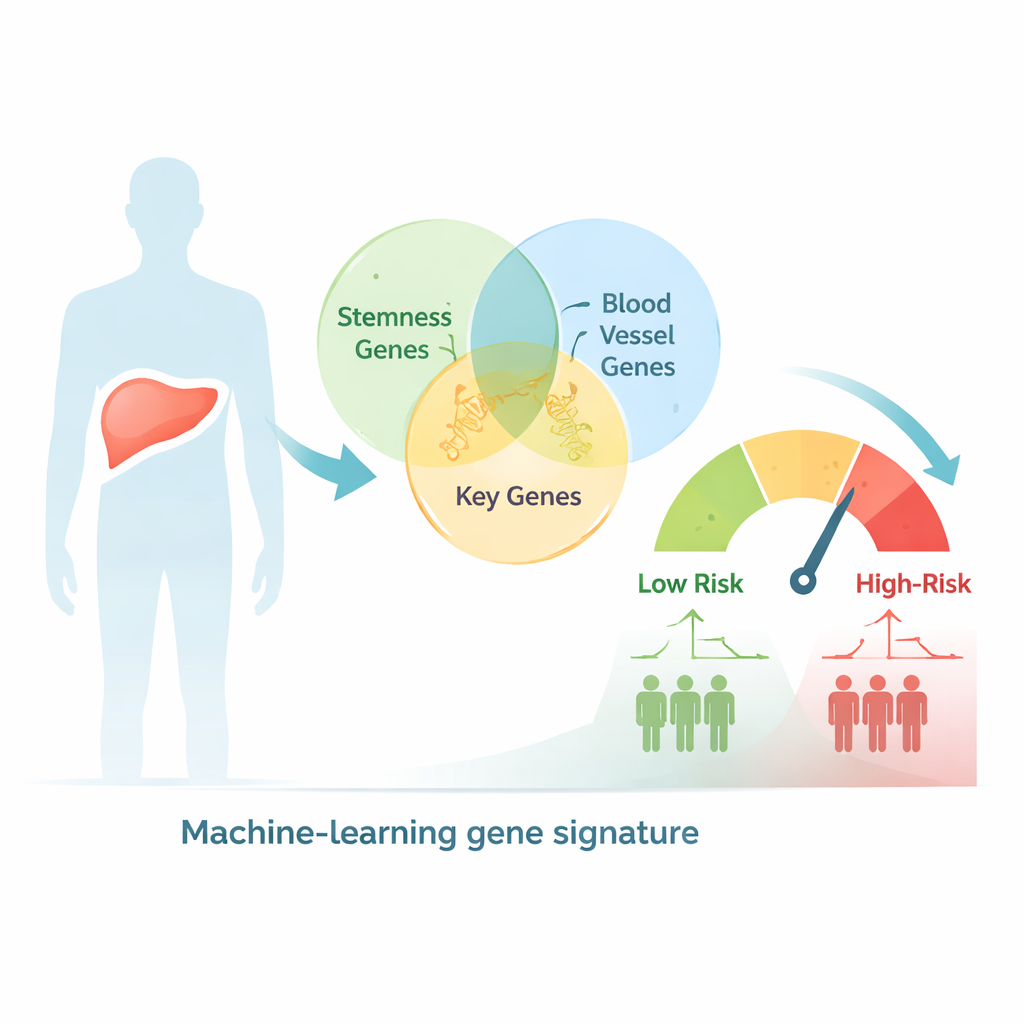
Использование больших данных для сортировки пациентов по риску
Исследователи начали с поиска в большой базе данных человеческих генов тех, которые связаны и со стволовыми свойствами, и с образованием сосудов, в результате выделив более 2600 пересекающихся кандидатов. Затем они проанализировали образцы печёночных опухолей у сотен пациентов, чья генетическая активность и клинические исходы были задокументированы в публичных онкологических базах. С помощью статистических тестов и методов кластеризации пациентов разделили на два генетических подтипа, которые существенно различались по стадии, размеру опухоли и выживаемости, что указывает на то, что объединённые сигналы, связанные со стволовостью и ангиогенезом, отражают значимую биологию при этом заболевании.
Построение риска на основе девяти генов
Из большого пула генов команда с помощью подходов машинного обучения сузила список до девяти ключевых генов, комбинация активности которых наилучшим образом предсказывала продолжительность жизни пациентов. На основе этих девяти генов был рассчитан риск‑балл для каждого пациента. У больных с высоким баллом общая выживаемость была значительно ниже как в исходной выборке, так и в независимой когорте для валидации. Точность модели сопоставима или превосходит многие существующие инструменты, а при объединении балла с простыми клиническими данными, такими как стадия опухоли, в номограмме прогнозирование выживаемости на 1, 3 и 5 лет улучшалось ещё сильнее.
Связь с иммунной системой и ответом на лечение
Авторы также изучили, что показывает девятигенный счёт о иммунной среде опухоли. Низко‑рисковые опухоли, как правило, были более «воспалёнными» — в них обнаруживались более высокие уровни разнообразных иммунных клеток и усиленные сигналы атакующих путей. Высоко‑рисковые опухоли напротив демонстрировали профили, согласующиеся с уклонением от иммунного надзора и более высокой частотой мутаций в ключевых генах, таких как TP53. С использованием проверенных вычислительных инструментов для оценки вероятного ответа на современные иммунотерапевтические препараты исследование предположило, что пациенты низкого риска могут лучше отвечать на ингибиторы контрольных точек иммунитета по сравнению с пациентами высокого риска. Эти предсказания требуют подтверждения в клинических условиях, но указывают на практический путь отбора пациентов, которые могут получить наибольшую пользу от таких препаратов.
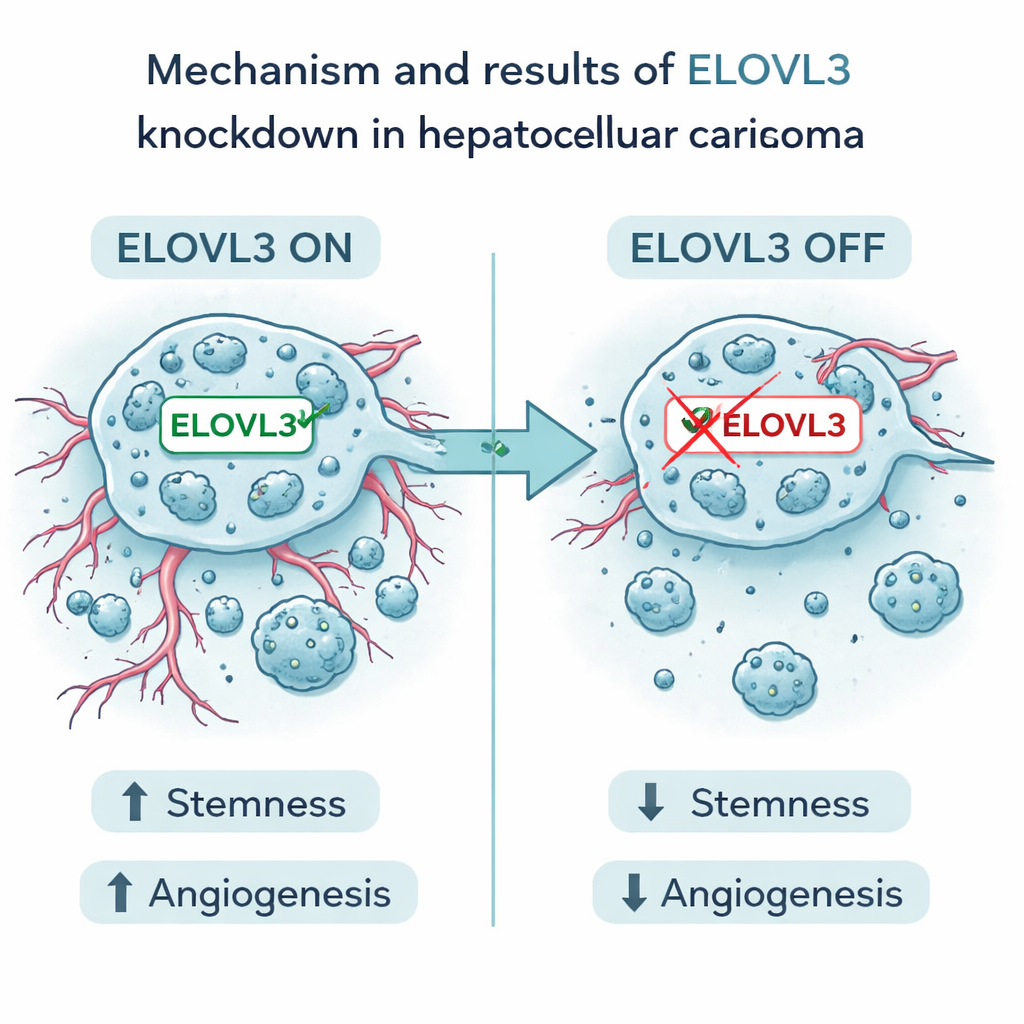
Фокус на одном перспективном мишени
Из девяти генов выделялся один — ELOVL3. Высокая экспрессия этого гена ассоциировалась с худшей выживаемостью. В лабораторных экспериментах авторы подавляли ELOVL3 в клетках человеческой раковой печени. Это уменьшало способность клеток формировать стволоподобные скопления и снижало уровни известных маркеров стволовости. Также уменьшалось производство и выделение двух ключевых факторов, стимулирующих ангиогенез — VEGFA и FGF2. Раковые клетки становились менее пролиферативными, менее подвижными и менее инвазивными, а в модельных экспериментах на мышах опухоли с пониженной экспрессией ELOVL3 были меньшими и демонстрировали менее агрессивные признаки. Эти результаты поддерживают идею, что ELOVL3 способствует как стволоподобному поведению клеток печени при раке, так и их способности формировать поддерживающую сосудистую сеть.
Что это может значить для будущего лечения
Проще говоря, у этого исследования два ключевых вывода. Во‑первых, простой риск‑балл на основе девяти генов, получаемый из образцов опухоли, позволяет разделить пациентов с раком печени на группы более высокого и более низкого риска и дать предположение о вероятной реакции на иммунотерапию. Во‑вторых, один из генов в этом профиле, ELOVL3, кажется центральным для регенеративного потенциала опухоли и ангиогенеза, что делает его привлекательной мишенью для будущей терапии. Хотя модель и сама мишень требуют подтверждения в проспективных клинических испытаниях, они открывают путь к более персонализированному лечению рака печени и комбинированным стратегиям, направленным как на «раковые семена», так и на их кровоснабжение.
Цитирование: Cheng, F., Shi, Y., Gao, X. et al. Machine learning-based prognostic model of stemness and angiogenesis-related genes for predicting prognosis and immune infiltration in patients with HCC. Sci Rep 16, 7271 (2026). https://doi.org/10.1038/s41598-026-38379-w
Ключевые слова: гепатоцеллюлярная карцинома, раковые стволовые клетки, ангиогенез, прогностическая генетическая подпись, ELOVL3