Clear Sky Science · ru
Ингибирование галанинового рецептора 3 замедляет дегенерацию сетчатки при пигментном ретините за счёт модуляции воспалительной реакции и окислительного стресса
Почему важно защищать угасающее ночное зрение
Пигментный ретинит — это группа наследственных заболеваний, которые постепенно лишают людей ночного и периферического зрения и часто приводят к значительной потере зрения в среднем возрасте. Широко эффективного лечения нет, отчасти потому, что заболевание могут вызывать многие разные генетические мутации. В этом исследовании рассматривается иной подход: вместо исправления повреждённого гена авторы спрашивают, можно ли замедлить потерю светочувствительных клеток и сохранить зрение, ослабив вредное воспаление и «ржавление» — окислительное повреждение в сетчатке.
Переключатель стресса, скрытый в сетчатке
Фоторецепторы, воспринимающие свет на задней части глаза, постоянно балансируют энергопотребление, кислород, питание и удаление отходов. При одной распространённой форме пигментного ретинита мутация в родопсине (известная как P23H) вызывает неправильную свёртку этого визуального пигмента, что засоряет внутриклеточные механизмы и запускает хронический стресс. Этот стресс, в свою очередь, провоцирует воспаление и окислительное повреждение, которые могут убить фоторецепторы. Авторы сосредоточились на сигнальном белке галаниновом рецепторе 3 (GALR3), присутствующем в нескольких типах клеток сетчатки. Они обнаружили, что у мышей с мутацией P23H GALR3 и его природные партнёрные молекулы были включены сильнее, чем в здоровых глазах, что указывает на то, что GALR3 может действовать как усилитель стресса в дегенерирующей сетчатке.
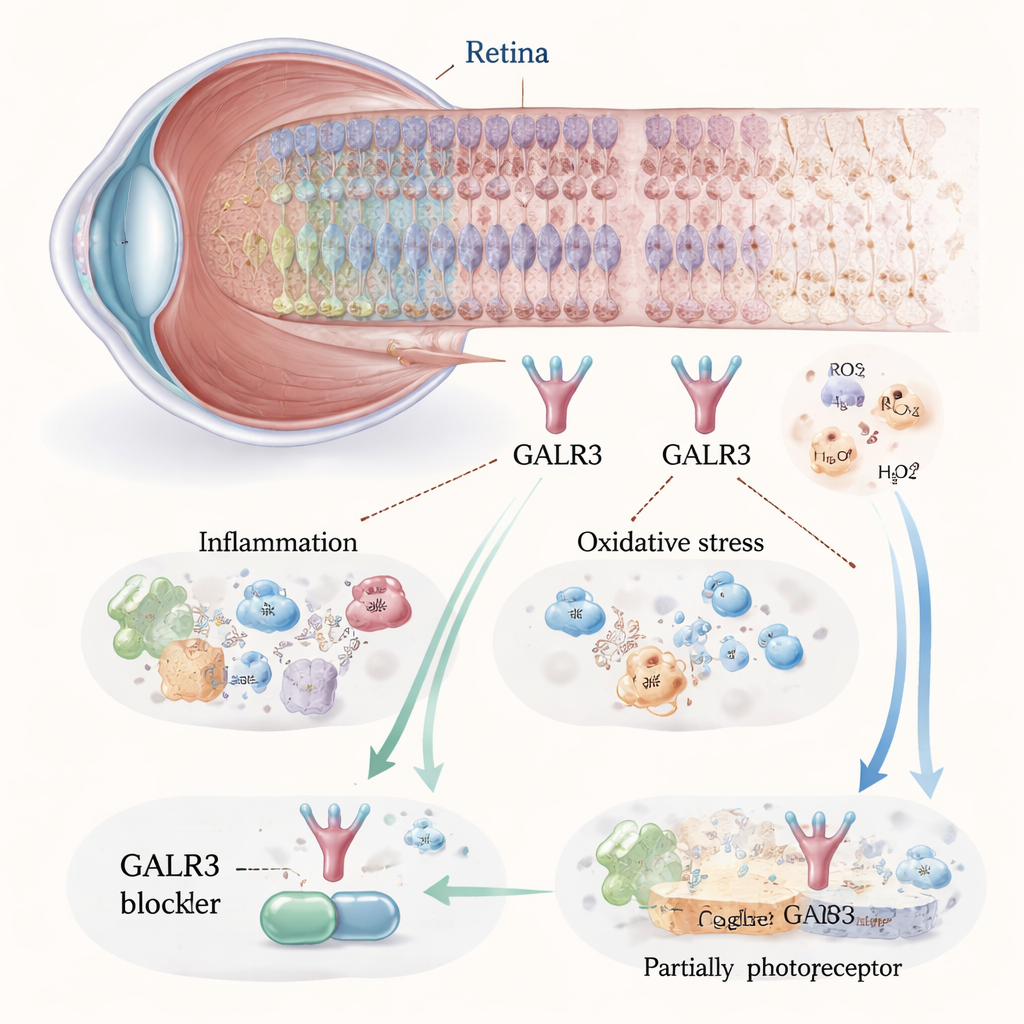
Замедление гибели клеток блокированием вредного сигнала
Чтобы проверить, движет ли GALR3 повреждение или защиту, исследователи использовали две стратегии на мышах P23H: они разводили животных, полностью лишённых гена Galr3, и лечили других препаратом SNAP-37,889, который специально блокирует этот рецептор. В течение нескольких недель они изучали структуру сетчатки с помощью высокоразрешающей визуализации и измеряли электрические ответы на свет. У нелечёных мышей P23H слой ядер фоторецепторов истончался примерно вдвое по сравнению с нормальными мышами к месячному возрасту и продолжал сокращаться. При блокировании GALR3 это истончение было значительно снижено, а ключевые зрительные белки, такие как родопсин и конусный опсин, сохранялись на более высоких уровнях. Электрические записи из сетчатки также показали более сильные световые ответы у леченных или лишённых GALR3 мышей, что означает: выжившие клетки функционировали лучше, а не просто оставались присутствующими.
Ослабление воспаления и усиление защитных механизмов
Команда затем выясняла, почему ингибирование GALR3 помогало. При пигментном ретините поддерживающие клетки сетчатки — клетки Мюллера и микроглия — переходят от роли попечителей к гиперактивным реагентам, подпитывающим хроническое воспаление. У мышей P23H маркёры этого «сигнального состояния», включая GFAP в глиальных клетках и IBA-1 в микроглии, были сильно повышены, а набор воспалительных молекул и комплексов распознавания опасности, таких как NF-κB и инфламмасома NLRP3, тоже увеличивался. Блокада GALR3 успокаивала этот ответ: активация глии уменьшалась, уровни провоспалительных цитокинов падали, а противовоспалительные сигналы, связанные с восстановлением тканей, такие как IL‑10 и TGF‑β1, повышались на ранних стадиях болезни. Параллельно ингибирование GALR3 укрепляло антиоксидантный потенциал сетчатки. Оно усиливало активность NRF2, главного регулятора антиоксидантных генов, и увеличивало ферменты, нейтрализующие реактивные формы кислорода, помогая ограничить дальнейшее повреждение от метаболического стресса.
Защита внутреннего барьера глаза
Здоровое зрение также зависит от плотного «кровь–сетчатка барьера», который не допускает попадания нежелательных молекул и иммунных клеток в деликатную нервную ткань. У мышей P23H этот барьер начал протекать: контакты между клетками пигментного эпителия сетчатки становились нарушенными, и белки крови просачивались в сетчатку. Как генетическое удаление, так и фармакологическая блокада GALR3 значительно уменьшали эти нарушения, сохраняя аккуратный, плиточный рисунок барьера и ограничивая утечку. В экспериментах на клеточных культурах фоторецептороподобные клетки, подвергшиеся воздействию воспалительных сигналов от активированной микроглии, усиливали экспрессию собственных воспалительных генов, но этот эффект ослабевал, когда GALR3 в фоторецепторных клетках был заглушен. В совокупности эти результаты показывают, что GALR3 находится на перекрёстке, связывающем активацию микроглии, окислительный стресс и разрушение барьера с гибелью фоторецепторов.
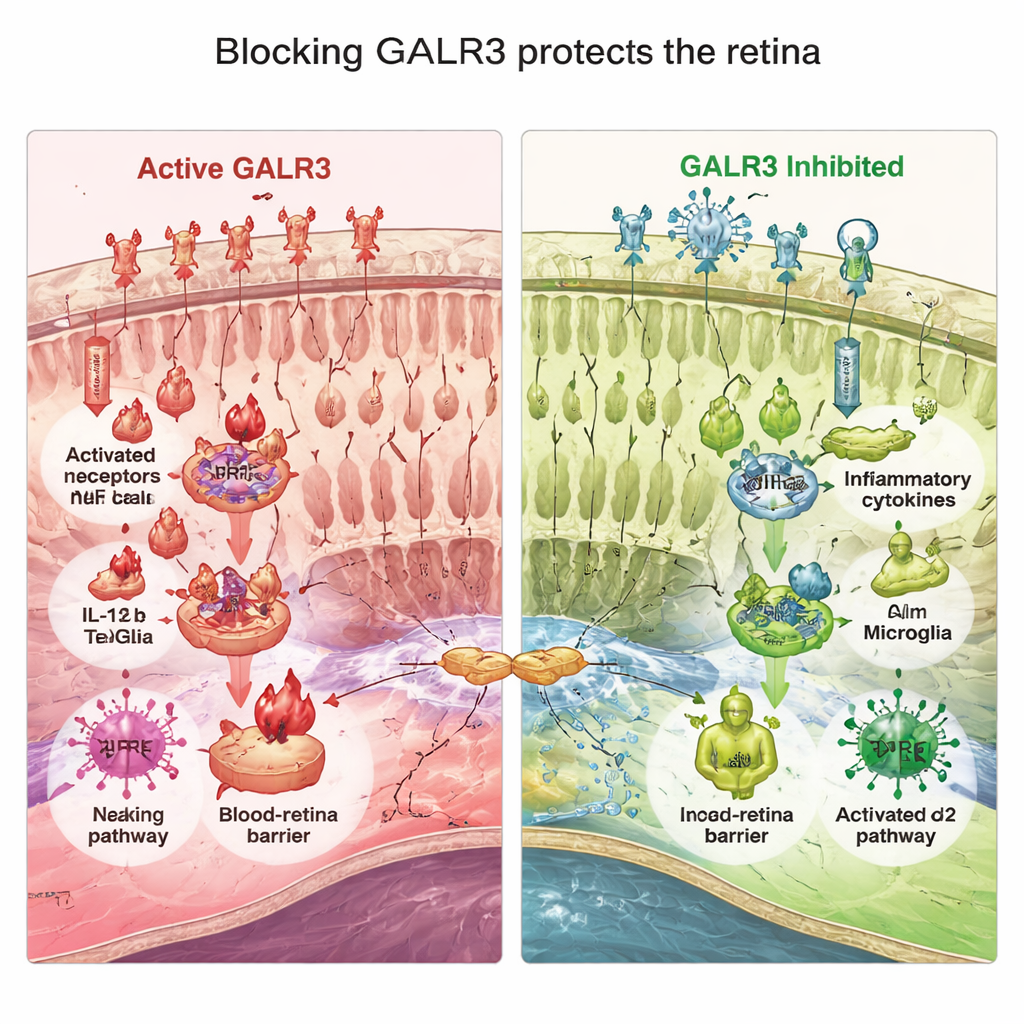
Подход к спасению зрения, не зависящий от конкретной мутации
Для людей с пигментным ретинитом, особенно для тех, кто может никогда не получить муто-специфическую терапию, стратегии, которые в целом замедляют повреждение сетчатки, имеют большую ценность. Это исследование выделяет GALR3 как ключевой «регулятор громкости» вредного воспаления и окислительного стресса в широко используемой мышиной модели болезни. Блокада GALR3 не излечивала пигментный ретинит, но стабильно замедляла потерю фоторецепторов, улучшала ответ сетчатки на свет, снижала токсичное воспаление, усиливала природные антиоксидантные защиты и помогала сохранять внутренний барьер глаза. Поскольку GALR3 воздействует на пути стресса и иммунитета, а не на конкретную мутацию, препараты, нацеленные на этот рецептор, теоретически могут помочь пациентам с разными генетическими причинами дегенерации сетчатки.
Цитирование: Azam, M., Pashandi, Z., Liu, M. et al. Inhibition of galanin receptor 3 slows down retina degeneration in retinitis pigmentosa through modulation of inflammatory and oxidative stress response. Sci Rep 16, 7765 (2026). https://doi.org/10.1038/s41598-026-38345-6
Ключевые слова: пигментный ретинит, воспаление сетчатки, выживание фоторецепторов, галаниновый рецептор 3, окислительный стресс