Clear Sky Science · ru
DGCR8 регулирует несколько этапов транскрипционно-связанного нуклеотидного восстановления
Как солнечный свет «разговаривает» с нашими генами
Каждый раз, выходя на солнце, мы подвергаемся действию невидимых ультрафиолетовых (УФ) лучей, которые повреждают ДНК в наших клетках. Чаще всего клетки незаметно исправляют такие повреждения до того, как они приведут к проблемам. В этом исследовании обнаруживается неожиданный участник этой защитной системы: белок DGCR8, ранее известный своей ролью в образовании микроРНК. Авторы показывают, что после УФ‑облучения DGCR8 может менять функцию и координировать несколько этапов ключевого пути восстановления ДНК, который помогает предотвращать развитие рака и других заболеваний.
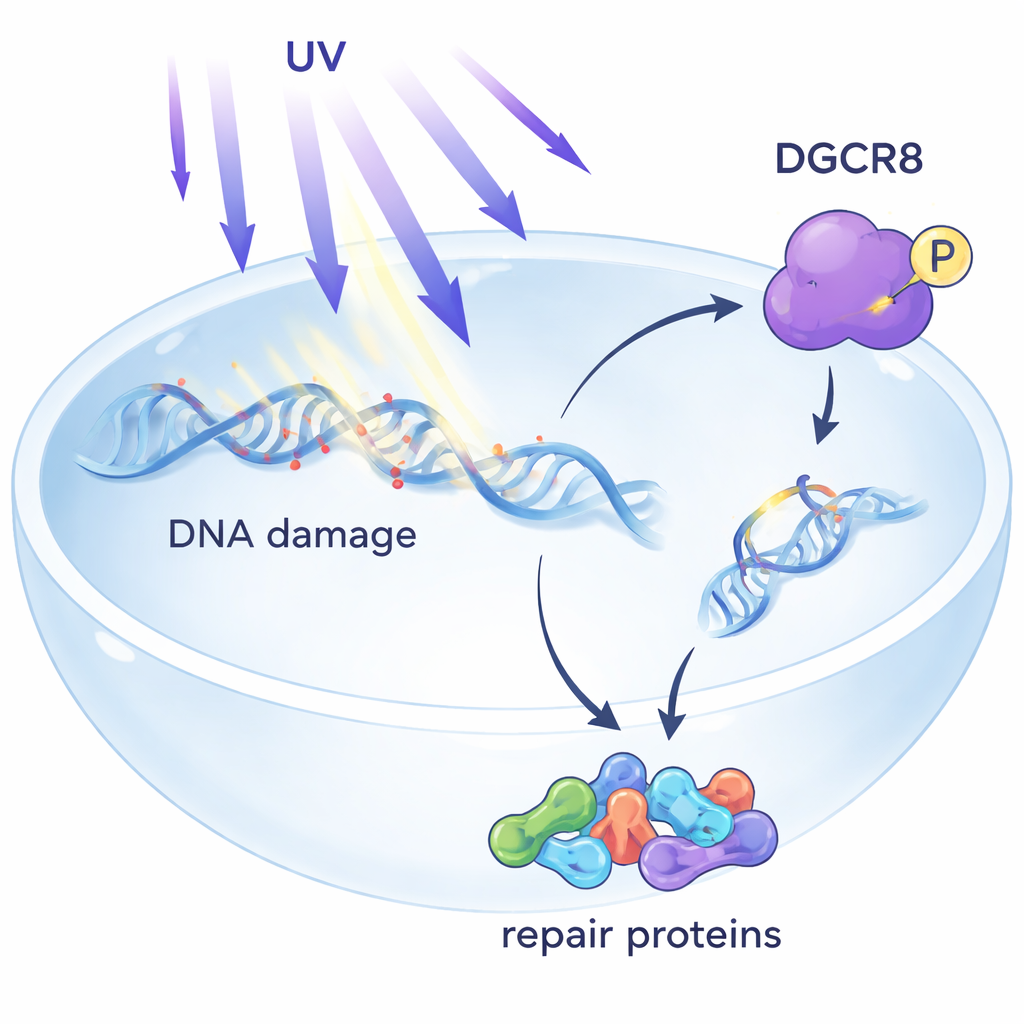
Скрытый страж внутри системы восстановления ДНК
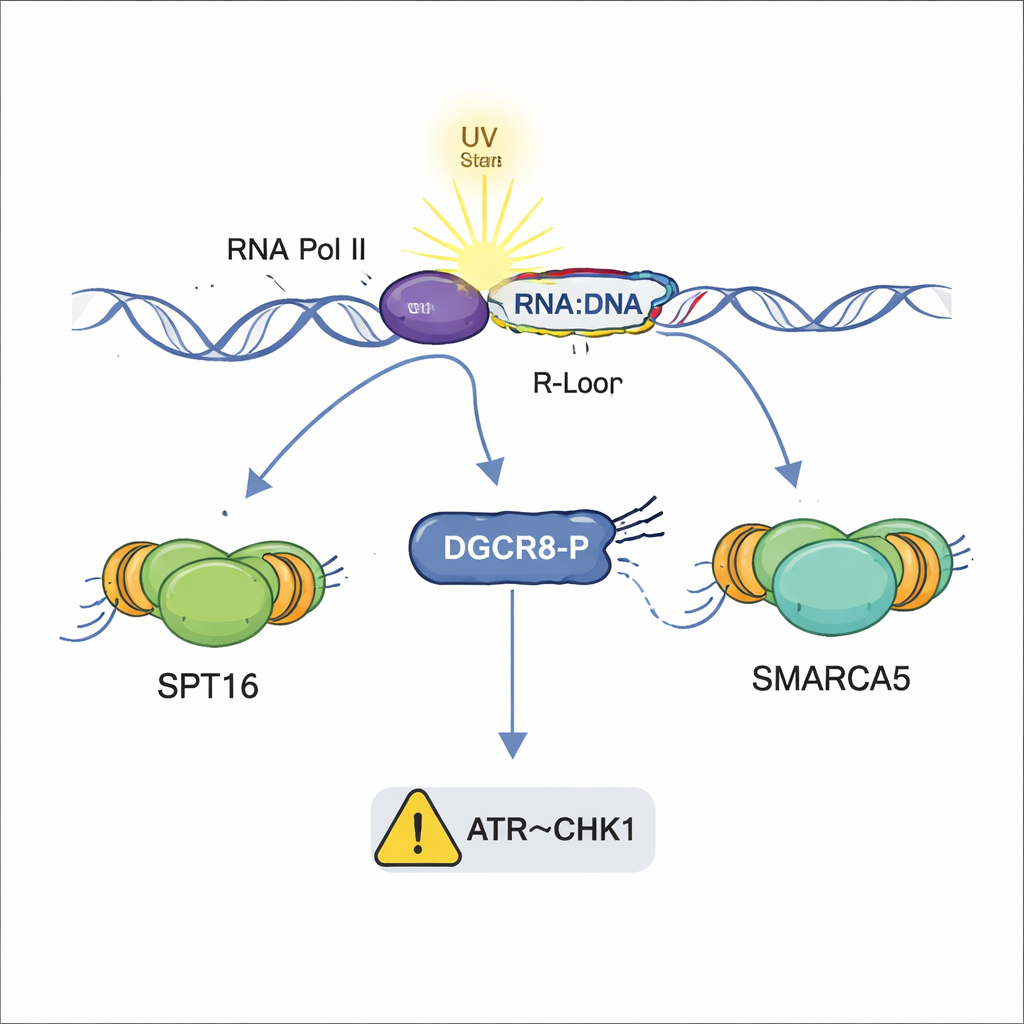
УФ‑свет создаёт небольшие повреждения в ДНК, которые могут блокировать молекулярные «машины», считывающие гены. Одна из основных защит — транскрипционно‑связанное нуклеотидное восстановление (TC‑NER), направленное на повреждения, останавливающие ферменты транскрипции. До сих пор DGCR8 в основном знали как фактор процессинга микроРНК — коротких РНК, регулирующих активность генов. Предыдущие исследования намекали, что DGCR8 также защищает клетки от УФ, но механизм оставался неясен. В этой работе показано, что при УФ‑воздействии DGCR8 физически ассоциируется с центральными факторами TC‑NER, действуя как организатор, который собирает компоненты восстановления прямо там, где тормозится считывание генов.
Молекулярный тумблер для DGCR8
Ключ к новой роли DGCR8 — одна химическая метка на одном из его аминокислотных остатков, серине в позиции 153. Когда этот сайт фосфорилируется — то есть к нему присоединяется фосфатная группа — DGCR8 приобретает способность связываться с основными участниками TC‑NER, включая РНК‑полимеразу II (фермент считывания генов) и факторы восстановления CSB, CSA и UVSSA. Клетки с вариантом DGCR8, который не может быть фосфорилирован в этой позиции (мутант S153A), показали ослабленные или утраченные взаимодействия между этими репарационными белками, и нормальная сборка комплекса в ответ на УФ не происходила. «Фосфоромиметический» вариант, имитирующий постоянную фосфорилированность, давал противоположный эффект — усиливал ключевые взаимодействия даже без УФ. Эти результаты указывают на то, что фосфорилирование на Ser153 действует как переключатель, переводящий DGCR8 из обычной роли в процессинге РНК в координатора ремонта ДНК.
Распутывание опасных узлов ДНК–РНК
Кроме сбора репарационных белков, DGCR8 также помогает управлять структурами, называемыми R‑петлями — короткими участками, где вновь синтезированная РНК вновь присоединяется к материнской ДНК, образуя гибрид ДНК–РНК. В малых количествах R‑петли могут быть полезны, но при накоплении после УФ они могут блокировать репликацию и дестабилизировать хромосомы. С помощью специальных антител и флуоресцентных зондов авторы обнаружили, что клетки, лишённые DGCR8 или несущие нефосфорилируемый вариант S153A, накапливают значительно больше R‑петель после УФ. Фосфорилированный DGCR8 визуализировали на этих гибридных структурах, особенно в местах перекрытия с УФ‑индуцированными повреждениями, что предполагает его роль в предотвращении или удалении вредных R‑петлей точно в активных генах под стрессом.
Контроль копирования ДНК
Когда повреждения ДНК или R‑петли мешают копированию генома, клетки обычно замедляют репликацию через контрольную точку ATR–CHK1. Эксперименты с отслеживанием волокон показали, что в клетках с нормальным DGCR8 длины репликативных треков замедлялись после УФ, что отражает включённую контрольную точку. В резком контрасте клетки, лишённые DGCR8 или несущие мутант S153A, продолжали реплицироваться почти с нормальной скоростью, несмотря на накопившиеся повреждения ДНК и R‑петли. Дополнительные испытания показали, что хотя сам ATR активировался, его ключевой партнёр CHK1 был слабо включён в этих мутантных клетках. Это указывает на то, что фосфорилированный DGCR8 помогает передавать сигнал стресса от повреждённой ДНК и R‑петель к CHK1, позволяя клетке приостановить и стабилизировать репликацию.
Почему это важно для здоровья и болезней
В совокупности данные выявляют DGCR8 как многофункционального стража, координирующего несколько уровней ответа на УФ‑повреждения: сбор команды TC‑NER, привлечение хроматин‑ремоделеров, которые открывают ДНК, сдерживание вредных гибридов ДНК–РНК и помощь в запуске замедления репликации через путь ATR–CHK1. Существенно, эти действия отделены от традиционной роли DGCR8 в биогенезе микроРНК и зависят от фосфорилирования одного сайта. Поскольку нарушения в репарации ДНК и контроле R‑петель связаны с раком и неврологическими заболеваниями, а мутации DGCR8 обнаружены в некоторых опухолях, понимание этого молекулярного переключателя может открыть новые пути для диагностики или лечения состояний, вызванных УФ‑повреждением и нестабильностью генома.
Цитирование: Watanabe, T., Yoshinami, D., Yamasaki, H. et al. DGCR8 regulates multiple processes of transcription coupled nucleotide excision repair. Sci Rep 16, 7112 (2026). https://doi.org/10.1038/s41598-026-38338-5
Ключевые слова: УФ‑повреждение ДНК, DGCR8, Ремонт ДНК, R‑петли, стабильность генома