Clear Sky Science · ru
Эффективная глубокая CNN‑BiLSTM архитектура с оптимизацией RanA для точного обнаружения кардиальных аритмий
Почему важны более умные проверки сердца
Нарушения ритма сердца, или аритмии, являются одной из основных причин внезапных заболеваний и смертей во всем мире. В настоящее время врачи в значительной степени полагаются на электрокардиограммы (ЭКГ) — знакомые извилистые линии на мониторе — чтобы выявлять опасность. Но просмотр длинных записей ЭКГ визуально занимает много времени, утомляет и легко приводит к ошибкам, особенно когда опасные события кратковременны или слабо выражены. В этой статье описана новая система искусственного интеллекта, способная просеивать большие записи ЭКГ и с высокой точностью обнаруживать два важных состояния — предсердную фибрилляцию и застойную сердечную недостаточность, что потенциально делает непрерывный мониторинг сердца в реальном времени значительно надежнее.
Разные ритмы — разные риски
Не все сердечные ритмы одинаковы. Предсердная фибрилляция (ПФ) — это нерегулярный, нередко учащенный ритм в верхних камерах сердца, который значительно повышает риск инсульта и сердечной недостаточности. Застойная сердечная недостаточность (ЗСН) — хроническое состояние, при котором сердце не может прокачивать достаточно крови, что приводит к утомляемости, задержке жидкости и, при отсутствии лечения, к летальному исходу. Напротив, нормальный синусовый ритм (НСР) — это устойчивый ритм, создаваемый естественным водителем ритма сердца. Авторы сосредоточены на двух практических вопросах: может ли компьютер надежно отличать ПФ от НСР и ЗСН от НСР, используя только данные ЭКГ? Решение этих задач поддержит более раннюю диагностику, более тщательное наблюдение пациентов с высоким риском и более быструю реакцию на скрытые предвестники болезни.
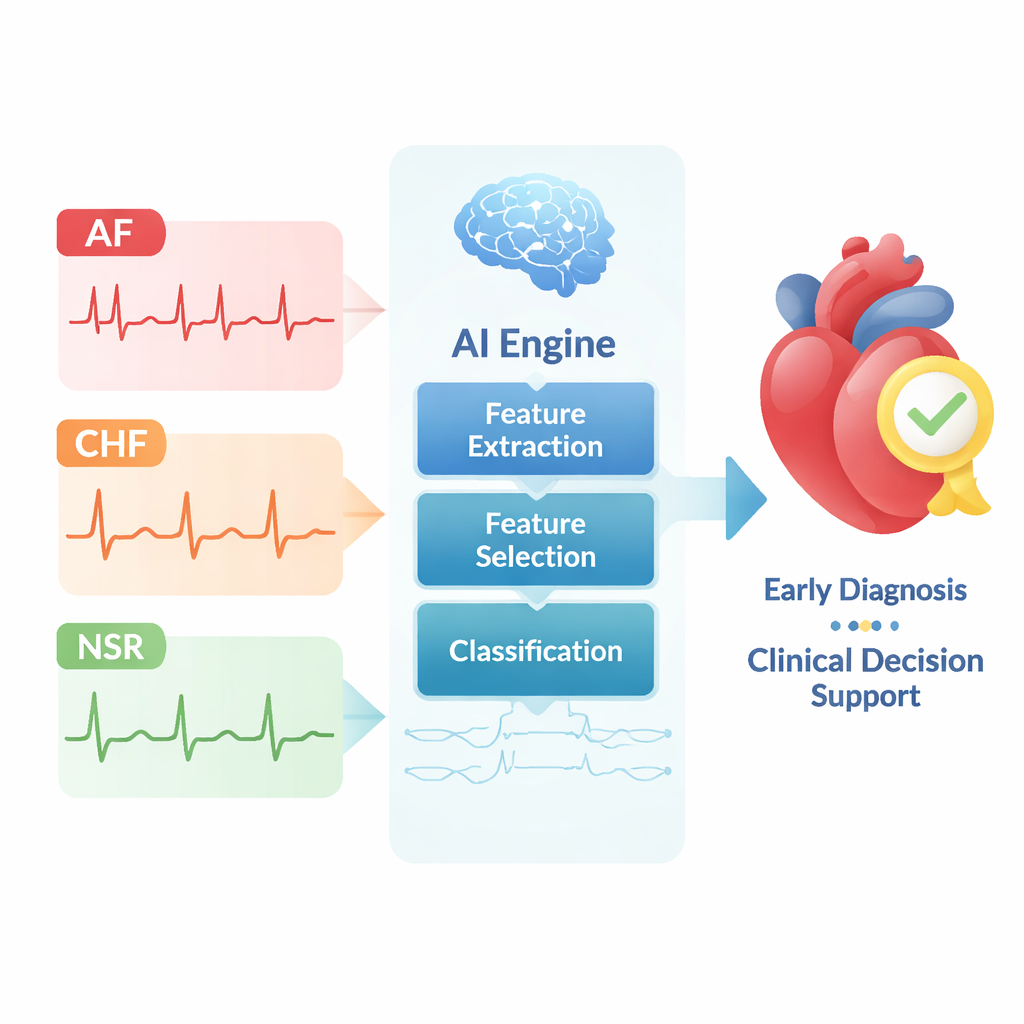
Обучение машин «читать» сердцебиение
Современные записи ЭКГ могут содержать миллионы точек данных на одного человека. Вручную выделить полезные шаблоны в этом море чисел практически невозможно. Поэтому исследователи строят многоступенчатый конвейер глубокого обучения. Сначала они собирают три хорошо известных набора данных ЭКГ из репозитория PhysioNet: записи с ПФ, записи с ЗСН и записи от людей с нормальным ритмом. Затем эти длинные сигналы разбивают на более короткие сегменты, чтобы компьютер мог эффективно их анализировать. Далее используется тип нейронной сети, называемой Capsule Network, чтобы сжать каждый сегмент в меньший набор чисел, сохраняя при этом общую форму и структуру сердечного цикла. Статистические тесты показывают, что этот шаг лучше разделяет патологические ритмы и нормальные, чем стандартные методы уменьшения размерности, такие как метод главных компонент.
Поиск самых показательных признаков сигнала
Даже после сжатия множество признаков сегментов ЭКГ остаются избыточными или слабо связанными с болезнью. Чтобы сосредоточиться на действительно важном, команда применяет несколько мощных нейросетей, изначально разработанных для обработки изображений — EfficientNet B3, ResNet152, DenseNet201 и VGG19 — в качестве интеллектуальных фильтров. Эти сети были созданы для распознавания объектов на картинках; здесь их перенаправляют на ранжирование признаков ЭКГ по способности отличать ПФ, ЗСН и нормальные ритмы. Среди них выделяется EfficientNet B3: она уравновешивает глубину и ширину сети, чтобы выделять только наиболее информативные шаблоны, и стабильно формирует признаки, более тесно связанные с метками заболеваний и лучше разделяющиеся между здоровыми и больными ритмами.
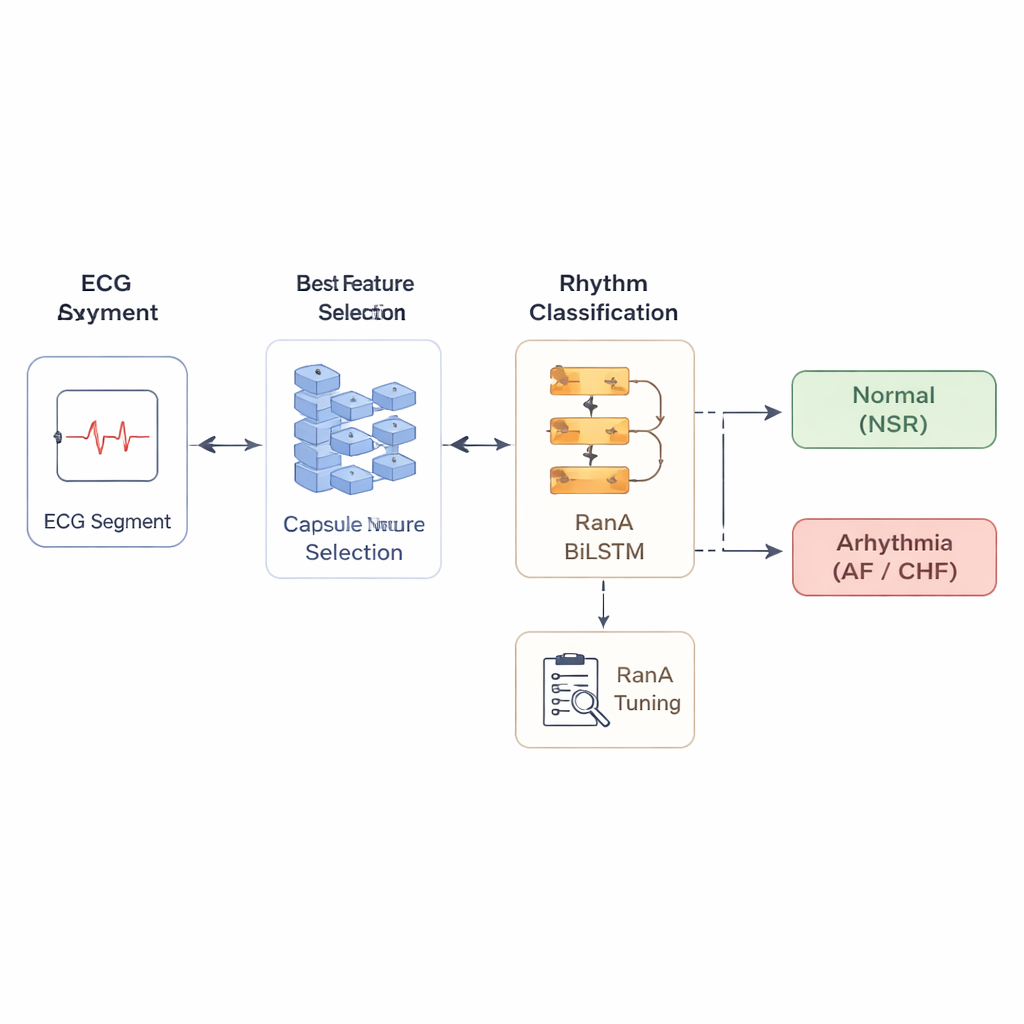
Слушая ритм во времени
Поскольку сигналы сердца разворачиваются как последовательности, окончательное решение принимает модель, хорошо обучающаяся на упорядоченных данных: двунаправленная сеть с длинной краткосрочной памятью, или BiLSTM. Эта модель «слушает» каждый сегмент в прямом и обратном направлениях, улавливая тонкие временные взаимосвязи, которые могут указывать на аритмию. Чтобы выжать дополнительную производительность, авторы настраивают многочисленные внутренние параметры этой модели с помощью стратегии, которую они называют Randomized Adam (RanA), вводящей контролируемую случайность в процесс обучения. Это помогает системе не застревать в плохих решениях и улучшает её способность обобщать на новых пациентах. Исследователи тщательно проверяют всю схему с помощью десятикратной кросс‑валидации и разбиения на обучение/тест в соотношении 70/30.
Насколько это хорошо работает на практике?
После оптимизации объединенная система EfficientNet B3 + BiLSTM + RanA демонстрирует впечатляющие показатели. Она правильно отличает ПФ от нормального ритма в 99.48% случаев и ЗСН от нормального ритма в 99.32% случаев — чуть лучше или сопоставимо с лучшими результатами, опубликованными в предыдущих работах. Метрики, особенно важные для несбалансированных медицинских данных, такие как F1‑мера, коэффициент корреляции Мэтьюса и площадь под ROC‑кривой, находятся очень близко к идеальным значениям. При этом модель обрабатывает каждый сегмент ЭКГ всего за несколько миллисекунд и использует относительно умеренное число параметров, что позволяет предположить возможность её работы на носимых устройствах или у постели пациента. Авторы отмечают, что расширение подхода на множество разных аритмий, работа с более шумными сигналами и дальнейшее снижение вычислительной сложности остаются ключевыми следующими шагами.
Что это значит для пациентов и врачей
Для неспециалиста основная мысль проста: эта работа показывает, что тщательно спроектированная система глубокого обучения может выступать в роли чрезвычайно точной «второй пары глаз» при анализе ЭКГ. Автоматически отделяя опасные нерегулярные ритмы и признаки сердечной недостаточности от нормальных комплексов и делая это практически в реальном времени, такие инструменты могут быстрее привлекать внимание клиницистов, поддерживать непрерывный домашний мониторинг и снижать вероятность того, что тихая, но серьезная проблема останется незамеченной. Хотя необходима дальнейшая валидация в более широких, реальных условиях, исследование указывает на будущее, в котором продвинутые алгоритмы незаметно сканируют наши сердцебиения в фоновом режиме, давая пациентам и врачам более ранние сигналы и больше уверенности.»}
Цитирование: Manivannan, G.S., Talawar, S.V., Vasundhara, M.G. et al. An efficient deep CNN based BiLSTM framework with RanA optimization for accurate cardiac arrhythmia detection. Sci Rep 16, 7156 (2026). https://doi.org/10.1038/s41598-026-38227-x
Ключевые слова: сердечная аритмия, электрокардиограмма, глубокое обучение, предсердная фибрилляция, сердечная недостаточность