Clear Sky Science · ru
Ингибирование пути SHH и ко‑культура с астроцитами вызывают разные ответы в глиобластоме и раковых стволовых клетках
Почему с опухолями мозга так трудно справиться
Глиобластома — один из самых смертельных видов рака мозга, и даже при хирургии, облучении и химиотерапии лишь небольшая часть пациентов живёт более пяти лет. Одна из причин в том, что эти опухоли состоят не из одного типа клеток. В них есть небольшая группа особенно устойчивых «раковых стволовых» клеток, которые могут пережить лечение и способствовать рецидиву. В этом исследовании поставлен ключевой вопрос: как разные клетки опухоли реагируют на блокирование сигнала, стимулирующего рост, и как присутствие нормальных поддерживающих клеток мозга — астроцитов — меняет эту реакцию?
Более пристальный взгляд на самые стойкие клетки опухоли
Исследователи работали с двумя основными типами клеток из распространённой модели глиобластомы: массовыми опухолевыми клетками и маленькой субпопуляцией, отмеченной белком CD133, которая ведёт себя как раковые стволовые клетки. Эти стволоподобные клетки делились реже, выглядели меньше и круглее и формировали более плотные скопления, чем массовые клетки. Команда также выращивала опухолевые клетки вместе с астроцитами — звездообразными клетками, поддерживающими здоровье мозговой ткани. Такая смешанная культура лучше имитирует реальное опухолевое окружение, где клетки постоянно «общаются» с соседями. 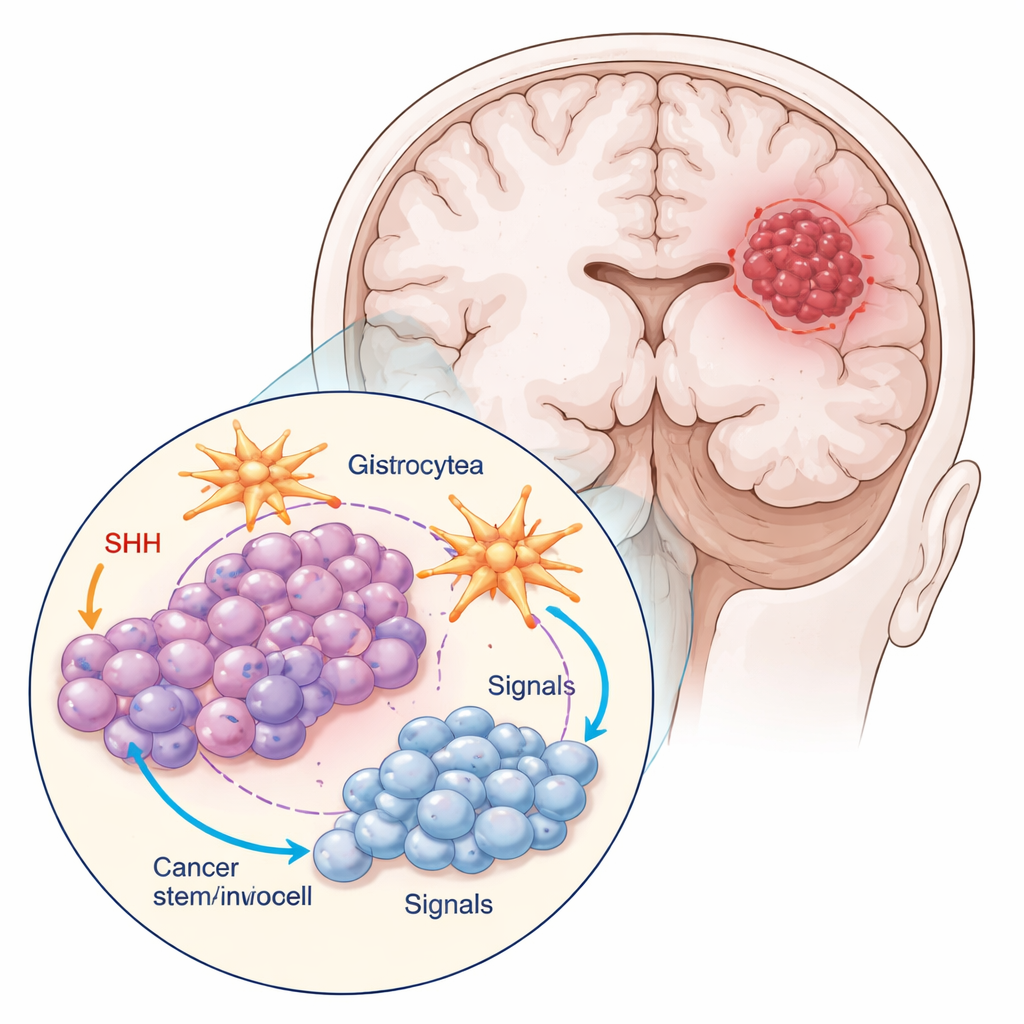
Блокирование эмбрионального сигнала, который опухоли используют повторно
Многие глиобластомы, особенно их стволоподобные клетки, захватывают молекулярный путь коммуникации под названием Sonic Hedgehog (SHH), который обычно активен во время развития мозга. Команда использовала циклопамина — соединение, блокирующее ключевой компонент SHH — чтобы посмотреть, как реагируют массовые опухолевые клетки и раковые стволовые клетки. Они измеряли активность генов и белков, связанных с SHH, скорость прохождения клеточного цикла и частоту программируемой гибели клеток (апоптоза). Циклопамин изменял SHH‑сигналинг в зависимости от типа клеток и от присутствия астроцитов. Раковые стволовые клетки выделяли наибольший SHH‑сигнал в культуре отдельно, но эта секреция уменьшалась при совместном выращивании с астроцитами и при воздействии препарата, что указывает на то, что окружающие клетки мозга могут ослаблять химическую «самоподдержку» опухоли.
Как окружение сдвигает баланс роста и гибели
Кроме самого SHH, команда отслеживала и другие генетические сети, которые определяют, будут ли клетки продолжать делиться, приостановят цикл или начнут специализацию. В простых культурах, содержащих только опухолевые клетки, блокада SHH вызывала у массовых клеток остановку на поздней фазе деления (G2/M), тогда как стволоподобные клетки накапливались в более ранней фазе покоя или входа в цикл (G0/G1). При добавлении астроцитов эти паттерны менялись: раковые стволовые клетки, которые раньше были более покоящимися, сдвигались к аресту в G2/M, что предполагает включение другого набора «тормозов» в смешанном окружении. Исследователи также обнаружили, что сигналы, связанные с судьбой клетки и формированием тканей — такие как пути WNT, BMP и TGF‑β — по‑разному настраивались в массовых и стволоподобных клетках при наличии астроцитов, что означает: микроокружение может склонять клетки либо к сохранению стволоподобного поведения, либо к более дифференцированному, менее агрессивному состоянию.
Индуцирование гибели в самых устойчивых клетках
В исследовании также оценивали готовность клеток к апоптозу. Генетические показатели и тест на распознавание повреждений ДНК (TUNEL‑анализ) показали, что циклопамин способствовал «внешнему» пути гибели клеток, опосредованному белком CASP8, особенно в популяции раковых стволовых клеток. Интересно, что в опухолевых клетках, выращенных отдельно, общая смертность иногда снижалась после блокады SHH, что говорит о том, что эти клетки могут включать запасные стратегии выживания. Напротив, когда стволоподобные клетки ко‑культивировали с астроцитами, циклопамин увеличивал маркеры апоптоза, указывая на то, что окружающие клетки мозга делают эти в противном случае упорные клетки более уязвимыми при подавлении SHH‑сигналинга. 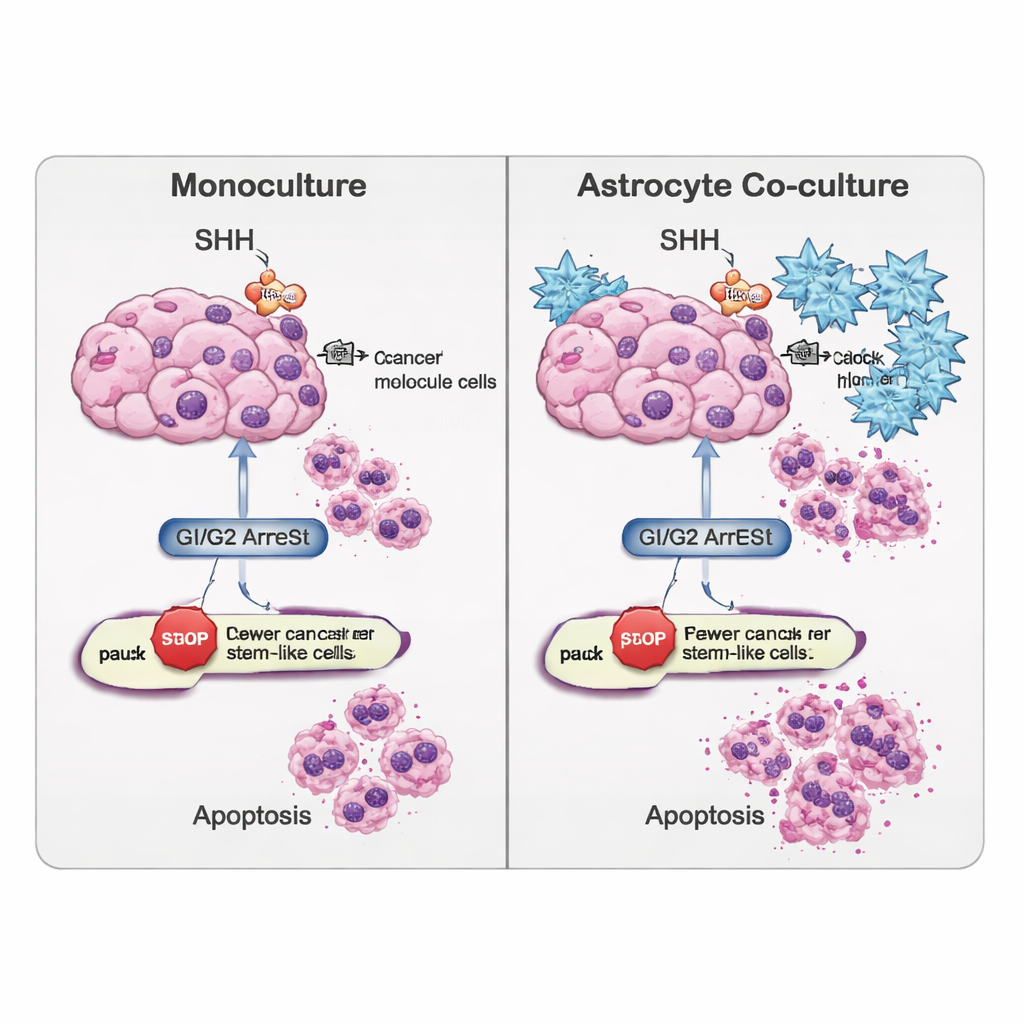
Что это значит для будущих методов лечения рака мозга
Для неспециалиста ключевая мысль такова: нацеливание на один ростовой сигнал в глиобластоме недостаточно, если игнорировать окружение опухоли. Эта работа показывает, что астроциты — нормальные клетки, соседствующие с опухолью — могут глубоко изменить реакцию как массовых раковых клеток, так и раковых стволовых клеток на блокаду пути SHH. В частности, раковые стволовые клетки становились более склонными к остановке клеточного цикла и к форме гибели клеток в присутствии астроцитов. Авторы делают вывод, что препараты, нацеленные на SHH и связанные пути, с большей вероятностью будут эффективны, если их тестировать и применять с учётом реального мозгового окружения, возможно в комбинации с другими методами лечения, направленными на запасные пути выживания опухоли. Короче говоря, понимание и использование «диалога» между опухолевыми клетками и их соседями может открыть более точные и стойкие стратегии против этой в остальном неумолимой болезни.
Цитирование: Kocaturk, D.C., Ozdil, B., Adali, Y. et al. SHH pathway inhibition and astrocyte co-culture induce distinct responses in glioblastoma and cancer stem cells. Sci Rep 16, 7712 (2026). https://doi.org/10.1038/s41598-026-38199-y
Ключевые слова: глиобластома, раковые стволовые клетки, путь Sonic Hedgehog, опухолевый микроокружение, астроциты