Clear Sky Science · ru
Модель гипоксического мышиного шкурного синдрома (tight‑skin) для изучения легочной гипертензии группы 3
Почему это исследование важно
Легочная гипертензия — это серьезное, часто фатальное повышение давления крови в легких. Одна из её наиболее распространённых форм, называемая легочной гипертензией группы 3, развивается у людей с хроническими заболеваниями легких, такими как эмфизема или легочный фиброз, либо у тех, кто длительно подвергается низкому уровню кислорода. При этом у врачей до сих пор нет целевых препаратов для этого состояния, отчасти потому, что учёным не хватало животной модели, которая бы правдоподобно воспроизводила процессы в человеческих легких. В этом исследовании представлена новая мышиная модель, близкая к патологии группы 3, и обнаружена вредоносная сигнальная цепочка, которую можно было бы в будущем блокировать терапевтически.
Мышь, имитирующая повреждённые легкие
Исследователи сосредоточились на штамме мышей, известном как «tight‑skin» (Tsk). Эти животные несут мутацию в структурном белке фибриллин‑1. Из‑за этого дефекта у них естественным образом развиваются изменения, похожие на эмфизему, и рубцевание в легких, подобно тому, что наблюдается при тяжёлых хронических заболеваниях легких у людей. Команда сравнивала этих мышей с нормальными сибсами, содержая их либо в обычном воздухе, либо в условиях низкой концентрации кислорода в течение четырёх недель, чтобы имитировать хронический дефицит кислорода, с которым сталкиваются многие пациенты. 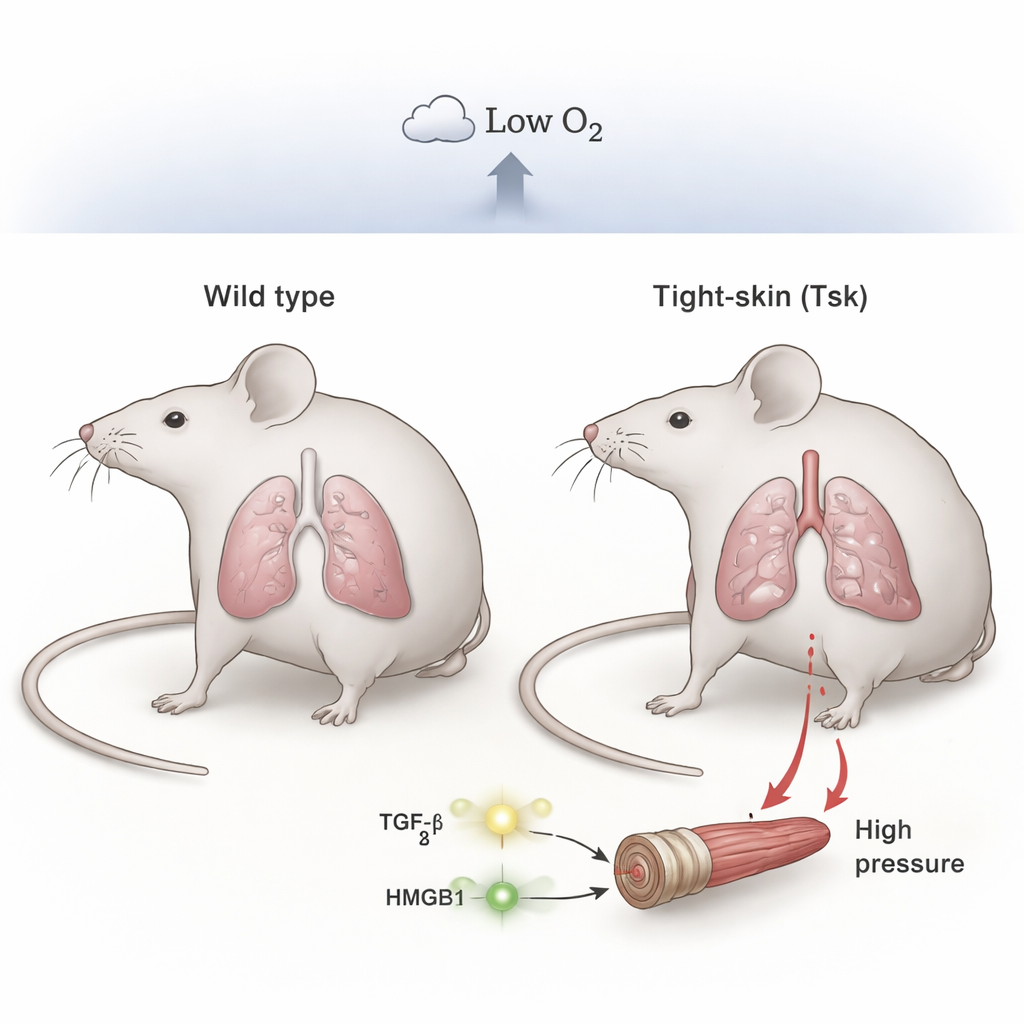
Гипоксия превращает уязвимые легкие в легкие с высоким давлением
Когда и нормальные, и tight‑skin мыши содержались в комнатном воздухе, давление крови в их легких было схожим и находилось в пределах нормы. Но при хронической гипоксии различия оказались поразительными. У нормальных мышей наблюдалось лишь умеренное повышение давления, тогда как у tight‑skin животных развилась тяжёлая легочная гипертензия с существенно повышенным давлением в правых отделах сердца и явным утолщением мелких артерий легких. Микроскопия показала расширенные альвеолярные пространства (эмфизему) и выраженную мускуляризацию мельчайших сосудов у tight‑skin мышей, что тесно соответствовало структурным повреждениям, видимым у больных с группой 3. Это указывает на то, что предварительное повреждение легких в сочетании с гипоксией переводит систему в более опасное состояние, чем одна только гипоксия.
Сигнал опасности в крови
Команда затем задалась вопросом, почему tight‑skin мыши так резко реагируют на низкий уровень кислорода. Они сосредоточились на молекуле HMGB1 — «сигнале опасности», белке, выделяемом стрессированными или повреждёнными клетками. У tight‑skin мышей уже в исходных условиях были повышенные уровни HMGB1 в крови, и при гипоксии эти уровни ещё увеличивались. Введение мышам небольшого пептидного препарата P5779, блокирующего взаимодействие HMGB1 с одним из его ключевых рецепторов (TLR4), в значительной степени предотвращало развитие тяжёлой легочной гипертензии у tight‑skin мышей. Лечёные животные имели более низкое давление в легких, меньшее утолщение сосудов и уменьшенное увеличение правых отделов сердца. Эти защитные эффекты были гораздо более выражены у tight‑skin мышей, чем у нормальных, что указывает на HMGB1 как на центральный усилитель болезни в этой модели.
Как фактор роста подпитывает сигнал опасности
Другим участником этой истории оказался TGF‑β — фактор роста, давно связанный с образованием рубцов и ремоделированием в больных легких. Исследователи обнаружили, что у tight‑skin мышей в легких в исходе была более высокая активность TGF‑β, что проявлялось повышенной активацией его сигнального посредника, SMAD‑3, вокруг кровеносных сосудов. В экспериментах с человеческими адвентициальными фибробластами легочной артерии — клетками, выстилающими наружный слой сосудов — добавление TGF‑β усиливало выработку HMGB1. В свою очередь, HMGB1 вызывал пролиферацию как этих фибробластов, так и соседних гладкомышечных клеток. Важно, что этот рост зависел от рецептора TLR4 и блокировался P5779, но не блокировался при ингибировании другого рецептора HMGB1, называемого RAGE. В сумме эти находки описывают петлю, в которой мутантный фибриллин‑1 способствует активации TGF‑β, TGF‑β повышает уровни HMGB1, а HMGB1 стимулирует чрезмерный рост клеток стенки сосуда, сужая легочные артерии. 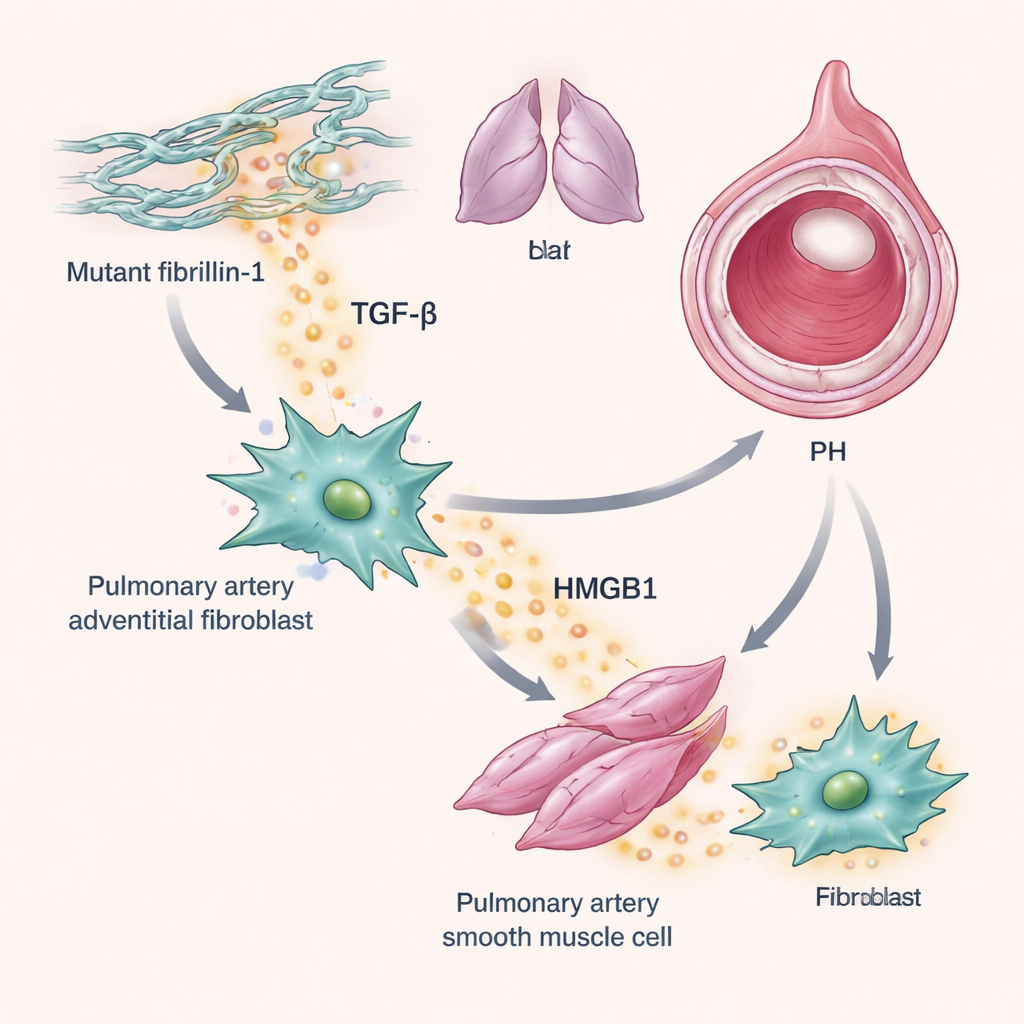
Последствия для пациентов
Комбинируя структуру легких, сходную с эмфиземой, и хроническую гипоксию, модель tight‑skin воспроизводит многие ключевые черты легочной гипертензии группы 3, которые упускают более простые модели, основанные только на гипоксии. Работа выделяет путь TGF‑β–HMGB1–TLR4, который превращает повреждённые, испытывающие дефицит кислорода легкие в легкие с высоким давлением. Для людей с хроническими заболеваниями легких это исследование предполагает новые терапевтические подходы: препараты, ослабляющие сигнализацию TGF‑β, или блокирующие взаимодействие HMGB1 с TLR4, подобно действию P5779 у мышей, могут в будущем помочь предотвратить или замедлить повышение давления в легочных сосудах. Сама модель также предлагает мощную платформу для тестирования таких вмешательств до их перехода в клинику.
Цитирование: Chi, L., Foley, A.E., Goodarzi, G. et al. The hypoxic tight-skin mouse model of Group 3 pulmonary hypertension. Sci Rep 16, 6968 (2026). https://doi.org/10.1038/s41598-026-38174-7
Ключевые слова: легочная гипертензия, хроническое заболевание легких, гипоксия, HMGB1, TGF-beta