Clear Sky Science · ru
Наночастицы из бычьего сывороточного альбумина улучшают стабильность бактериофагов и их антимикробную активность против Pseudomonas aeruginosa
Почему важно защищать полезные вирусы
По мере роста устойчивости к антибиотикам врачам становится всё труднее лечить опасные инфекции. Одним из упрямых возбудителей является Pseudomonas aeruginosa — бактерия, которая часто поражает легкие людей со сниженным иммунитетом и может противостоять множеству препаратов. В этом исследовании рассматривается креативный подход: использование «дружественных» вирусов, атакующих бактерии — бактериофагов — и защита их внутри крошечных белковых шариков, изготовленных из распространённого плазменного белка бычьего сывороточного альбумина (BSA). Цель — сохранить эти вирусы стабильными и активными достаточно долго, чтобы эффективнее бороться с тяжёлыми легочными инфекциями.
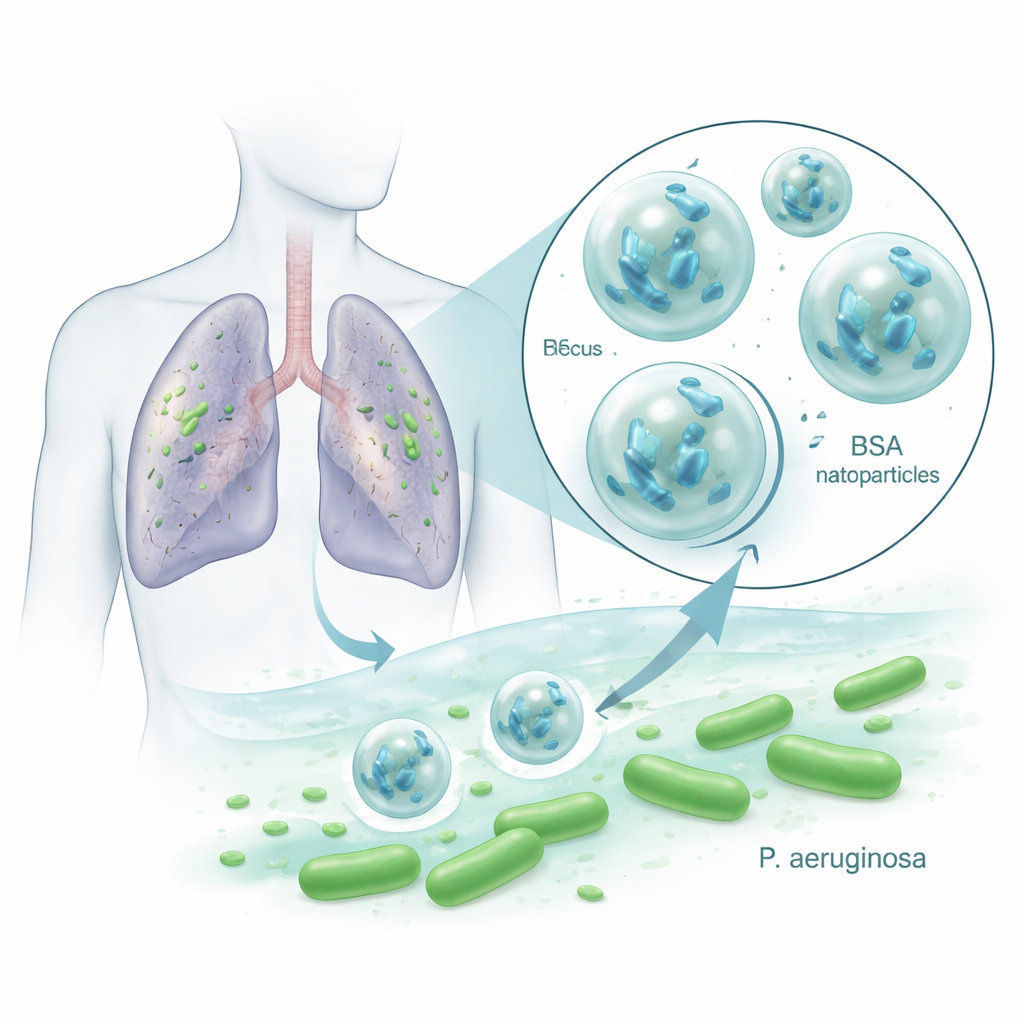
Маленькие союзники против стойких легочных микроорганизмов
Pseudomonas aeruginosa печально известна в больницах из‑за множественной устойчивости к антибиотикам и способности образовывать слизистые биопленки, защищающие её от лечения. Бактериофаги, или фаги, — это вирусы, инфицирующие и разрушивающие определённые бактерии, при этом человеческие клетки и полезная микрофлора в основном остаются нетронутыми. Они способны размножаться там, где присутствует их бактериальный хозяин, что делает их привлекательным дополнением или альтернативой антибиотикам. Но фаги хрупки: тепло, кислота, ферменты и иммунная система быстро инактивируют их, что ограничивало их успех в клинике. Исследователи задали вопрос, сможет ли упаковка фага, убивающего Pseudomonas и названного VAC1, внутри наночастиц BSA защитить его и повысить эффективность лечения.
Создание защитной белковой оболочки
Команде сначала нужно было разработать частицу, не повреждающую фаг. Они протестировали обычные растворители, используемые для формирования наночастиц BSA, и обнаружили, что этанол и метанол разрушали VAC1, тогда как ацетон не повреждал его — поэтому в процессе использовали ацетон. Фага смешивали с раствором BSA и затем осторожно добавляли ацетон, заставляя белок слипаться в наноскопические сферы и стабилизируя их с помощью сшивающего вещества. Эти частицы, загруженные фагом и названные NPPha, в среднем имели диаметр около 220 нанометров — намного меньше человеческой клетки — и удерживали более 95% фага внутри. Снимки электронного микроскопа показали неправильной формы частицы BSA с более плотными участками, которые, вероятно, соответствовали фагам, а тесты подтвердили, что активные вирусы медленно высвобождаются как минимум в течение двух дней при температуре тела, не теряя инфективности.
Усиленная бактерицидная активность в лаборатории
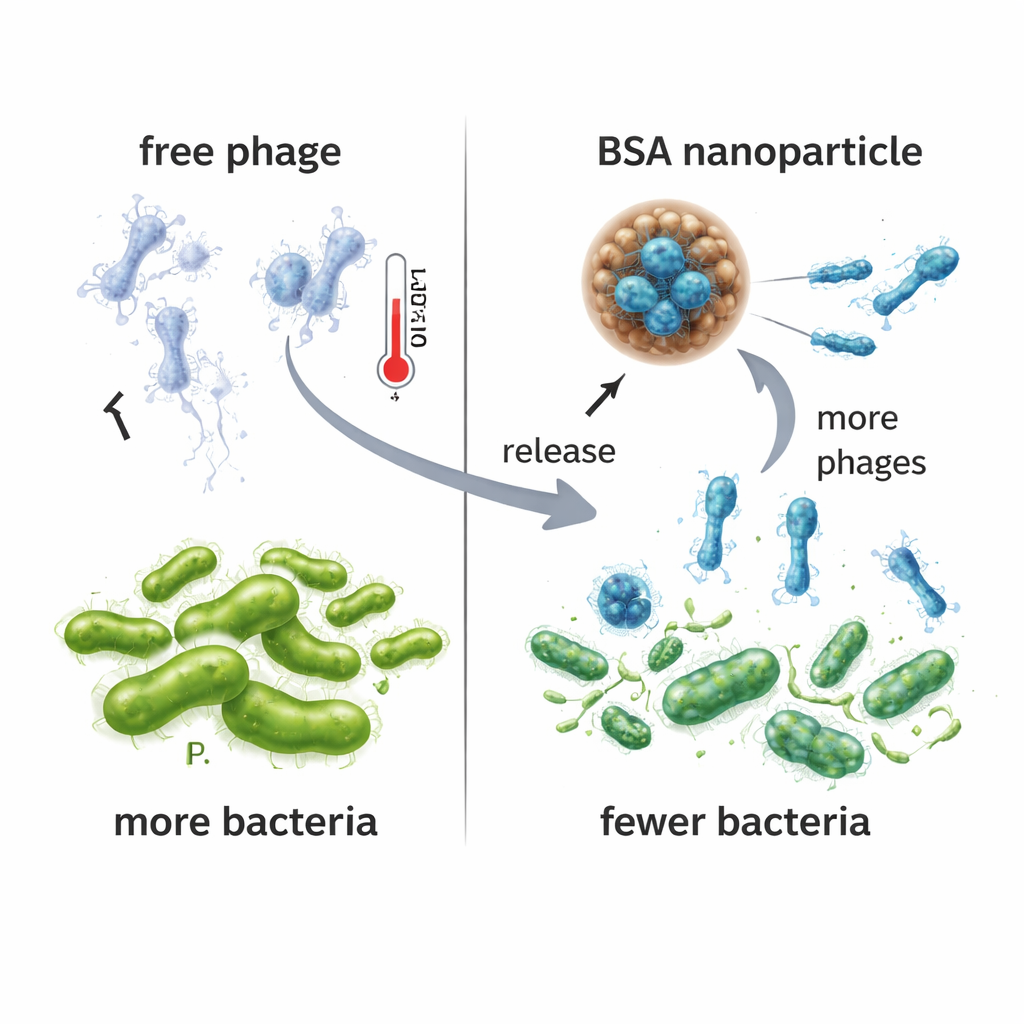
Затем исследователи сравнили, насколько свободный VAC1 и NPPha контролировали Pseudomonas в жидкой культуре. При воздействии NPPha рост бактерий подавлялся значительно сильнее, чем при той же дозе свободного фага или при применении пустых наночастиц. В течение 24 часов культуры, обработанные NPPha, дали примерно в сто тысяч раз больше новых фаговых частиц, чем культуры с свободным VAC1, что указывает на то, что постепенное высвобождение из наночастиц обеспечивало более устойчивую «битву» между вирусом и бактерией. Важно, что наночастицы BSA — как с фагом, так и пустые — не вредили клеткам человека, происходящим из печени, в тестах на токсичность, что поддерживает их потенциальную безопасность как носителя. Эксперименты по стабильности при 37 °C показали, что свободный фаг быстро терял активность в течение двух дней, тогда как фаг внутри NPPha оставался инфекционным до пяти дней.
Испытание подхода на инфицированных мышах
Чтобы проверить, переносятся ли эти преимущества на живых животных, команда использовала модель острой пневмонии у мышей, вызванной Pseudomonas. Мышей инфицировали через нос, а через час лечили NPPha, свободным VAC1, пустыми наночастицами или солевым раствором. В этой очень тяжёлой модели все животные, независимо от лечения, погибли в течение 12 часов, поэтому выживаемость не улучшилась. Однако при исследовании лёгких выяснилось, что у мышей, получавших NPPha, было меньше бактерий и чаще обнаруживался фаг по сравнению с теми, кто получал свободный VAC1. Тонкие срезы тканей лёгких от животных, леченных NPPha, показали меньше структурных повреждений, более тонкие перегородки между альвеолами и уменьшенное скопление воспалительных клеток по сравнению с другими инфицированными группами, что указывает на то, что инфекция была в некоторой степени ослаблена, хотя этого оказалось недостаточно, чтобы спасти животных в этих суровых условиях.
Что это значит для будущего лечения инфекций
Для неспециалистов ключевая мысль такова: упаковка бактериофагов в крошечные белковые «пузырьки» помогает сохранять их живыми и действенными дольше, что повышает их способность атаковать трудноизлечимые бактерии, такие как Pseudomonas aeruginosa. В пробирках и в лёгких мышей наночастицы BSA увеличивали количество фагов, сокращали бактериальный рост и уменьшали повреждение лёгких, хотя пока не обеспечили спасения при крайне агрессивной модели инфекции. Работа указывает на то, что альбуминовые наночастицы предлагают простой, недорогой и, по-видимому, безопасный способ стабилизации терапевтических фагов. При оптимизации дозировки, времени введения и, возможно, применении в менее тяжёлых или более хронических инфекциях такие фаги в наноупаковке могли бы стать ценным инструментом наряду с антибиотиками в борьбе с мультирезистентными бактериями.
Цитирование: Cunha, G.A.d., Marangoni, G.S., Durante, M.F.R. et al. Bovine serum albumin nanoparticles improve bacteriophage stability and antimicrobial activity against Pseudomonas aeruginosa. Sci Rep 16, 7146 (2026). https://doi.org/10.1038/s41598-026-38106-5
Ключевые слова: фаговая терапия, наночастицы, Pseudomonas aeruginosa, антибиотикорезистентность, инфекция легких