Clear Sky Science · ru
Обинутузумаб вызывает дестабилизацию лизосом через сфингомиелин‑зависимое ингибирование TRPML2
Почему эта история об антителе важна
Для многих пациентов с В‑клеточными лимфомами современные препараты на основе антител превратили ранее почти всегда смертельный диагноз в заболевание, поддающееся лечению. Однако не все антитела одинаковы: одни убивают раковые клетки мощнее и надежнее, чем другие. В этой работе исследуют, почему одно из таких лекарств, обинутузумаб, эффективнее вызывает прямую гибель клеток лимфомы по сравнению с предшественником ритуксимабом, сосредоточив внимание на неожиданном виновнике глубоко внутри клетки — собственных центрах утилизации клетки, лизосомах, и тонком балансе липидов и ионных каналов в их мембранах.
От поверхностной мишени к внутреннему самоуничтожению
И ритуксимаб, и обинутузумаб распознают одну и ту же мишень на В‑клетках — белок CD20. Авторы показывают, что обинутузумаб захватывается в клетку значительно быстрее и эффективнее. Связавшись с CD20 на поверхности раковой клетки, комплексы «антитело‑рецептор» втягиваются внутрь посредством эндоцитоза и доставляются в кислотные компартменты, включая лизосомы. Там обинутузумаб вызывает проницаемость лизосомальной мембраны: обычно прочная мембрана становится течной, позволяя таким пищеварительным ферментам, как катепсины, выливаться в клетку и запускать пути клеточной гибели. Изменения солевого и водного баланса в этих компартментах, которые приводят к набуханию лизосом, сильно усиливают этот губительный эффект.
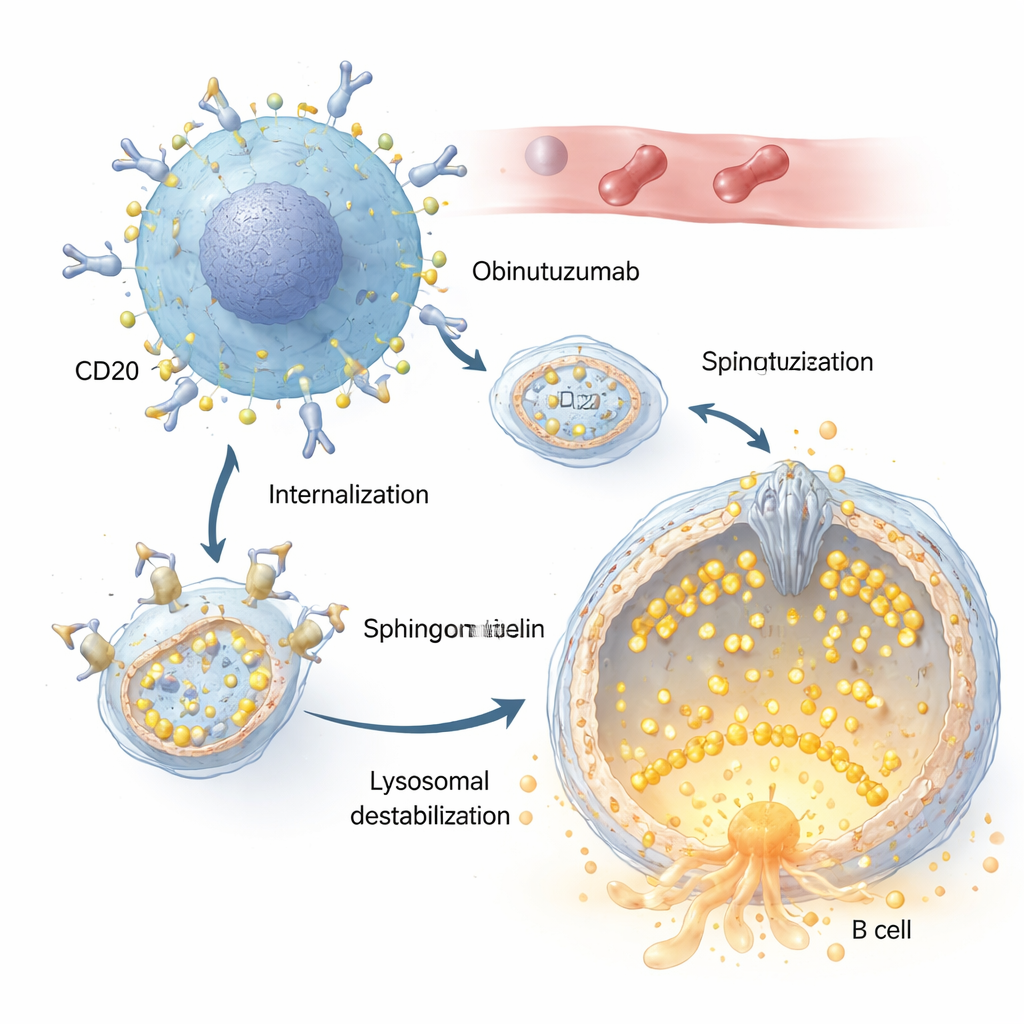
Роль крошечного сторожевого канала
Ключевым в этой истории является TRPML2 — кальциевый канал, встроенный в лизосомальную мембрану. В норме TRPML2 помогает лизосомам справляться с механическим и осмотическим стрессом, высвобождая кальций, что поддерживает ремонт мембран, транспорт и контроль объема. С помощью комбинации флуоресцентных красителей для кальция и инженерных версий TRPML2 с чувствительностью к кальцию исследователи показывают, что обинутузумаб быстро выключает этот канал: в течение нескольких минут после лечения вещество, которое обычно открывает канал TRPML, больше не вызывает всплеска кальция. Генетические подходы, уменьшающие уровень TRPML2, или малые молекулы‑ингибиторы, блокирующие активность TRPML, делают клетки лимфомы более уязвимыми к обинутузумабу, что приводит к большему утечению лизосом и повышенной частоте прямой гибели клеток.
Как липиды мембраны меняют баланс
Далее в работе рассматривают, что связывает захват антитела и отключение канала. Внимание обращают на сфингомиелин — липид, обильный в клеточных мембранах и известный своим влиянием на каналы TRPML. С помощью флуоресцентного зонда, связывающего сфингомиелин, авторы обнаруживают, что везикулы, содержащие обинутузумаб, богаты сфингомиелином, когда достигают кислотных компартментов, намного больше, чем везикулы с ритуксимабом. Если клетки обрабатывают сфингомиелиназой — ферментом, расщепляющим сфингомиелин — активность TRPML2 по высвобождению кальция восстанавливается даже в присутствии обинутузумаба. В этих условиях лизосомы реже протекают, и умирает меньше клеток, что сильно указывает на то, что накопление сфингомиелина подавляет TRPML2 и готовит лизосомы к разрыву.
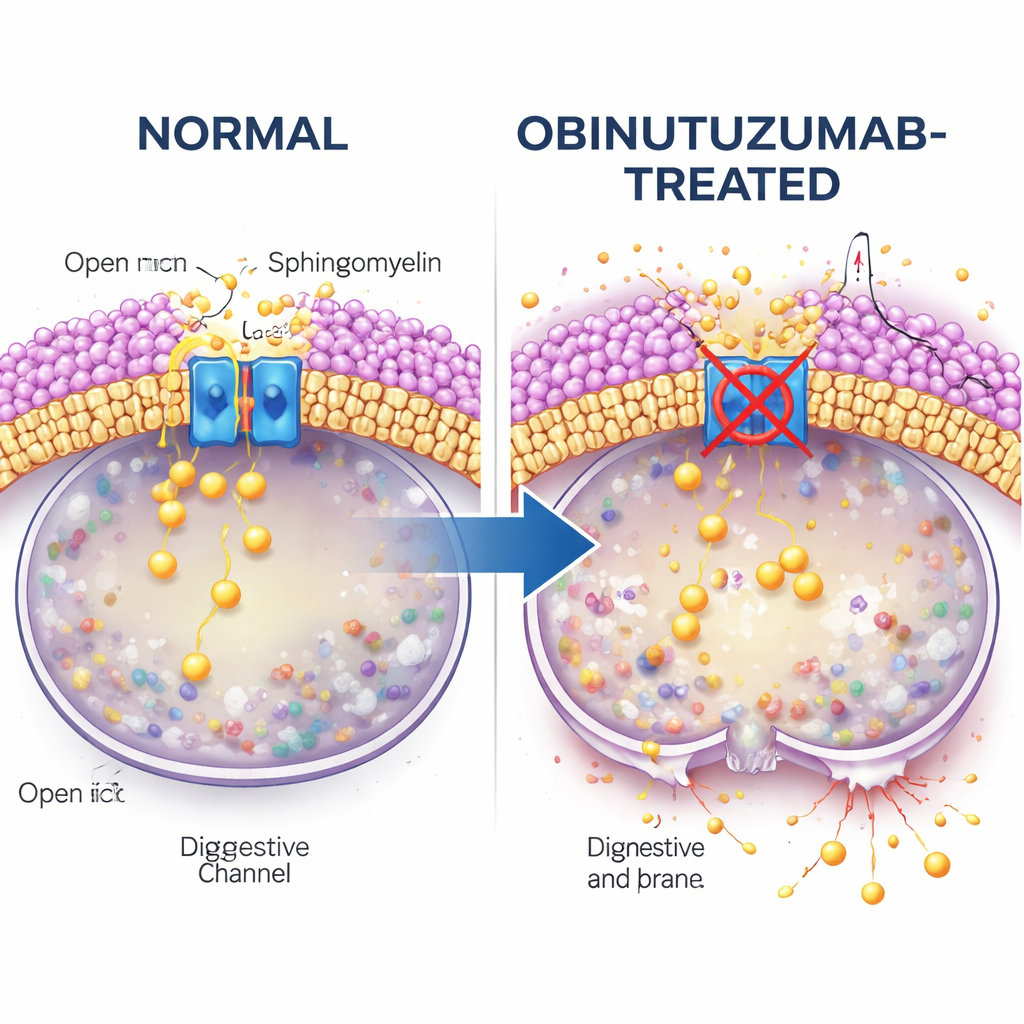
Маршруты транспорта и холестериновые контрольные точки
Важен также путь, по которому обинутузумаб попадает в клетку. Электронная микроскопия и метки антител, чувствительные к pH, показывают, что обинутузумаб быстрее покидает поверхность клетки и входит в внутриклеточные везикулы, чем ритуксимаб. При вмешательстве в определенные пути захвата исследователи обнаруживают, что блокирование холестерин‑зависимой формы эндоцитоза (с помощью вещества филипина) предотвращает выключение TRPML2 обинутузумабом и частично уменьшает повреждение лизосом и гибель клеток. Другие ингибиторы эндоцитоза не дают такого защитного эффекта. Это указывает на специализированный путь, богатый холестерином и сфингомиелином, который доставляет обинутузумаб в лизосомы таким образом, что возникает ингибирование TRPML2 и последующая дестабилизация мембран.
Что это значит для будущих противораковых терапий
Проще говоря, эта работа показывает, что обинутузумаб так эффективно уничтожает В‑клеточные лимфомы, потому что он переводит их лизосомы в хрупкое состояние. Направляя комплексы антитело–CD20 в сфингомиелин‑богатые компартменты, препарат косвенно выключает защитный кальциевый канал TRPML2. Как только эта защита исчезает, лизосомы с большей вероятностью лопаются под нагрузкой, выпуская коррозионные ферменты, которые разрушают раковую клетку изнутри. Понимание этой оси «липид — ионный канал» не только объясняет, почему обинутузумаб превосходит ритуксимаб, но и предлагает новые стратегии усиления антительного лечения — например, комбинирование с препаратами, меняющими сфинголипиды или повышающими активность TRPML2, чтобы тонко регулировать, как и когда лизосомы опухолевых клеток подвергаются самоуничтожению.
Цитирование: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
Ключевые слова: обинутузумаб, В‑клеточная лимфома, лизосома, сфингомиелин, TRPML2