Clear Sky Science · ru
Создание полиэтиленимин–металлофункционализированных криогелей для улучшенного связывания каталазы, активности и долговременной прочности
Почему важно фиксировать ферменты на месте
Перекись водорода — распространённый побочный продукт в таких областях, как пищевая переработка и медицинские процедуры, а живые клетки используют фермент каталазу для её разложения до безвредной воды и кислорода. В промышленности каталаза обычно применяется в растворённой форме: она быстро теряет активность, её трудно восстановить и приходится часто заменять. В этом исследовании рассматривается способ «припарковать» каталазу внутри губкообразного материала, чтобы она дольше сохраняла активность, могла многократно использоваться и работала эффективнее — все это потенциально уменьшит затраты и сделает ферментные процессы более чистыми и устойчивыми.

Создание «умной» губки
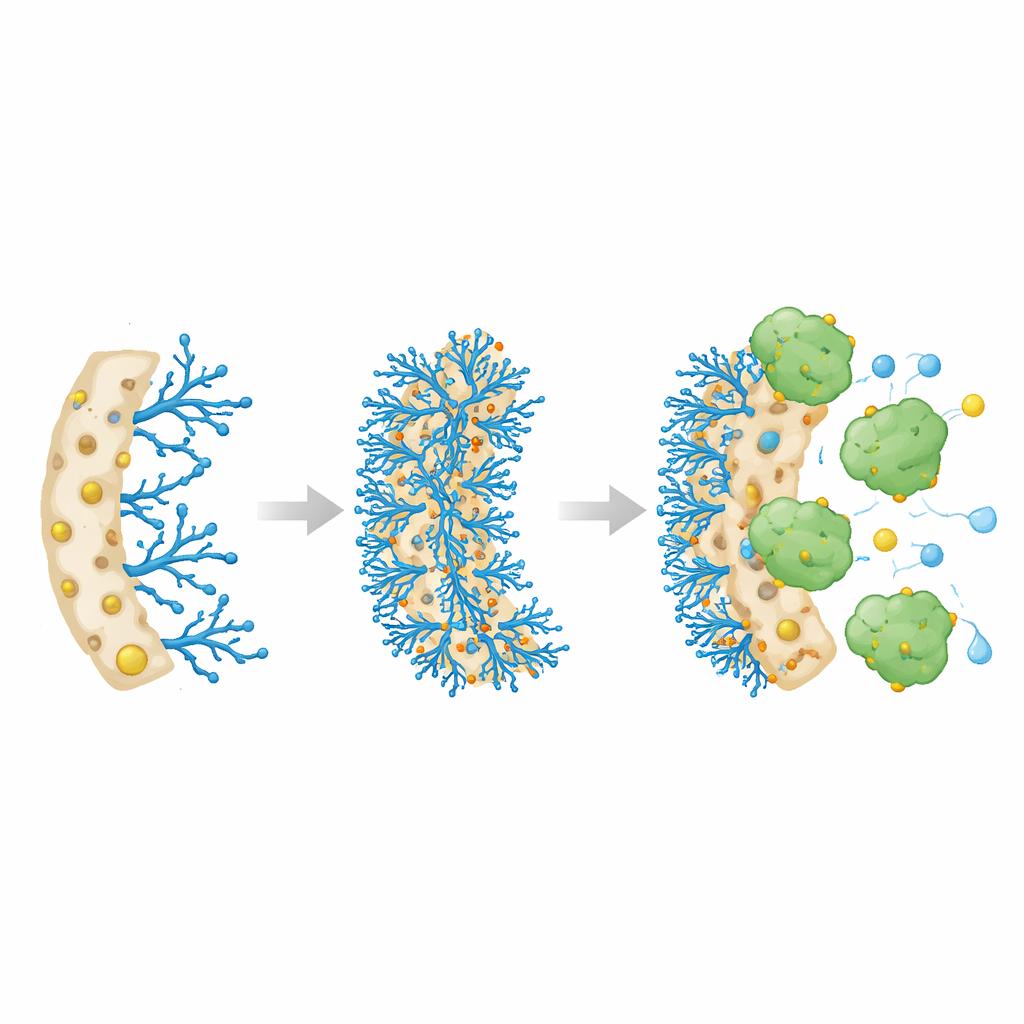
Исследователи разработали специальную полимерную губку — криогель, формируемую посредством замораживания и оттаивания жидкой смеси, при котором кристаллы льда вырезают крупные взаимосвязанные поры. Эти поры обеспечивают свободный поток жидкости, как вода через мочалку, в то время как твёрдый каркас остаётся прочным и эластичным. В качестве основы использовали материал Poly(HEMA-co-GMA), на который затем химически прирастили разветвлённую молекулу, богатую азотсодержащими группами — полиэтиленимин (PEI). Наконец, к этим азотным участкам присоединили ионы металлов — меди, никеля или кобальта. Идея состояла в том, что ионы металлов будут действовать как док-пойнты, которые сильно притягивают и удерживают молекулы каталазы, не препятствуя при этом потоку жидкости через губку.
Настройка материала для лучшей работы
Чтобы понять, как каждый этап модификации влияет на материал, команда использовала несколько лабораторных методов для исследования его структуры, химии и стабильности. Они показали, что добавление PEI, а затем металлов не разрушило пористую сеть, а на самом деле увеличило способность губки удерживать воду, что полезно для поддержания активности ферментов. Среди трёх металлов медь создала наиболее гидратированную и упорядоченную среду. Микроскопические изображения показали, что исходный материал выглядел как упакованные зерна, тогда как версии, обработанные PEI и металлами, раскрылись в более чистую, непрерывную сеть крупных пор. Измерения содержания металлов подтвердили, что медь связывается сильнее и в больших количествах, чем никель или кобальт, что указывает на её большую эффективность как док-площадок для каталазы.
Фиксация каталазы на месте
Когда каталаза вводилась в разные металлические губки, все три быстро захватывали фермент, но версия с медью выделялась. Она загрузила наибольшее количество каталазы — около 392 миллиграммов на грамм сухой губки — и достигла равновесного состояния примерно за восемь часов. Затем исследователи оценили работу иммобилизованного фермента по сравнению со свободной каталазой в растворе. Хотя максимальная скорость реакции на грамм фермента несколько снизилась, иммобилизованная каталаза продемонстрировала существенно более сильную кажущуюся аффинность к своему субстрату, перекиси водорода. Практически это означает, что связанный фермент эффективнее работает при более низких концентрациях субстрата, вероятно потому, что пористая, наполненная водой медная губка концентрировала субстрат возле фермента и помогала поддерживать его активную конформацию.
Фермент, который выдерживает испытание временем
Одно из главных преимуществ иммобилизации ферментов — возможность многократного использования и длительного хранения. Здесь каталаза, прикреплённая к криогелю на основе меди, оказалась значительно более прочной, чем её свободный аналог. После 15 повторных циклов использования иммобилизованный фермент сохранял около трети первоначальной активности, тогда как свободную каталазу обычно выбрасывают после однократного применения. В тестах хранения при температуре холодильника в течение 70 дней иммобилизованная каталаза сохраняла более 60% активности, примерно вдвое больше, чем свободный фермент. Губка также позволяла отщеплять и вновь загружать фермент несколько раз с помощью простого солевого раствора, что показывает: сам материал можно повторно использовать без значительной потери ёмкости.
Что это значит для практического применения
Для неспециалиста главный вывод таков: исследователи создали своего рода многоразовую «ферментную губку», которая надёжно, но мягко удерживает каталазу, помогая ей работать лучше при низких концентрациях реагентов и служить значительно дольше в работе и при хранении. Сочетая высокопористый криогель с PEI и ионами меди, они получили платформу с высокой загрузкой фермента, улучшенной эффективностью и сильной долговременной стабильностью. Такие материалы можно интегрировать в промышленные или экологические системы для более надёжного разложения перекиси водорода и родственных веществ с меньшими отходами, что представляет собой практический шаг к более «зелёным», ферментно-опосредованным технологиям.
Цитирование: Erol, K., Alkan, M.H. & Alacabey, İ. Engineering polyethylenimine–metal functionalized cryogels for superior catalase binding, activity, and long-term durability. Sci Rep 16, 7880 (2026). https://doi.org/10.1038/s41598-026-38040-6
Ключевые слова: иммобилизация ферментов, каталаза, криогель, полимеры, функционализированные медью, биокатализ