Clear Sky Science · ru
Инструмент для прогнозирования влияния pH и температуры на активность пепсина свиней и человека при in vitro желудочном переваривании
Почему ферменты желудка важны для повседневного питания
Каждый раз, когда мы едим, мощные ферменты в желудке начинают расщеплять пищевые белки на более мелкие фрагменты, которые организм может использовать. Один из важнейших таких ферментов — пепсин. Пищевые исследователи часто используют свиной вариант пепсина в лабораторных тестах вместо человеческого, предполагая, что они ведут себя примерно одинаково. В этом исследовании задан простейший, но ключевой вопрос: при меняющихся условиях в реальном желудке — где одновременно колеблются и кислотность (pH), и температура — действительно ли человеческий и свиной пепсин действуют одинаково и как предсказать их поведение?
Как меняющиеся условия в желудке формируют процесс переваривания
Внутри желудка pH и температура далеки от постоянства. Холодный напиток может временно охладить желудок более чем на 10 градусов, а большой или щелочной приём пищи может повысить pH на несколько единиц, прежде чем он медленно вернётся к более кислотному состоянию. Поскольку способность пепсина расщеплять белки сильно зависит как от кислотности, так и от температуры, эти колебания могут ускорять или замедлять переваривание. Непросто отслеживать это прямо у людей, поэтому исследователи опираются на in vitro модели — тщательно контролируемые лабораторные имитации переваривания. В этих моделях обычно используют поросий пепсин в качестве аналога человеческого, но до сих пор учёным не хватало ясной карты того, как оба фермента реагируют при одновременных изменениях pH и температуры, как это происходит после приёма пищи.
Измерение активности пепсина в многочисленных условиях
Авторы проверяли человеческий пепсин, выделенный из желудочного сока, и коммерческий свиной пепсин в 37 комбинациях pH (от сильно кислого до почти нейтрального) и температуры (от холодильной до довольно высокой). Затем они использовали эти измерения для построения математических моделей, способных предсказывать активность каждого фермента при любой комбинации кислотности и температуры, приближённой к желудочным условиям. Оба фермента действовали лучше всего около pH 2 и при температуре тела, но человеческий вариант сохранял активность в более широком интервале. При pH 3 и 4 человеческий пепсин по‑прежнему сохранял значительную активность, тогда как активность свиного пепсина резко падала. Интересно, что хотя порокий пепсин был мощнее в своей «зоне комфорта», он оказался гораздо чувствительнее к изменениям pH, то есть его работа может быстрее снижаться по мере ухода условий от оптимальных.
Что позволяет новый инструмент прогнозирования
Преобразовав эти измерения в удобные уравнения, встраиваемые в таблицы, исследователи создали способ для коллег оценивать активность пепсина в лабораторных экспериментах по перевариванию. Они провели несколько примеров использования, чтобы показать возможности инструмента. В полудинамической модели переваривания молока смоделированные человеческий и свиной пепсин показали схожие общие шаблоны, но человеческий пепсин дольше сохранял полезную активность по мере сдвига pH, что приводило к большей общей «площади под кривой» активности во времени. Инструмент также сравнил традиционные статические экспериментальные схемы — где pH удерживается постоянным — с полудинамическими, которые постепенно подкисляют среду, и смоделировал, как активность пепсина может отличаться у молодых и пожилых взрослых, у которых обычно секретируется меньше пепсина. Эти примеры подчёркивают, что одна и та же пища и тот же протокол могут приводить к разным уровням разрушения белков в зависимости от типа фермента и используемой модели переваривания.
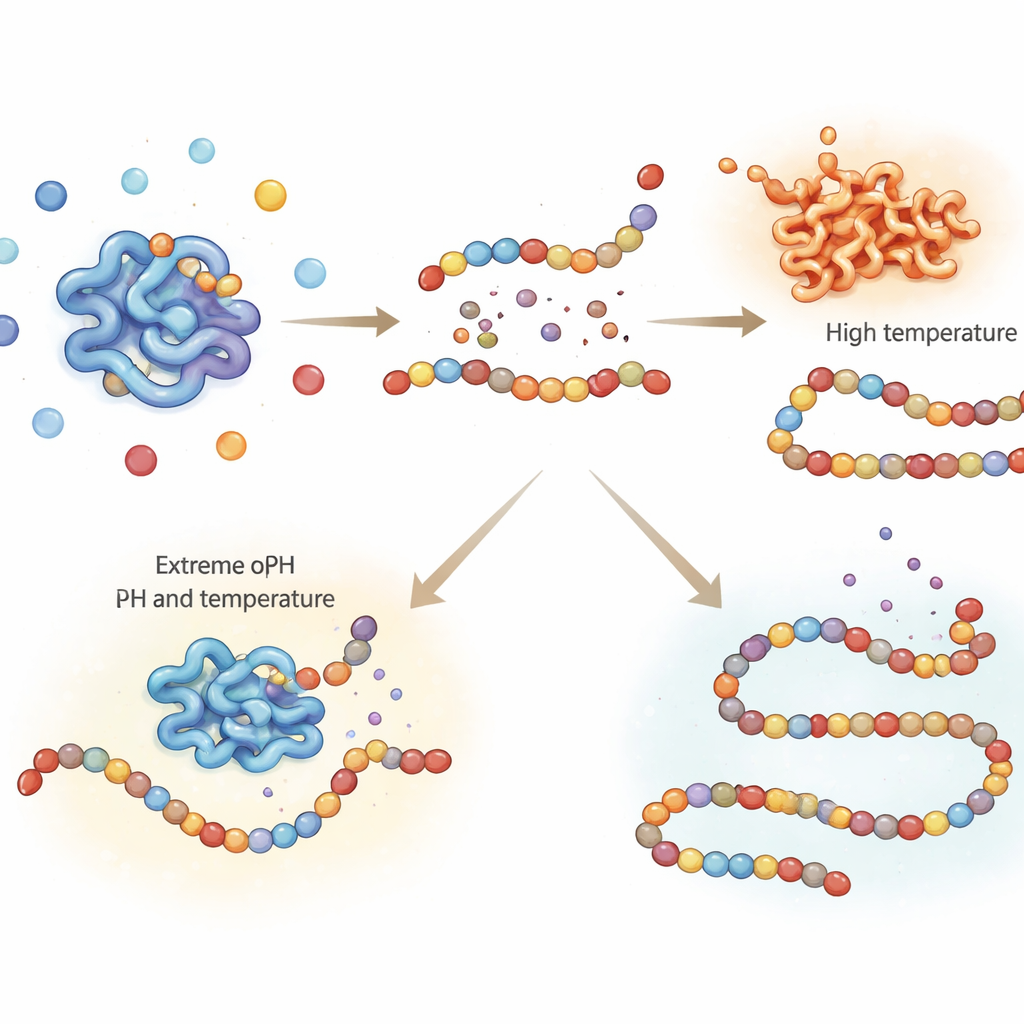
Нахождение бережной точки, где жара отключает пепсин
В экспериментах по перевариванию важно останавливать действие пепсина в определённые моменты, чтобы последующие измерения отражали то, что произошло в «желудке», а не продолжавшееся расщепление в пробирке. Обычный способ выключения ферментов — нагревание, но слишком высокая температура может повредить другие компоненты пищи и исказить результаты. В этом исследовании тщательно протестировали, как долго и насколько горячо нужно прогревать свиной пепсин, чтобы необратимо его инактивировать. Нагрев при 65 °C до 15 минут лишь частично снижал его активность, то есть фермент мог продолжать работать и после этого. Напротив, прогревание при 75 °C или выше всего 5 минут полностью и необратимо выключало пепсин. Инфракрасная спектроскопия структуры фермента показала, что эти более высокие температуры вызывают стойкое распадение третичной структуры и агрегацию белка, что согласуется с потерей активности.
Что это значит для пищевых исследований и здоровья
Для неспециалистов главный вывод в том, что свиной пепсин, широко используемый в лабораторных моделях, не ведёт себя точно так же, как человеческий, если учитывать реальные желудочные условия — меняющуюся кислотность и температуру. Новый инструмент прогнозирования помогает исследователям оценивать, какая мощность по расщеплению белков присутствует в каждый момент эксперимента, и судить, насколько их установка действительно отражает возможное поведение в человеческом желудке, включая желудок пожилых людей. Одновременно работа определяет бережное, но надёжное тепловое воздействие — пять минут при 75 °C — для выключения пепсина без излишнего повреждения других компонентов пищи. В совокупности эти достижения сделают лабораторные исследования переваривания более точными и сопоставимыми, улучшая наше понимание того, как разные продукты и методы обработки влияют на переваривание белков в повседневной жизни.
Цитирование: C. J., F., D., F., I., C. et al. A tool for predicting pH and temperature effects on porcine and human pepsin activity during in vitro gastric digestion. Sci Rep 16, 9176 (2026). https://doi.org/10.1038/s41598-026-38033-5
Ключевые слова: пепсин, желудочное переваривание, pH и температура, in vitro модели, переваривание белков