Clear Sky Science · ru
Вычислительное выявление и механистическая характеристика природных соединений, связывающихся с туннелем привения PDE6D
Обратить любимый выключатель рака против него самого
Многие из самых смертоносных опухолей — от поджелудочной железы до кишечника и легких — зависят от одного молекулярного «включателя» под названием RAS. Когда этот переключатель заедает в положении ВКЛ, клетки начинают бесконтрольно делиться. На протяжении десятилетий разработчики лекарств испытывали трудности с прямым выключением RAS. В этом исследовании рассматривается иной подход: поиск природных соединений, которые могут тихо блокировать вспомогательный белок, необходимый RAS для достижения места его действия, потенциально ослабляя его сигнал без прямой атаки на сам RAS. 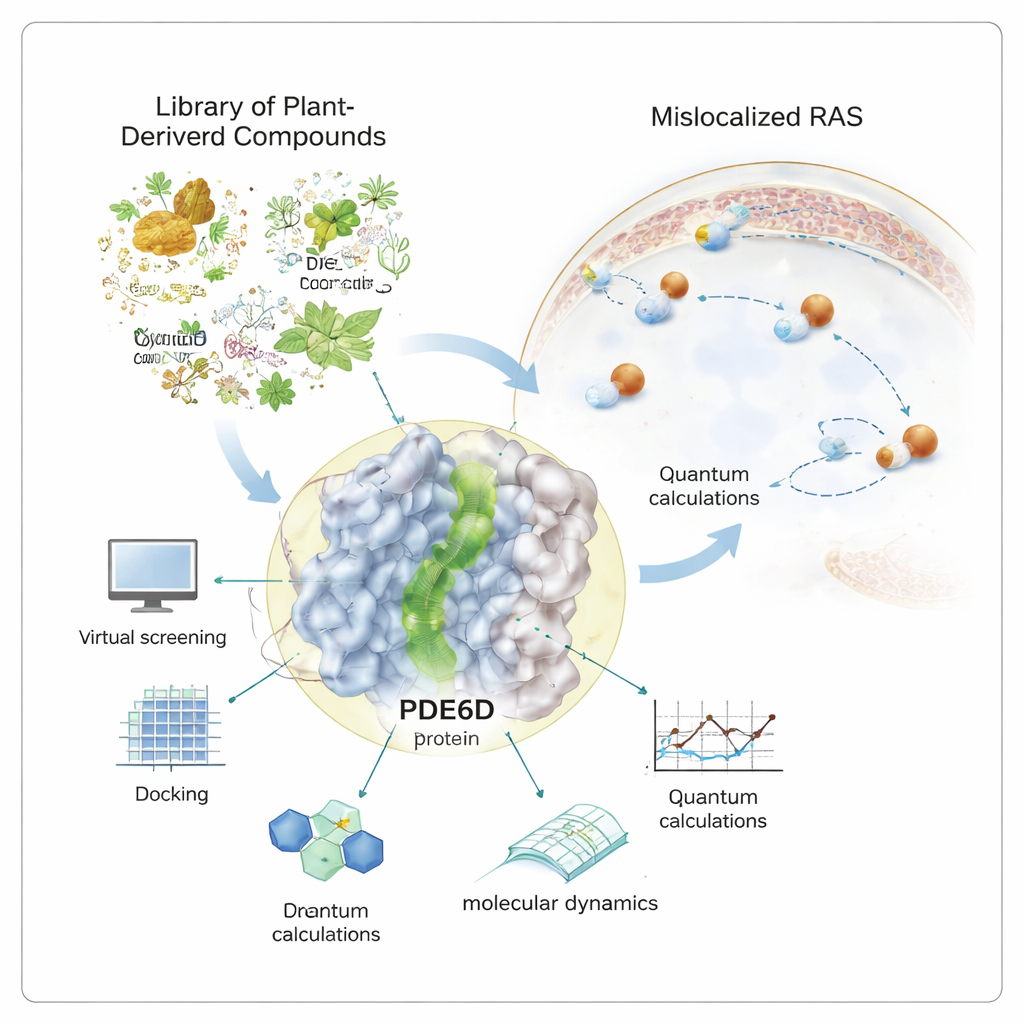
Скрытый помощник в раковых клетках
Белки RAS должны располагаться на внутренней поверхности клеточной мембраны, чтобы передавать сигналы роста. Для этого они несут «жирный» хвост, который позволяет им прикрепляться к мембране. Шаперонный белок PDE6D действует как такси, защищая этот хвост, когда RAS перемещается через водную среду клетки. У PDE6D есть узкий, облицованный маслом туннель, который захватывает хвост RAS. Если этот туннель заблокировать, RAS с большей вероятностью окажется не в том месте, что ослабляет его способность стимулировать развитие рака. Поскольку многие существующие препараты против RAS эффективны лишь для небольшой группы мутаций, исследователи заинтересованы в изучении PDE6D как косвенной, но более широко релевантной мишени.
Использование компьютеров для добычи химической библиотеки природы
Вместо того чтобы полагаться исключительно на синтетические соединения, автор обратился к курируемой библиотеке из более чем тысячи доступных для покупки природных продуктов — молекул, первоначально извлеченных из растений, микроорганизмов и других живых источников. Мощные компьютерные инструменты были использованы для скрининга этой библиотеки против трехмерной структуры PDE6D. В этом виртуальном тесте каждая молекула «швартовалась» в туннеле, чтобы проверить, насколько плотно и благоприятно она может связываться. Лучшие по оценкам кандидаты затем изучались более детально с помощью квантово-механических расчетов, которые исследуют расположение электронов в каждой молекуле и то, насколько легко они могут участвовать в стабилизирующих взаимодействиях внутри белкового кармана.
Стресс-тестирование перспективных кандидатов в движении
Белки и малые молекулы не статичны внутри клеток, поэтому исследование пошло дальше статических снимков. С помощью длинных молекулярно-динамических симуляций, отслеживающих движение атомов в течение полумикросекунды, автор наблюдал, как каждое перспективное природное соединение вело себя внутри туннеля PDE6D со временем. Два кандидата, обозначенные MolPort-039-052-621 и MolPort-002-507-186, оставались зафиксированными в туннеле с устойчивыми сетями контактов, в то время как третья молекула сместилась к выходу туннеля и стала слабее прикрепленной. Дополнительные анализы показали, какие участки структуры PDE6D напрягались или успокаивались при связывании и как комплекс исследует свою «энергетическую ландшафт» — по сути, какие конформации наиболее комфортны и долгоживущи. 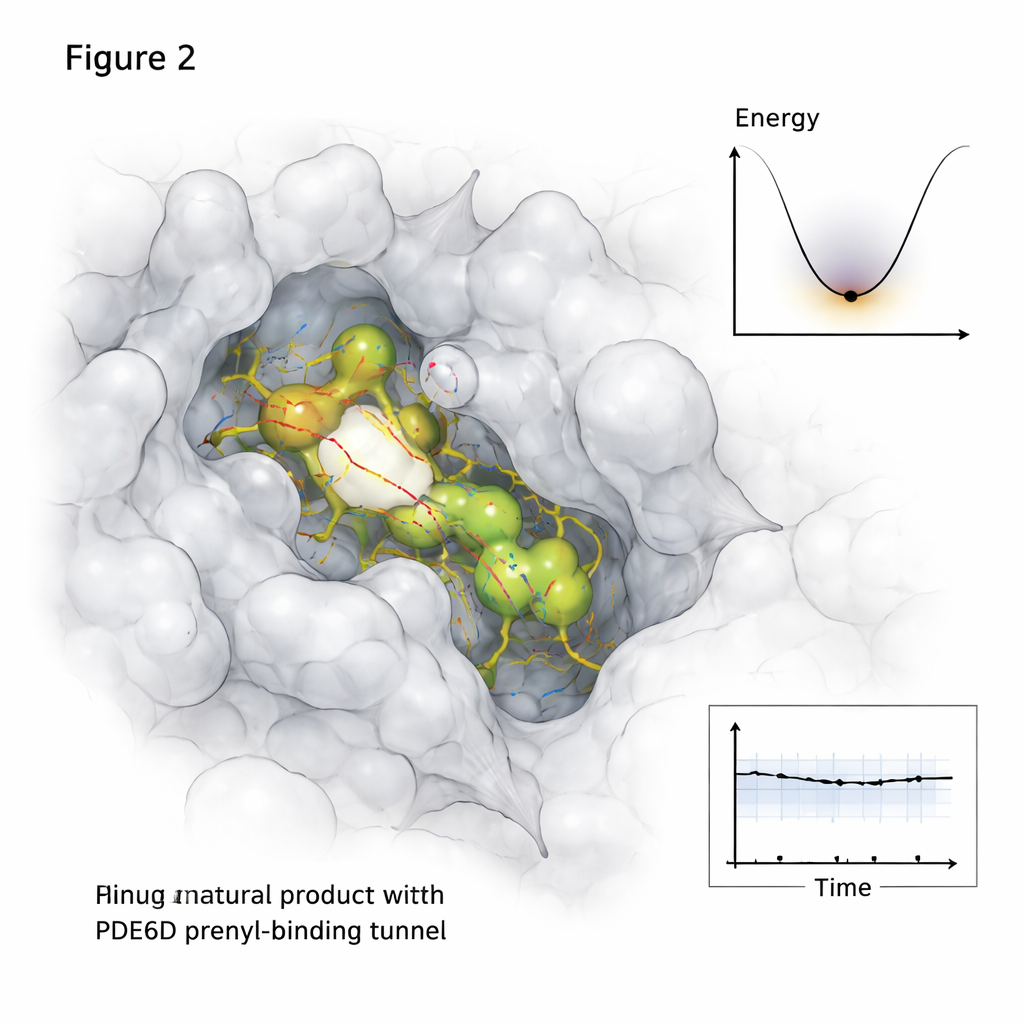
Баланс между силой связывания и свойствами, подходящими для лекарств
Исследование также использовало онлайн-инструменты прогнозирования, чтобы оценить, выглядят ли эти природные соединения реалистичными отправными точками для лекарств. Все три лучших кандидата обладали химическими признаками, соответствующими базовой «лекарственности», но у каждого были предупредительные сигналы. Некоторые, по прогнозам, имели плохую всасываемость или растворимость; другие показали признаки возможной токсичности, такие как влияние на ритм сердца или на ДНК. Эти проблемы означают, что молекулы в их текущем виде вряд ли готовы стать готовыми препаратами. Вместо этого их лучше рассматривать как структурные шаблоны, которые химики могут модифицировать, сохранив признаки, обеспечивающие посадку в туннель, и устранив проблемные фрагменты.
Что это значит для будущих методов лечения рака
Проще говоря, эта работа не представляет собой нового противоракового препарата, но прокладывает многообещающий путь. Комбинируя несколько уровней вычислений — от быстрого докинга до детальных симуляций и квантовых расчетов — исследование сужает огромный набор природных молекул до небольшой группы, которые, по-видимому, хорошо подходят для закупорки туннеля PDE6D. Если последующие лабораторные эксперименты подтвердят, что эти соединения действительно искажают локализацию RAS внутри клеток и замедляют рост опухолей, управляемых RAS, они могут послужить вдохновением для нового класса методов лечения, направленных на «логистику» рака, а не на его главный драйвер напрямую.
Цитирование: Alshahrani, M.M. Computational identification and mechanistic characterization of natural product binders targeting the PDE6D prenyl binding tunnel. Sci Rep 16, 6571 (2026). https://doi.org/10.1038/s41598-026-37939-4
Ключевые слова: RAS-сигнализация, ингибиторы PDE6D, природные продукты, вычислительная разработка лекарств, терапия рака