Clear Sky Science · ru
Радиомика МРТ на основе «мест обитания» для улучшенной диагностики болезни Паркинсона
Почему это важно для пациентов и их семей
Болезнь Паркинсона часто развивается постепенно — с едва заметными тремором или скованностью, которые трудно распознать. Сегодня врачи по‑прежнему во многом опираются на клинические симптомы и специализированные, дорогие исследования для постановки диагноза, и ранние случаи легко пропустить. В этом исследовании показано, что те же самые рутинные МРТ‑сканы, которые уже выполняются во многих больницах, можно проанализировать на предмет скрытых закономерностей — это дает более быстрый, менее инвазивный и впечатляюще точный способ выявления болезни Паркинсона.
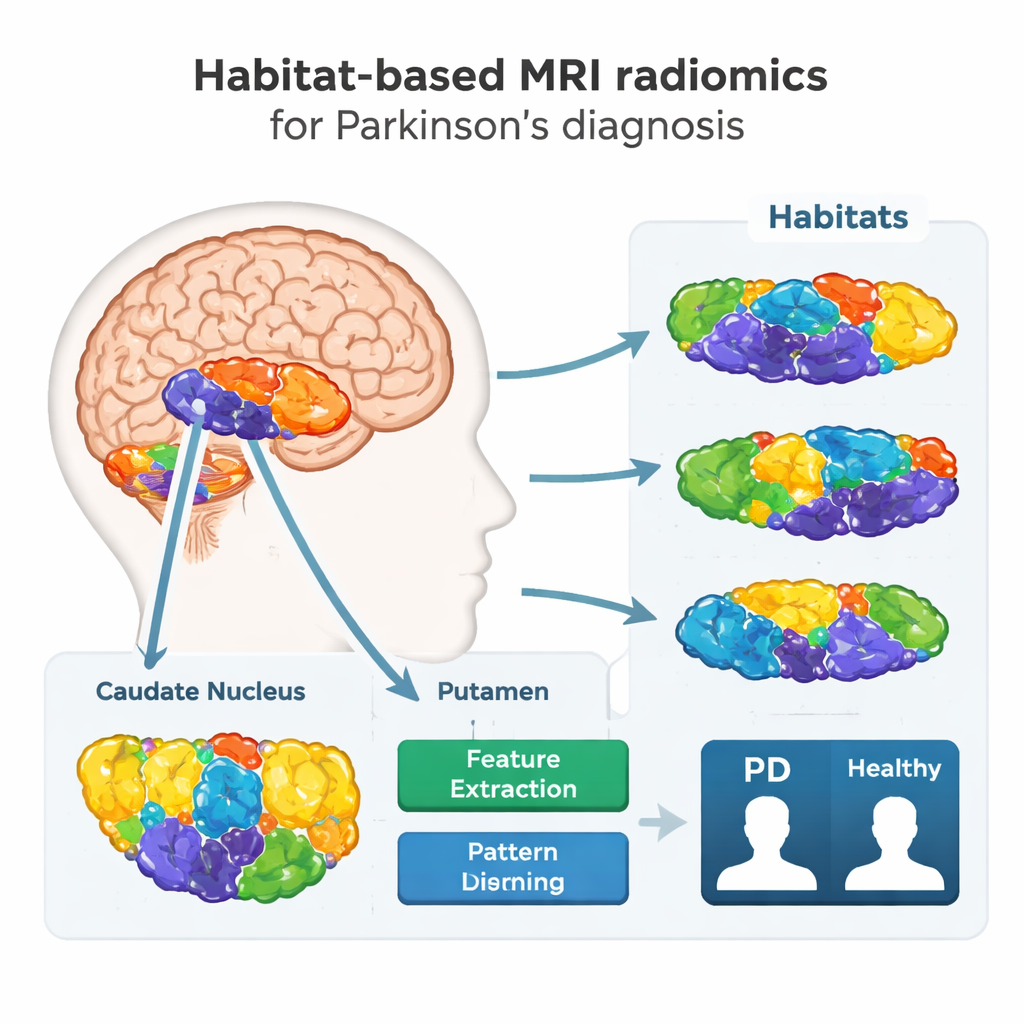
Новый взгляд внутрь мозга
Исследователи сосредоточились на двух глубоких структурах мозга — хвостатом ядре и путамене, — которые играют ключевую роль в контроле движений и сильно поражаются при болезни Паркинсона. Вместо того чтобы рассматривать каждую структуру как однородный кусок ткани, они задали более детальный вопрос: ведут ли себя по‑разному разные участки внутри этих регионов на МРТ и могут ли эти различия указывать на заболевание? Для этого собрали рутинные МРТ‑сканы 308 человек — 173 с болезнью Паркинсона и 135 здоровых добровольцев — в двух больницах с использованием разных сканеров, что отражает разнообразие, встречающееся в клинической практике.
От «районов» мозга к цифровым отпечаткам
С помощью метода, называемого радиомикой на основе мест обитания (habitat‑based radiomics), команда разбила каждую целевую область на более мелкие «районы» или «места обитания» на основе тонких различий яркости и текстуры на МРТ‑изображениях. Алгоритм сгруппировал воксели (маленькие 3D‑пиксели) со схожими характеристиками изображения в эти места обитания, затем извлёк сотни числовых признаков из каждого. Эти признаки формируют своего рода цифровой отпечаток состояния ткани, фиксируя крошечные аномалии, невидимые невооружённым взглядом, но возможные отражения потери нервных клеток, рубцевания или отложений железа, связанных с болезнью Паркинсона.
Обучение диагностической модели на рутинных сканах
Имея эти отпечатки, ученые обучили модель машинного обучения, известную как опорный векторный классификатор, отличать пациентов с болезнью Паркинсона от здоровых контролей. Они протестировали различные способы деления областей мозга на места обитания — от одной большой зоны до десяти мелких. Для оценки производительности использовались как основная обучающая выборка, так и независимая валидационная. При делении регионов на пять мест обитания модель показала наилучший результат: на новых, невидимых данных она правильно выявляла болезнь Паркинсона почти у 9 из 10 человек и достигала общей диагностической точности свыше 94% в полном исследовании. Это превосходит предыдущие подходы, которые рассматривали каждую область мозга как единое целое и часто застревали в районе 80–85% точности.
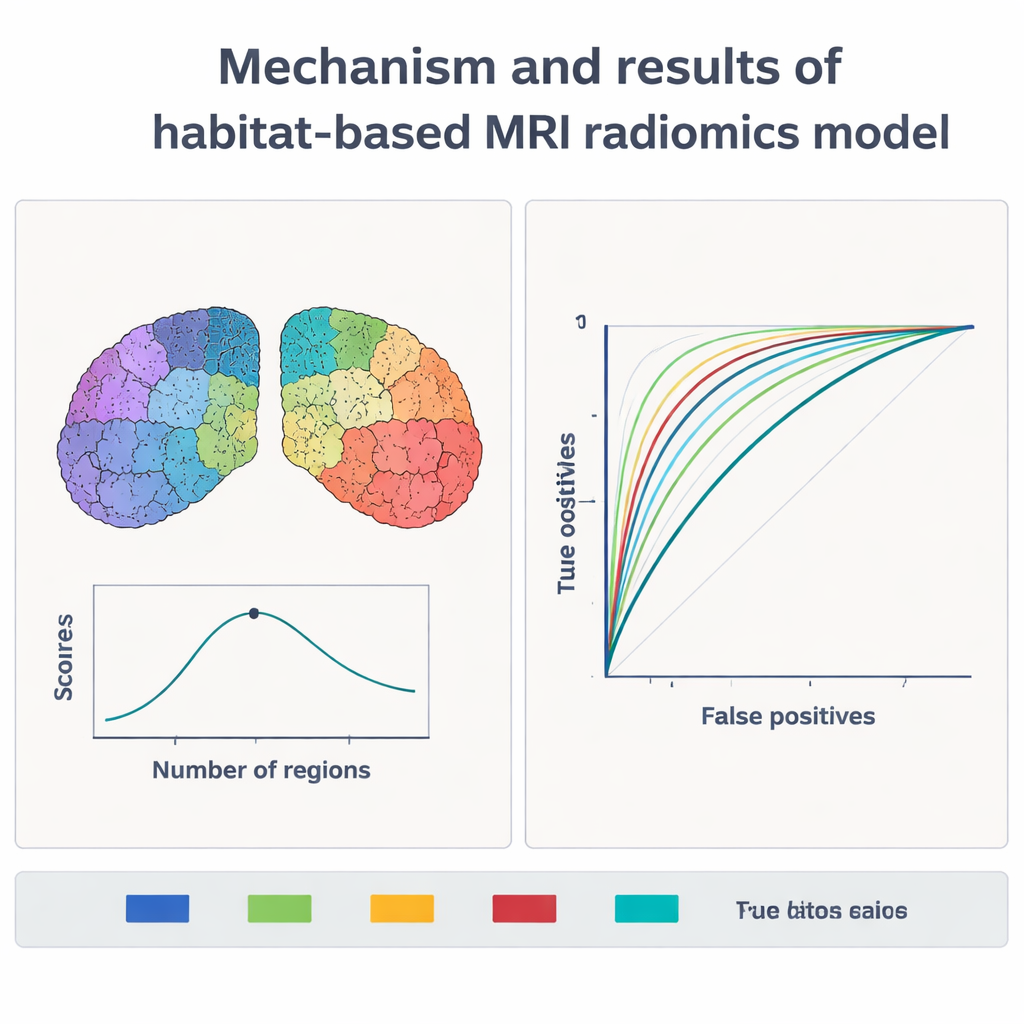
Что модель на самом деле «видит»
Чтобы не превращать модель в «чёрный ящик», команда использовала метод объяснимости SHAP, чтобы понять, какие признаки изображения влияли на решения модели. Наиболее важные сигналы поступали из T2‑взвешенных МРТ — распространённой клинической последовательности. У людей с болезнью Паркинсона соответствующие места обитания показывали большую вариативность интенсивности, более выраженные яркие и тёмные пятна и смещённые распределения интенсивности по сравнению со здоровыми участниками. Эти закономерности, вероятно, отражают известные патофизиологические процессы в базальных ганглиях, такие как гибель дофаминпродуцирующих нейронов, локальное рубцевание и аномальные отложения железа. Важно, что те же признаки повторялись при различных разбиениях и переразборах данных и оставались устойчивыми при использовании разных сканеров, что указывает на устойчивость метода, а не на совпадение, связанное с конкретным аппаратом.
От исследовательского инструмента к клинике
Анализы кривых решений, которые взвешивают выгоды от обнаружения истинных случаев против вреда ложных тревог, показали, что модель может помочь клиницистам решить, кому действительно требуется дальнейшее обследование, например DaTscan, а кому можно безопасно избежать дополнительных дорогостоящих процедур. Поскольку метод опирается только на стандартные МРТ‑сканы и программное обеспечение, он может быть особенно полезен в условиях, где передовая ядерная визуализация недоступна или слишком дорога. Авторы утверждают, что радиомика на основе мест обитания превращает привычные МРТ‑изображения в богатые карты данных, предлагая мощный неинвазивный инструмент для более ранней и более точной диагностики болезни Паркинсона и закладывая основу для будущих методов, которые также могут отслеживать прогрессирование болезни и помогать в выборе лечения.
Цитирование: Li, YZ., Wang, Y., Cai, C. et al. Habitat-based MRI radiomics for enhanced parkinson’s diagnosis. Sci Rep 16, 4755 (2026). https://doi.org/10.1038/s41598-026-37923-y
Ключевые слова: Болезнь Паркинсона, МРТ, радиомика, машинное обучение, ранняя диагностика