Clear Sky Science · ru
Белок нуклеокапсида SARS-CoV-2 образует комплексы с растворимыми регуляторными белками комплемента, способные связываться с вирионом
Почему этот скрытый вирусный трюк важен
Большинство из нас слышали о «шиповидном» белке коронавируса — он является основной мишенью вакцин. Но внутри вируса есть другой белок, называемый нуклеокапсидным или N-белком, который оказывается не просто структурной упаковкой. В этом исследовании показано, что N-белок способен захватывать ключевые регулирующие белки иммунитета в крови и переносить их на поверхность вируса. Делая это, SARS-CoV-2 может частично выключать одну из наших ранних систем защиты — систему комплемента — помогая вирусу выживать и, возможно, способствуя тяжести COVID-19.
Ближе к внутреннему белку вируса
N-белок служит «оберткой» генома вируса, помогая упаковать и стабилизировать его РНК. Врачи обнаруживали высокие уровни N-белка в крови пациентов с COVID-19, особенно при тяжёлом течении, а предыдущие работы указывали, что он может вызывать воспалительные сигналы. Авторы задались вопросом, может ли N также мешать работе комплемента — сети белков крови, которые помечают захватчиков для уничтожения и способны проделывать отверстия в мембранах микробов. Многие вирусы эволюционно научились занимать или имитировать собственные регуляторы комплемента организма, чтобы избежать атаки. Команда поставила три вопроса: связывается ли N со спайком и самим вирусом, связывает ли он человеческие регуляторные белки комплемента в крови и может ли переносить эти регуляторы на поверхность вируса?
Как N и спайк встречаются на вирусе
С помощью нескольких тестов на связывание белков исследователи показали, что N-белок может напрямую прилипать к спайку, как к лабораторно полученному спайку, так и к спайку на реальных частицах SARS-CoV-2. Они подтвердили это взаимодействие в разных экспериментальных системах и измерили его силу, обнаружив сродство, сопоставимое со многими антителами. Разрезая спайк на фрагменты и определяя, какие участки оставались связанными с N, они картировали вероятные зоны контакта в основном в N-концевом домене спайка — области, уже известной как «горячая точка» для связывания антител и для связки с некоторыми молекулами хозяина. Это указывает на то, что N может формировать плотный, биологически значимый мост к спайку на реальных вирионах.
Похищение собственных предохранительных переключателей организма
Система комплемента строго контролируется растворимыми «тормозами», называемыми регуляторными белками комплемента, которые защищают наши клетки от «дружественного огня». Команда сосредоточилась на четырёх из них — C1-ингибиторе, C4-связывающем белке, факторе H и витронектине — потому что они действуют на различных этапах каскада комплемента. В тестах на основе сыворотки крови и в экспериментах с очищенными белками N-белок связывал все четыре регулятора, тогда как спайк при тех же условиях не связывался ни с одним из них. Это означает, что в плазме могут образовываться комплексы N–CRP. Важно, что когда N предварительно смешивали с человеческой сывороткой, а затем контактировали с вирусными частицами, исследователи обнаруживали эти регуляторные белки, прикреплённые к вирионам — но только при наличии N. Чем больше N использовали, тем больше регуляторов комплемента появлялось на вирусе, что указывает на дозозависимый механизм рекрутирования. 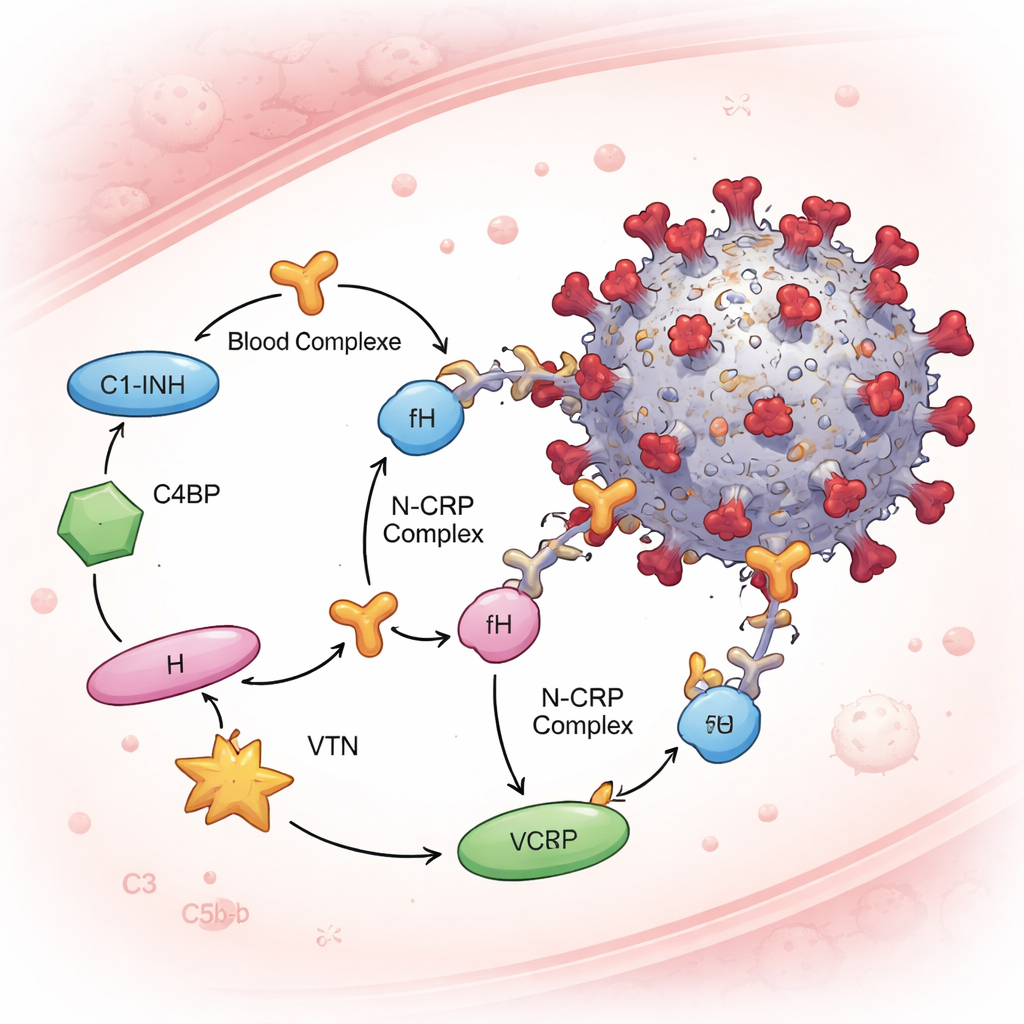
Ослабление завершающего шага атаки
Ключевым орудием системы комплемента является мембранно-атакующий комплекс (MAC) — кольцевидная структура, образующая поры в клеточных или вирусных оболочках. Авторы проверяли, может ли N менять образование MAC на SARS-CoV-2. Они инкубировали очищенный вирус с человеческой сывороткой — с добавлением N или без него — и затем измеряли, сколько комплекса C5b-9 (часть MAC) оказалось на вирионах. Без N вирус накапливал C5b-9, что указывает на активную атаку комплемента. При наличии N отложение MAC уменьшалось в концентрационно‑зависимом режиме: больше N — меньше C5b-9 на вирусе. Это согласуется с идеей, что N, украшая вирион регуляторами комплемента, защищает его от образования пор. 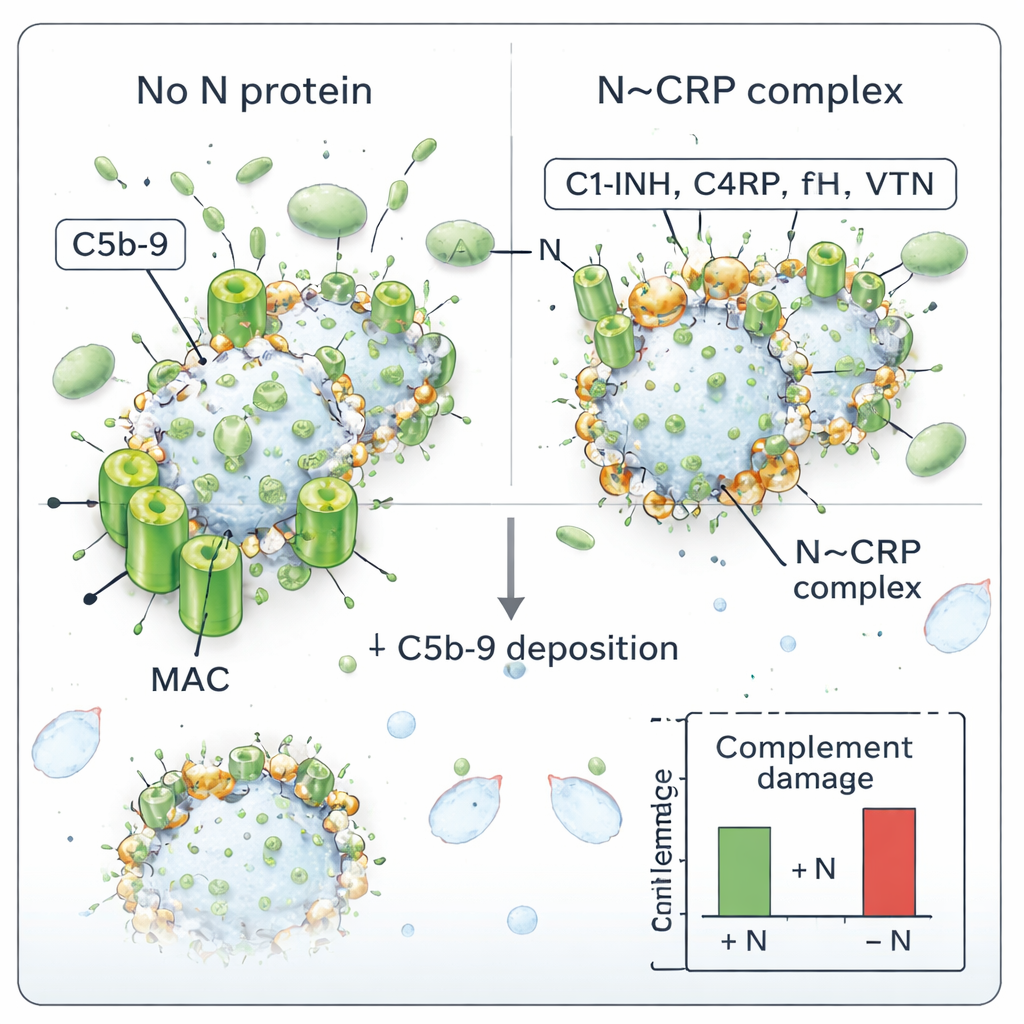
Что это значит для пациентов и будущих терапий
Для неспециалиста ключевая мысль такова: SARS-CoV-2 полагается не только на известный спайк, чтобы перехитрить иммунную систему. Его внутренний N‑белок может попадать в кровоток, захватывать собственные «тормоза» комплемента организма и переносить их обратно на поверхность вируса. Там они могут помочь вирусу скрыться от мощной ветви врождённого иммунитета и снизить прямое повреждение, вызванное комплементом. Это может способствовать как персистенции инфекции, так и запутанным нарушениям комплемента, наблюдаемым при тяжёлом COVID-19. Хотя эксперименты были выполнены в контролируемых лабораторных условиях, они подчёркивают взаимодействия N с комплементом как потенциальную новую цель: терапии, блокирующие связывание N с этими регуляторными белками, или восстанавливающие сбалансированную активность комплемента, могут со временем помочь переломить ход борьбы в пользу иммунной системы.
Цитирование: Víglaský, J., Bhide, K., Talpasova, L. et al. SARS-CoV-2 nucleocapsid protein forms complexes with soluble complement regulatory proteins that can bind to the virion. Sci Rep 16, 6599 (2026). https://doi.org/10.1038/s41598-026-37866-4
Ключевые слова: нуклеокапсид SARS-CoV-2, система комплемента, уклонение от иммунитета, регуляторные белки комплемента, тяжесть течения COVID-19