Clear Sky Science · ru
Моделирование и применение предсказания сложного признака болезни Альцгеймера на основе многозадачного обучения
Почему это исследование важно для семей и пациентов
Болезнь Альцгеймера — один из самых пугающих диагнозов нашего времени, однако врачам до сих пор трудно предсказать, у кого заболевание быстро прогрессирует, у кого стабильно сохраняется на протяжении лет и какие ранние признаки действительно имеют значение. В этом исследовании поставлен простой, но мощный вопрос: если рассматривать несколько результатов тестов и снимков мозга, связанных с Альцгеймером, вместе и объединять их с генетической информацией человека, сможет ли современный искусственный интеллект выявить закономерности, которые помогут точнее прогнозировать ход болезни?
Многие лица одной и той же болезни
Альцгеймер — это не только потеря памяти. Пациенты различаются по результатам когнитивных тестов, по тому, как они справляются с повседневными задачами, и по тому, как выглядят их снимки мозга. Эти разные измерения — такие как общие шкалы памяти и мышления, опросники о повседневном функционировании и ПЭТ-сканы метаболизма или накопления амилоида — известны тем, что частично зависят от генов. Важно и то, что они также разделяют некоторые общие генетические корни. Традиционные методы прогнозирования обычно фокусируются на одной мере за раз, упуская полезный факт взаимосвязи этих признаков. Авторы утверждают, что модели, как и врач, видящий полную картину, а не отдельный тест, должны учиться на нескольких признаках одновременно.
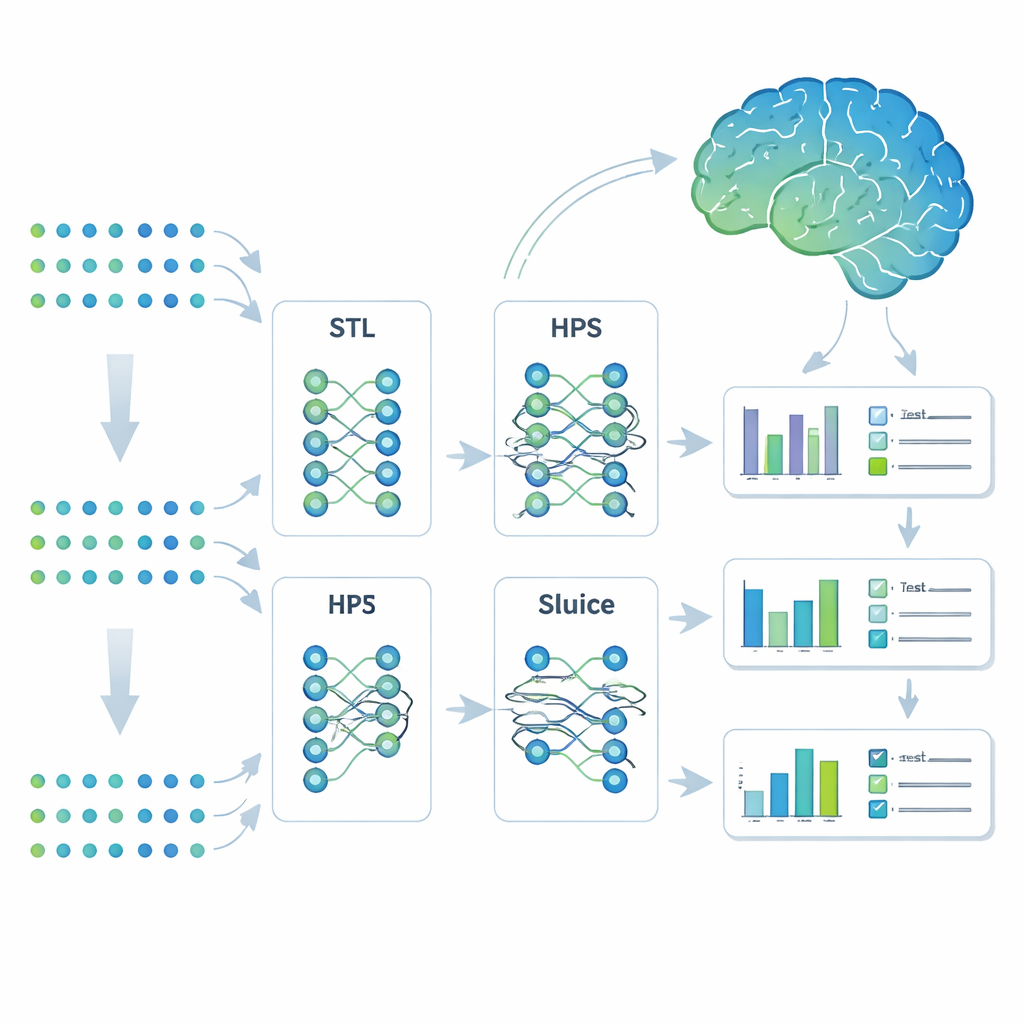
Обучение одной модели многим связанным задачам
Исследователи обратились к стратегии машинного обучения, называемой многозадачным обучением. Вместо создания отдельных моделей для каждого результата они обучили единую систему прогнозировать семь признаков, связанных с Альцгеймером, одновременно. Они сравнили четыре подхода: полностью отдельные модели (обучение на одну задачу), простая общая модель, разделяющаяся только в конце (жёсткое совместное использование параметров), более гибкая ветвящаяся архитектура, способная делить задачи на подгруппы, и высокоадаптивная конструкция под названием Sluice Network, которая может тонко настраивать степень обмена информацией на каждом слое сети. Все четыре модели получали одинаковые генетические входные данные; различие заключалось в том, как они делились выученной информацией между признаками.
Проверка идей на смоделированных геномах
Прежде чем доверять модели на реальных пациентах, команда создала подробные симуляции, используя реальные генетические паттерны из Инициативы по нейровизуализации болезни Альцгеймера (ADNI), но с контролируемыми исходами. Они построили сценарии, в которых все признаки имели одни и те же генетические причины, где признаки формировали перекрывающиеся группы, и где у каждого признака были свои собственные причины. Также варьировали силу генетических сигналов и уровень шума, имитируя грязную реальность человеческих данных. Во почти всех условиях Sluice Network показала наибольшую точность прогнозов и оставалась стабильной даже когда признаки были слабо связаны. Более простые общие модели хорошо работали при большом числе общих генетических факторов, но испытывали трудности при низкой степени общего унаследования, тогда как полностью отдельные модели были устойчивы, но в целом менее точны.
Данные реального мира и сила группировки генов
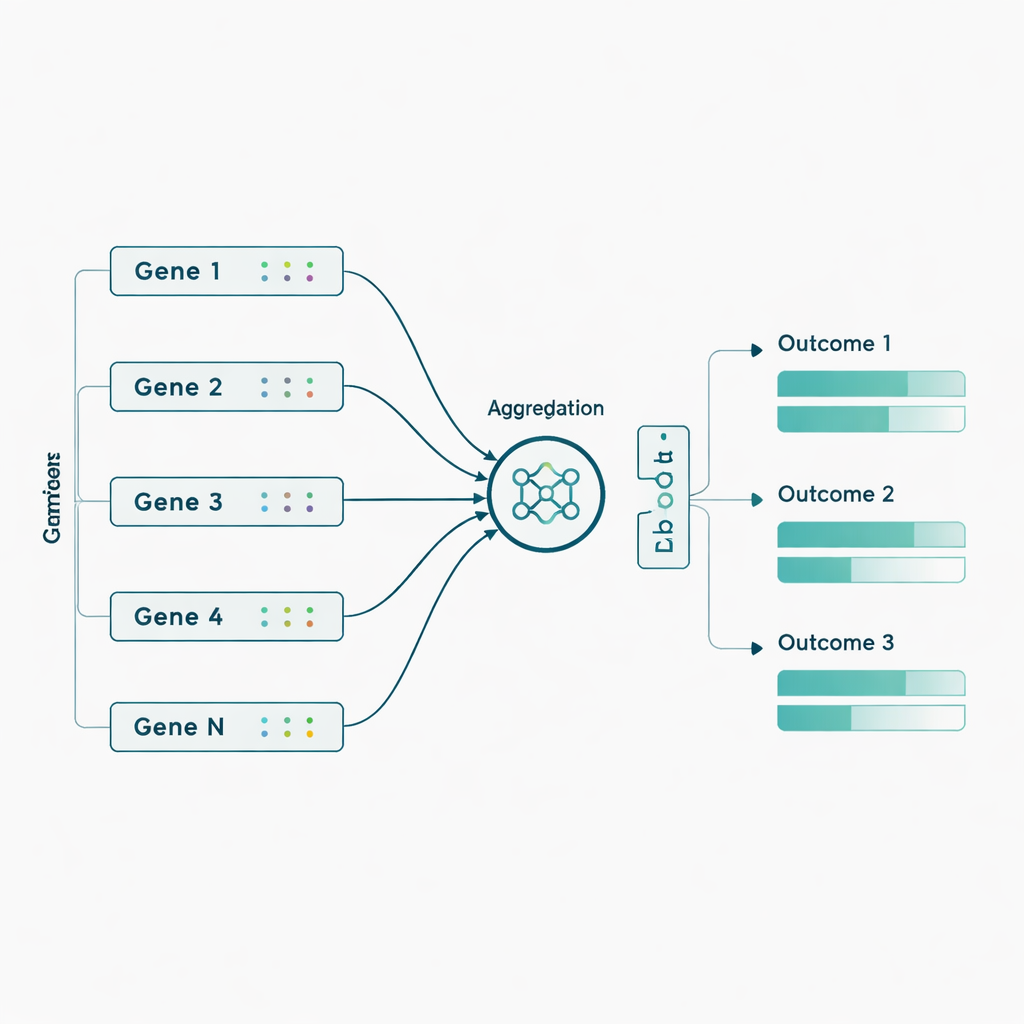
Затем авторы применили эти модели к реальным данным ADNI от 463 человек, используя почти 3800 генетических маркеров из 56 генов, ранее связанных с Альцгеймером. Здесь они добавили биологически обоснованную идею: вместо того чтобы подавать в сеть тысячи отдельных маркеров, они сначала сгруппировали маркеры по генам и позволили сети выучить компактный «сводный» сигнал для каждого гена перед прогнозированием семи исходов. Такая агрегация на уровне генов улучшила результаты для большинства моделей и особенно для Sluice Network, которая приблизительно удвоила среднюю корреляцию с реальными исходами. Прирост был наиболее заметен для показателей ПЭТ-сканирования и некоторых когнитивных и функциональных шкал, что указывает на то, что слабые генетические эффекты становятся более обнаружимыми при объединении на уровне гена, а не при рассмотрении их как отдельных маркеров.
Что это означает для будущего прогнозирования и ухода
Для неспециалиста вывод таков: более умные, гибкие модели ИИ могут извлечь больше информации из тех же генетических и клинических данных, обучаясь на нескольких связанных исходах одновременно и учитывая биологическую организацию в виде генов. Хотя текущие улучшения скромны и далеки от клинического теста, подход указывает путь к более надёжным инструментам для оценки профильного риска человека, отслеживания вероятного прогрессирования и, возможно, индивидуализации мониторинга или вмешательств. В сложных заболеваниях, таких как Альцгеймер, где многие мелкие генетические эффекты взаимодействуют, методы, которые обмениваются информацией между признаками и агрегируют слабые сигналы, могут дать более ясную и информативную картину, чем традиционные одно-признаковые оценки.
Цитирование: Zhou, W., Xue, Z., Liang, J. et al. Modeling and application of alzheimer’s disease complex trait prediction based on multi-task learning. Sci Rep 16, 7749 (2026). https://doi.org/10.1038/s41598-026-37820-4
Ключевые слова: Генетика болезни Альцгеймера, многозадачное обучение, прогнозирование с помощью глубокого обучения, нейровизуализационные биомаркеры, агрегация на уровне генов