Clear Sky Science · ru
Предварительная оценка распределения по тканям и нацеливания флуоресцентного молекулярного зонда Cy7-SYL3C в модели колоректального рака с положительной экспрессией EpCAM у мышей
Почему это важно для выявления рака
Колоректальный рак — одна из ведущих причин смертности от рака в мире, отчасти потому, что многие опухоли обнаруживаются на поздних стадиях. Сегодня основной скрининговый метод, колоноскопия, эффективен, но инвазивен и неприятен, поэтому многие люди его избегают. В этом исследовании изучается новый тип «умного» светящегося трейсера, который однажды может помочь врачам видеть опухоли кишечника раньше и яснее, используя свет вместо скальпеля или длинной трубки.
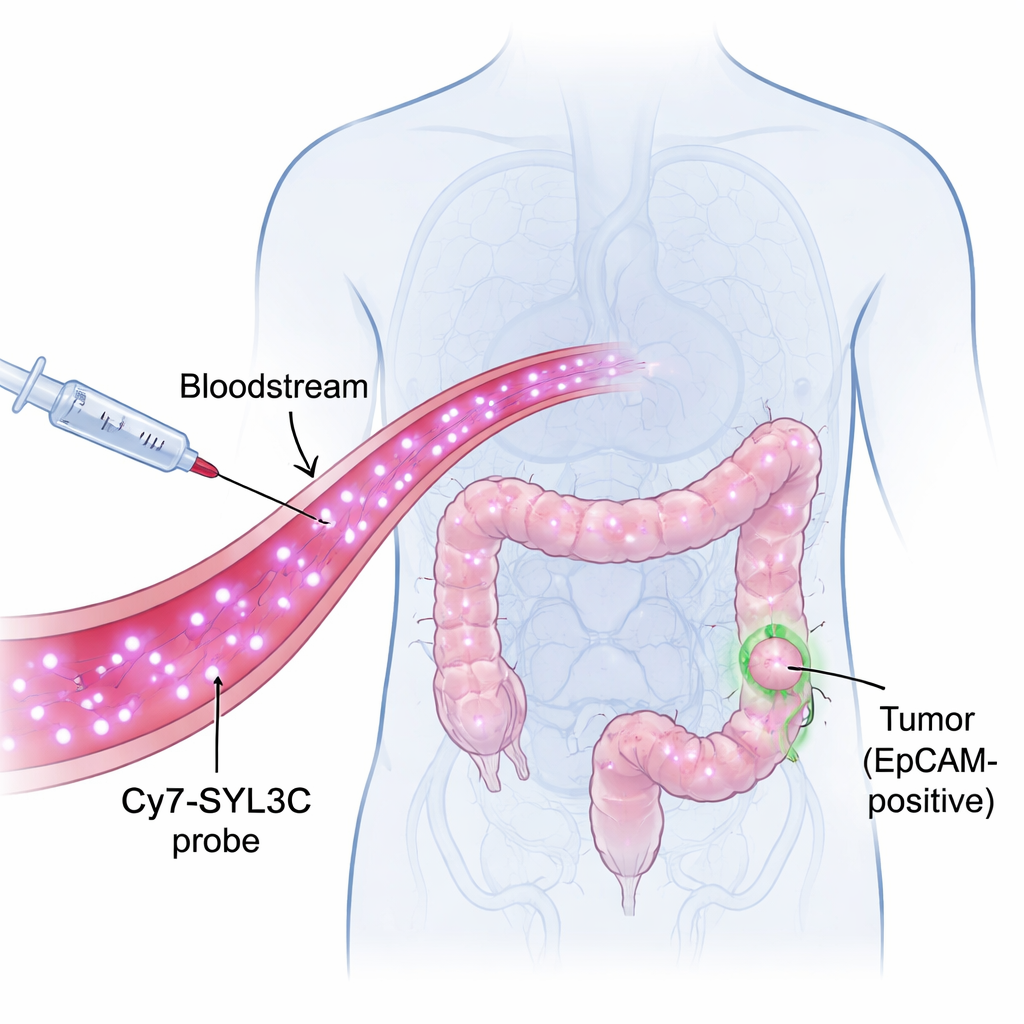
Светящийся ярлык, распознающий опухолевые клетки
Исследователи сосредоточились на молекуле EpCAM, которая находится на поверхности многих клеток колоректального рака, но мало присутствует в здоровых тканях. Они создали зонд Cy7-SYL3C, присоединив краситель ближней инфракрасной области (Cy7) к короткой цепочке ДНК — аптамеру (SYL3C), — который узнаёт EpCAM подобно тому, как ключ подходит к замку. Ближний инфракрасный свет невидим глазу, но может проникать на несколько миллиметров в ткань, что позволяет камерам фиксировать сигналы изнутри тела с высоким контрастом. Идея проста: ввести Cy7-SYL3C в кровоток, дать ему найти клетки опухоли, богатые EpCAM, а затем с помощью специальной камеры заставить эти клетки светиться на тёмном фоне.
Проверка безопасности и стабильности в лаборатории
Прежде чем применять зонд на живых животных, команда проверила его стабильность и безопасность. Они смешали Cy7-SYL3C с сывороткой крови мышей и крупного рогатого скота и обнаружили, что большая часть зонда остаётся целой как минимум в течение восьми часов — достаточно для проведения визуализации во время медицинской процедуры. Затем зонд подвергали воздействию на клетки человеческого колоректального рака и нормальные клетки толстой кишки при разных концентрациях. Рост клеток фактически не изменялся, а при смешении с эритроцитами зонд не вызывал их гемолиза. Эти тесты указывают на то, что Cy7-SYL3C химически стабильный и щадящий для клеток — ключевые требования к любому контрастному веществу, применимому у пациентов.
Куда зонд направляется в организме
Учёные затем проследили путь Cy7-SYL3C в организме здоровых мышей с помощью системы визуализации для мелких животных. Вскоре после инъекции самый сильный сигнал появлялся в печени и почках — органах, фильтрующих и выводящих вещества из крови. Сигнал в печени достиг пика примерно через час и затем ослабевал, тогда как почки продолжали светиться дольше, что указывает на мочу как основной путь выведения зонда. Через два дня оставалась лишь малая доля первоначального сигнала, а микроскопическое исследование основных органов не выявило очевидных повреждений тканей. Это означает, что зонд выводится достаточно быстро и не наносит видимого вреда жизненно важным органам в рамках этого краткосрочного исследования.
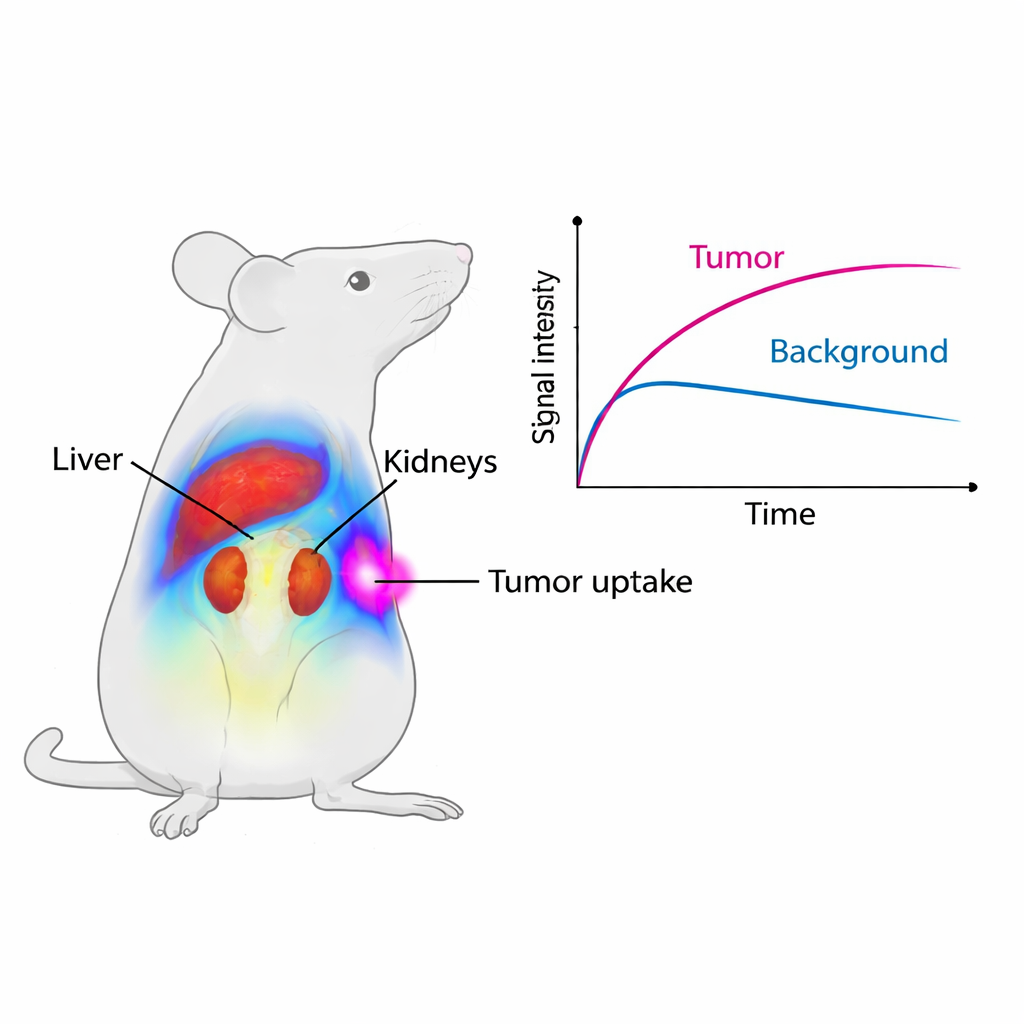
Наведение на колоректальные опухоли
Чтобы проверить, действительно ли Cy7-SYL3C находит раковые клетки, команда использовала мышей с имплантированными человеческими колоректальными опухолями, экспрессирующими EpCAM. Уже через пять минут после инъекции опухоли начали светиться на системе визуализации. В течение первых четырёх часов средний сигнал в опухолях был почти вдвое сильнее, чем у мышей, у которых опухоли были «предзаблокированы» избытком немеченого SYL3C, временно занявшего места EpCAM и помешавшего флуоресцентному зонду связываться. Отношение сигнала в опухоли к сигналу в близлежащей мышце поднялось выше единицы и достигло пика примерно через восемь часов, что означает, что опухоли были заметно ярче окружения в течение полезного окна для визуализации. Детальные микроскопические исследования подтвердили, что флуоресцентный зонд совпадал с окраской на EpCAM в опухолевых клетках, тогда как в нормальных органах EpCAM был минимален или отсутствовал.
Как это может помочь при хирургии и диагностике
Для неспециалиста главный вывод таков: Cy7-SYL3C ведёт себя как «умный» краситель, который находит клетки колоректального рака и затем в основном выводится через почки. Он выглядит стабильным, щадящим для клеток и способен быстро и в течение нескольких часов делать опухоли светящимися, что может помочь хирургам лучше видеть границы опухоли в реальном времени или помочь рентгенологам выявлять подозрительные участки при малоинвазивных процедурах. Хотя эти результаты получены в ранних экспериментах на мышах и до применения у людей потребуется ещё много работы, исследование закладывает важную основу для нового класса световых трассеров, которые могут сделать обнаружение и хирургическое лечение колоректального рака более точным и менее инвазивным.
Цитирование: Li, Y., Li, M., Li, P. et al. Preliminary assessment of biodistribution and targeting of the fluorescent molecular probe Cy7-SYL3C in an EpCAM-positive colorectal cancer mouse model. Sci Rep 16, 6589 (2026). https://doi.org/10.1038/s41598-026-37787-2
Ключевые слова: визуализация колоректального рака, флуоресценция в ближней инфракрасной области, нацеливание на EpCAM, аптамерный зонд, навигация при операции опухоли