Clear Sky Science · ru
Многомерная стратегия позволяет масштабировать разнообразие метаболома в микробных ферментациях
Почему мелкие изменения «заводов» важны для новых лекарств
Многие современные лекарства происходят от природных соединений, вырабатываемых бактериями и грибами. Но превращение перспективного лабораторного кандидата в реальную лекарственную молекулу часто терпит неудачу на удивительно приземлённом этапе: при выращивании того же микроорганизма в другой посуде или в больших объёмах. В этом исследовании задают простой, но важный вопрос — как сохранить устойчивость и разнообразие химической продукции микроба при переходе с малых планшеток на большие колбы и биореакторы? Ответ может ускорить поиск следующего поколения антибиотиков и других терапий.
Три способа вырастить один и тот же микроб
Исследователи сосредоточились на почвенной бактерии Streptomyces griseochromogenes, известной синтезом множества «вторичных метаболитов» — малых молекул с потенциалом лекарственных свойств. Они сравнили три распространённые системы культивирования, используемые на ранних этапах поиска: колбы с перегородками для встряхивания, 48‑луночные микротитровые планшеты «цветок» и мешалочный биореактор. В каждой системе измеряли рост, форму и структуру клеток и, что особенно важно, профиль химических сигналов, детектируемых масс‑спектрометрией, используемой здесь как отпечаток секретируемого микробом метаболома. Сначала применили классическое инженерное правило: сохранить одинаковую доступность кислорода во всех системах и рассчитывать на похожее поведение. Вместо этого они обнаружили, что кривые роста, форма клеток и химические «отпечатки» резко различаются в разных сосудах.
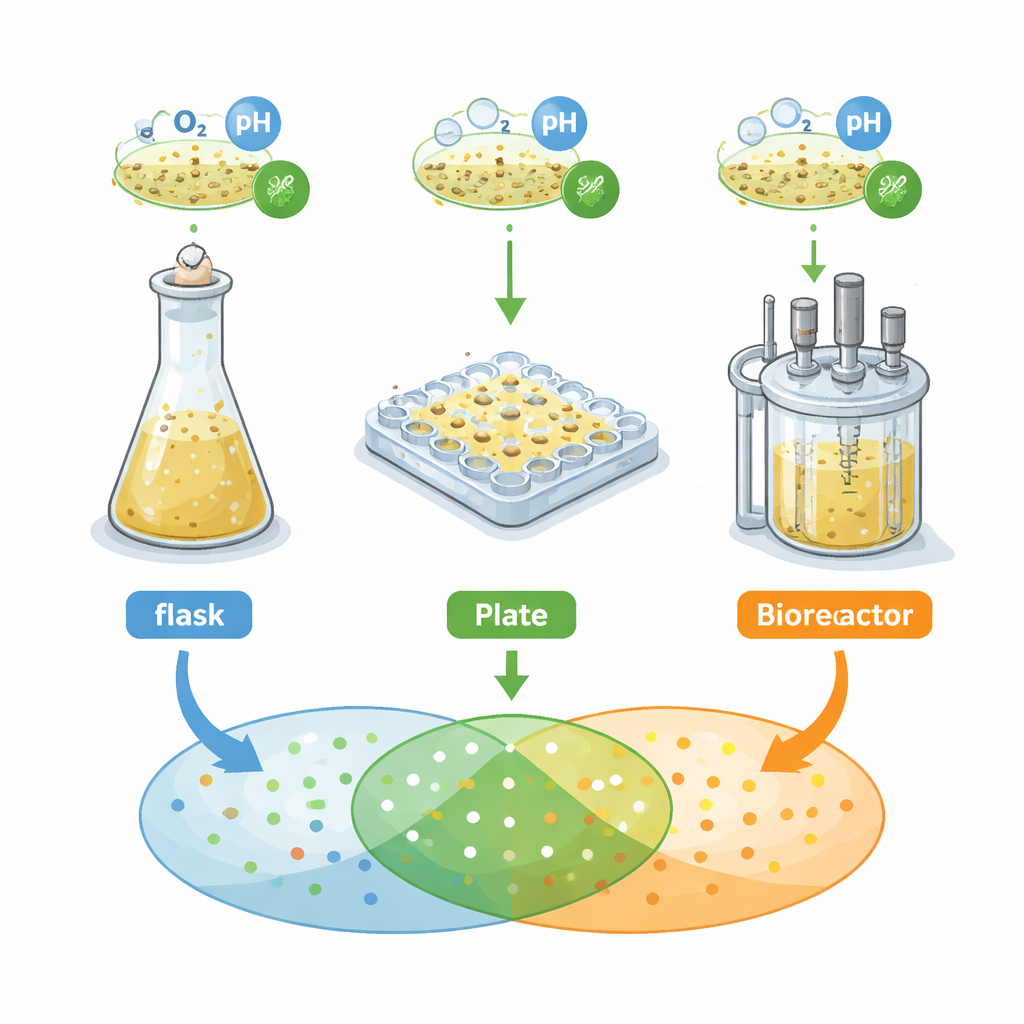
Когда одного правила недостаточно
Согласование только по кислороду привело к очень разным «метаболическим отпечаткам» — наборам масс‑пиков, соответствующих отдельным молекулам. Лишь около 18 процентов этих пиков были общими для всех трёх систем. Микротитровые планшеты давали гораздо больше уникальных сигналов, чем колбы или биореактор. Команда затем протестировала другой однофакторный подход: меняли либо долю этанола в среде (малое соединение, способное стимулировать синтез метаболитов), либо скорость перемешивания, что влияет на поступление кислорода. Эти одномерные настройки умеренно улучшили совпадение химических отпечатков, но лишь примерно на дополнительные 18 процентов. Иными словами, простые рецепты вроде «добавьте кислород» или «добавьте этанол» не могли гарантировать, что метаболит, обнаруженный в крошечной лунке, надёжно появится в большем ферментере.
Как форма клеток направляет химическое разнообразие
Чтобы выяснить, что действительно важно, авторы объединили данные из 80 различных культивирований и использовали статистический метод, выявляющий скрытые факторы, формирующие результат. Этот анализ выделил две ключевые темы: сам тип среды культивирования и морфология клеток — растут ли бактерии в виде компактных пеллет, рыхлых мицелиальных ковров или тонко диспергированных нитей. Условия, дававшие похожие морфологии, как правило, приводили и к более похожим метаболическим отпечаткам и облегчали «масштабирование» молекул из малых систем в мешалочный бак. Целенаправленный подбор наборов условий, обеспечивающих сопоставимые формы клеток во всех трёх системах, увеличил совпадение химических признаков примерно на 50 процентов по сравнению с классическим согласованием по кислороду.
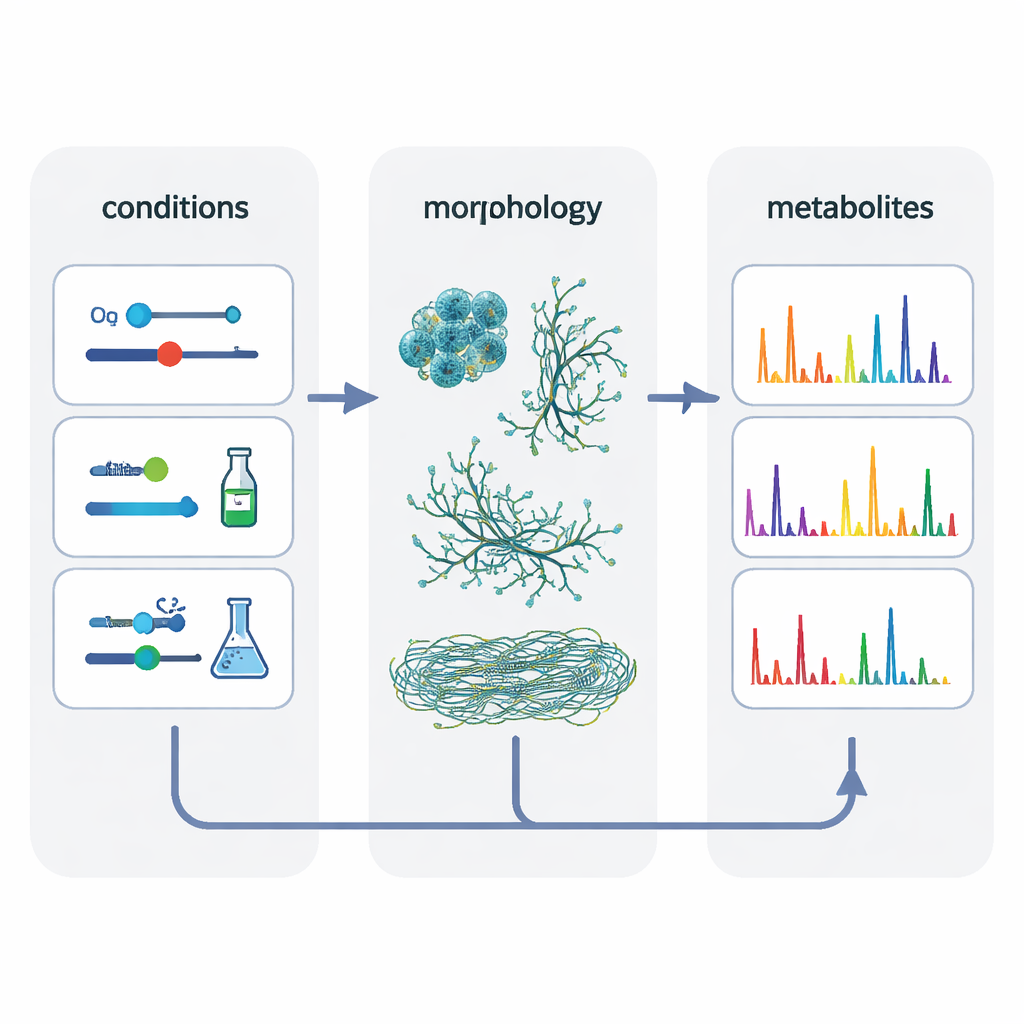
Скрытые химические семейства и молекулы, специфичные для системы
Помимо простого подсчёта сигналов, команда построила молекулярные сети, группирующие родственные масс‑пики в семейства структурно схожих метаболитов. Крупные семейства часто включали хотя бы один представитель, обнаруживаемый во всех системах культивирования, что указывает на некоторую «ядровую» химию, устойчивую к изменениям масштаба. Но многие более мелкие семейства — и отдельные молекулы — появлялись лишь в одном типе сосуда. Полистирольные микротитровые планшеты особенно давали самое богатое разнообразие соединений, включая многочисленные варианты железосвязывающих сидерофоров десферроксаминов и несколько нон‑рибосомных пептидов. Авторы предполагают, что тонкие стрессовые факторы в этих планшетах, например повышенные уровни реактивных форм кислорода, могут стимулировать бактерии к диверсификации химии, тогда как хорошо перемешанный биореактор благоприятствует меньшему набору «основных» структур.
Что это значит для поиска новых природных продуктов
Для команд по поиску лекарств послание ясно: нельзя полагаться на одно инженерное правило или на одну «оптимальную» условие, если вы хотите одновременно богатого химического разнообразия и надёжного масштабирования. Вместо этого нужна многомерная стратегия, учитывающая тип сосуда, перенос кислорода, добавки вроде этанола и, что важно, мониторинг морфологии клеток в реальном времени. Использование микротитровых планшетов, имитирующих ключевые особенности биореакторов, и настройка условий для получения сходных форм роста могут сильно повысить вероятность того, что перспективные молекулы, обнаруженные в микролитровом масштабе, вновь появятся при выращивании в литрах. Такой подход помогает превратить хрупкие ранние находки в надёжные, воспроизводимые кандидаты, увеличивая шансы, что новые природные продукты благополучно пройдут путь от лаборатории до аптек.
Цитирование: Lindig, A., Fataeri, M., Hubmann, G. et al. Multidimensional strategy enables scalable metabolome diversity in microbial fermentations. Sci Rep 16, 4084 (2026). https://doi.org/10.1038/s41598-026-37748-9
Ключевые слова: открытие природных продуктов, ферментация Streptomyces, метаболомика, масштабирование в биореакторе, вторичные метаболиты