Clear Sky Science · ru
Синергетическое воздействие на ось ARID2–MYC помалидомидом и панобиномистатом преодолевает внутриполную резистентность к IMiD при множественной миеломе
Почему это исследование важно для пациентов
Множественная миелома — это рак клеток, вырабатывающих антитела в костном мозге; он стал более поддающимся лечению, но все еще редко излечим. У многих пациентов со временем развивается потеря ответа на стандартные препараты, и врачам остается меньше вариантов терапии. В этом исследовании выясняют, почему сочетание двух уже существующих классов препаратов — так называемых IMiD (например, помалидомид) и ингибиторов гистондеацетилаз (HDAC), таких как панобиномистат, может работать совместно, чтобы убивать клетки миelомы даже тогда, когда опухоль устойчива к IMiD в одиночку. Понимание этого взаимодействия на молекулярном уровне может помочь в подборе более эффективных комбинированных схем и позволит большему числу пациентов получить выгоду от уже доступных лекарств.
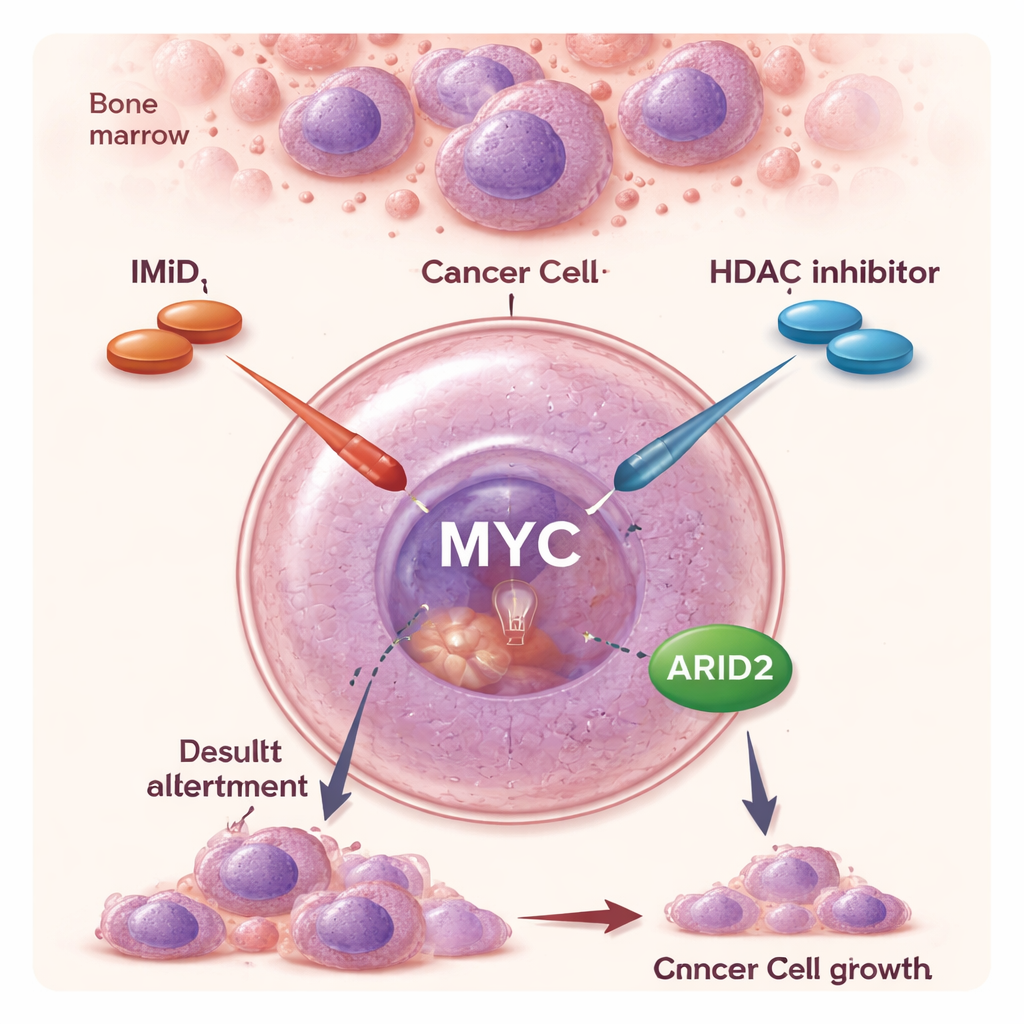
Два старых класса препаратов, одно новое партнерство
За последние два десятилетия IMiD и другие таргетные препараты значительно продлили выживаемость при множественной миеломе. IMiD действуют необычным образом: вместо простого блокирования белка они приводят к тому, что определенные белки помечаются для разрушения, фактически устраняя их из клетки. Это ослабляет ключевые сигналы выживания, от которых зависят клетки миеломы. Ингибиторы HDAC, такие как панобиномистат, работают иначе: они ослабляют плотную упаковку ДНК и тем самым в широких чертах меняют, какие гены включены или выключены. Как отдельные агенты, ингибиторы HDAC оказывают умеренное действие и могут вызывать побочные эффекты, но клинические испытания указывали на то, что их сочетание с IMiD дает гораздо более сильный противоопухолевый эффект, в том числе у пациентов, чья болезнь перестала отвечать на IMiD. Молекулярная причина этой синергии, однако, оставалась неясной.
Общий уязвимый узел: подавление MYC
Исследователи систематически проверяли комбинации нескольких IMiD с различными ингибиторами HDAC на панели клеточных линий миеломы, используя стандартизированную шкалу, чтобы оценить, насколько сильнее работают комбинации по сравнению с каждым препаратом в отдельности. Они обнаружили, что помалидомид в сочетании с панобиномистатом демонстрирует особенно сильную синергию в большинстве моделей, и что этот эффект зависит от белка церебролона, через которого IMiD направляют свои «мишени» на разрушение. Анализ глобальной активности генов показал, что панобиномистат и связанный с ним широкодейственный ингибитор HDAC сильно выключали MYC — мастер‑ген роста, часто описываемый как «онкогенный двигатель» в раковых клетках — и что IMiD оказывали дополнительное давление на тот же узел. Когда ученые принудительно заставили клетки миеломы продолжать экспрессировать MYC из источника, нечувствительного к препаратам, мощный эффект пары препаратов в значительной степени исчезал, что показало: подавление MYC является ключевым для их сотрудничества.
Взлом резистентности через альтернативный путь
Некоторые клетки миеломы изначально устойчивы к IMiD: хотя ожидаемые ранние мишени и разрушаются, MYC и другие сигналы выживания не подвергаются должному подавлению, и клетки продолжают расти. В одной такой резистентной модели стандартный путь IMiD, связывающий ранние мишени с MYC, был «разомкнут». Команда задалась вопросом, существует ли альтернативный маршрут, который все еще связывал бы IMiD с MYC. Они сосредоточились на ARID2, компоненте большого комплекса ремоделирования хроматина SWI/SNF. Предыдущие работы показали, что помалидомид может помечать ARID2 для разрушения и что это способствует снижению MYC. В резистентных клетках помалидомид в одиночку лишь умеренно сокращал ARID2, отчасти потому, что клетка повышала производство ARID2 в ответ. При добавлении панобиномистата подавлялся сам ген ARID2, что преодолевало этот петлевой механизм обратной связи. Вдвоем оба препарата резко снижали уровень белка ARID2, а затем и MYC, приводя к мощному уничтожению раковых клеток даже в линиях, устойчивых к IMiD.
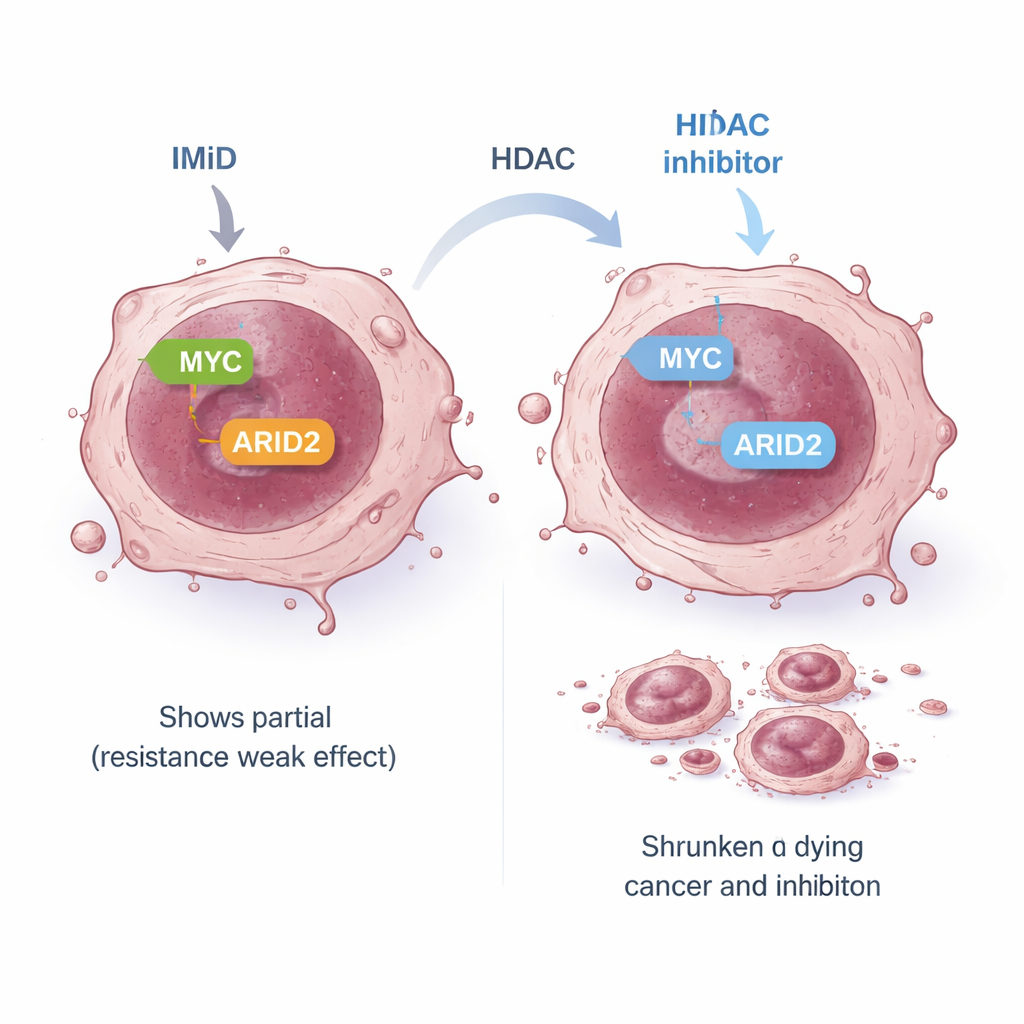
Выявление более широкой уязвимости в раковых клетках
Поскольку ARID2 — лишь один компонент комплекса SWI/SNF, авторы задумались, не является ли весь комплекс терапевтической слабостью. Они обнаружили, что ингибиторы HDAC понижают уровни нескольких компонентов SWI/SNF, а отдельное малое молекулярное соединение, нацеленное на блокирование основных «двигателей» комплекса (BRG1/BRM), само по себе замедляло рост клеток миеломы и снижало MYC. Важно, что этот ингибитор SWI/SNF также проявлял синергию с помалидомидом и панобиномистатом, а комбинация из трех препаратов еще сильнее снижала ARID2 и MYC и решительно подавляла пролиферацию клеток. Изучая, какие конкретные изоформы HDAC вовлечены, исследователи выделили HDAC1 как ключевой фактор, помогающий поддерживать путь ARID2–MYC, тогда как другие HDAC, по-видимому, влияют на MYC через параллельные механизмы.
Что это означает для будущего лечения миеломы
Для неспециалистов основной вывод таков: клетки миеломы, по-видимому, опираются на общий «узел контроля роста», сосредоточенный вокруг MYC, и в этот узел ведет более чем одна дорога. Стандартная терапия IMiD главным образом ударяет по одной дороге; в некоторых резистентных опухолях эта дорога заблокирована, и MYC остается активным. Это исследование показывает, что альтернативная дорога — через ARID2 и комплекс SWI/SNF — остается открытой, и что использование панобиномистата вместе с помалидомидом может ее закрыть. Целенаправленное сочетание препаратов, оказывающих давление на MYC с нескольких сторон, может помочь преодолеть некоторые формы врожденной лекарственной резистентности и, возможно, позволить применять более низкие дозы каждого лекарства. Хотя необходимы дальнейшие доклинические и клинические исследования, результаты дают более ясную схему для разработки умных, основанных на механизмах комбинированных терапий для пациентов с трудноизлечимой множественной миеломой.
Цитирование: Yamamoto, J., Asatsuma-Okumura, T., Ito, T. et al. Synergistic targeting of the ARID2–MYC axis by pomalidomide and panobinostat overcomes intrinsic IMiD resistance in multiple myeloma. Sci Rep 16, 7375 (2026). https://doi.org/10.1038/s41598-026-37740-3
Ключевые слова: множественная миелома, лекарственная резистентность, помалидомид, панобиномистат, MYC