Clear Sky Science · ru
Автономное планирование траектории для межреберной роботизированной ультразвуковой визуализации с использованием обучения с подкреплением
Роботы помогают врачам «видеть» через рёбра
Когда врачи используют ультразвук для наблюдения за такими органами, как печень или сердце, рёбра часто мешают, отбрасывая тёмные тени, которые скрывают важные детали. Получение чёткого изображения во многом зависит от навыков и опыта человека, держащего датчик. В этом исследовании изучается, как робот под управлением искусственного интеллекта может автоматически планировать путь сканирования между рёбрами так, чтобы опухоли и другие цели были видны ясно и стабильно, независимо от оператора.
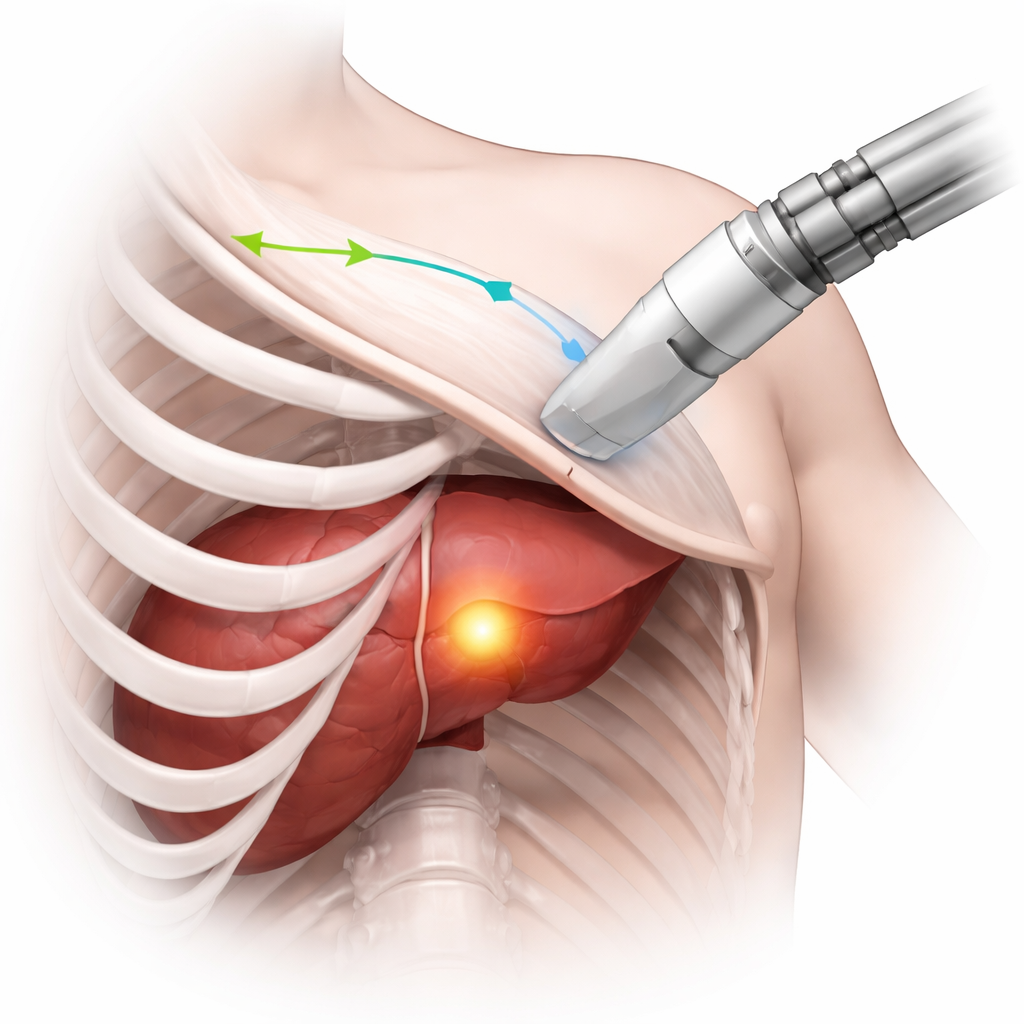
Почему видеть между рёбрами так трудно
Ультразвук популярен, потому что он безопасен, доступен и даёт изображения в реальном времени. Но чтобы визуализировать органы, расположенные за грудной клеткой, датчик нужно аккуратно направлять через узкие интервалы между рёбрами. Если звуковые волны ударяются о кость, они блокируются, создавая большие чёрные участки на изображении, где ничего не видно. Операторы учатся, в ходе тренировок и практики, как наклонять и перемещать датчик, чтобы избегать этих теней, одновременно сохраняя интересующую область в поле зрения. Это особенно важно в процедурах, таких как абляция опухолей печени, когда хирурги должны многократно проверять, что вся опухоль обработана. Задача состоит в том, чтобы превратить этот деликатный трёхмерный навык в то, что робот сможет выполнять самостоятельно.
Обучение робота на виртуальных пациентах
Вместо того чтобы учиться напрямую на шумных и изменчивых ультразвуковых изображениях, исследователи создали виртуальную тренировочную среду на базе компьютерных томограмм (КТ). КТ даёт чёткую трёхмерную карту костей, кожи и печени; опухоли можно добавлять с разными формами и расположением, создавая множество реалистичных сценариев. В этом симуляторе виртуальный ультразвуковой датчик перемещается по поверхности кожи над рёбрами, а пути ультразвуковых лучей моделируются как лучи, проходящие через мягкие ткани и блокируемые костью. Эта простая, но реалистичная модель сообщает системе, какие части опухоли видны, насколько ослаблен сигнал при прохождении и где появляются тени.
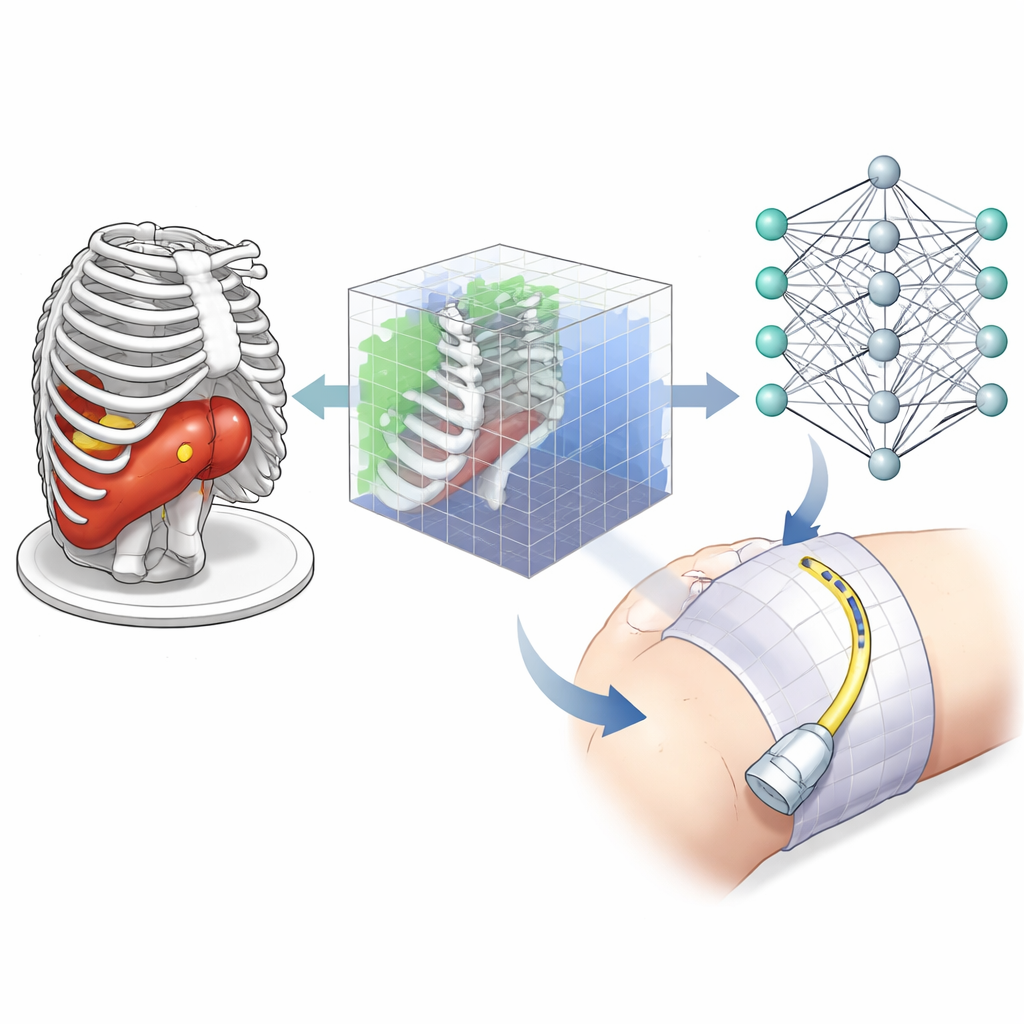
Как система обучения решает, где сканировать
Команда использовала форму искусственного интеллекта, называемую обучением с подкреплением, где «агент» методом проб и ошибок учится выбирать действия, приводящие к более высоким вознаграждениям. На каждом шаге агент видит компактное 3D-представление сцены вокруг опухоли: какие маленькие объёмы содержат опухолевую ткань, какие — кость, и какие пересекаются моделируемыми ультразвуковыми лучами. Затем он может перемещать или наклонять виртуальный датчик малыми приращениями либо переключаться между режимами «исследование» и «запись», используемыми для построения итогового 3D‑изображения. Вознаграждение складывается из трёх целей: покрыть как можно большую часть объёма цели, держать датчик достаточно близко, чтобы уменьшить потерю сигнала, и избегать областей, где лучи блокируются костью, что привело бы к бесполезным затемнённым изображениям.
Испытание метода
Чтобы проверить, обобщается ли выученная стратегия за пределы тренировочных примеров, исследователи протестировали её на новых КТ‑сканах и новых формах опухолей, с которыми агент ранее не сталкивался. В этих испытаниях план сканирования считался успешным, если по крайней мере 95% объёма цели было визуализировано в ограниченном числе шагов. Для маленьких, средних и больших целей система достигала коэффициентов успеха до 95%, при этом обеспечивая высокий процент изображений без теней и разумные расстояния между датчиком и опухолью. Метод также работал при наличии множества целей, например при распределённых остаточных очагах опухоли в печени, хотя производительность естественно несколько снижалась по мере усложнения задачи.
От симуляции к операционной
Пока работа сосредоточена на планировании траектории, а не на физическом перемещении настоящего робота. Траектории генерируются на основе КТ‑сканов конкретного пациента либо на основе общих КТ‑«атласов», которые затем можно сопоставить с анатомией пациента с помощью существующих методов регистрации. В будущем этот модуль планирования планируется сочетать с управлением роботом, компенсацией движений при дыхании и более реалистичной симуляцией ультразвуковых изображений. Для неспециалиста ключевой вывод таков: этот подход может сделать ультразвуковой мониторинг во время процедур, таких как лечение опухолей печени, более надёжным и менее зависимым от мастерства оператора, позволив роботу находить оптимальные, безтеневые маршруты между рёбрами, чтобы держать всю цель в поле зрения.
Цитирование: Bi, Y., Qian, C., Zhang, Z. et al. Autonomous path planning for intercostal robotic ultrasound imaging using reinforcement learning. Sci Rep 16, 6356 (2026). https://doi.org/10.1038/s41598-026-37702-9
Ключевые слова: роботизированный ультразвук, обучение с подкреплением, визуализация опухолей печени, межреберное сканирование, медицинская робототехника