Clear Sky Science · ru
Классификация глиом по липидному метаболизму
Почему жиры в опухолях мозга важны
Опухоли мозга, называемые глиомами, входят в число самых опасных видов рака, однако пациенты с внешне одинаковым диагнозом могут иметь очень разные исходы. В этом исследовании поставлен кажущийся простым, но крайне значимый вопрос: как способы использования опухолью жиров — липидов организма — влияют на её агрессивность, реакцию на лечение и возможно ли увидеть эти различия на стандартных снимках мозга? Проследив пути использования липидов в сотнях опухолей, авторы выявляют скрытые подтипы глиом, которые могут изменить прогнозирование и подходы к терапии.
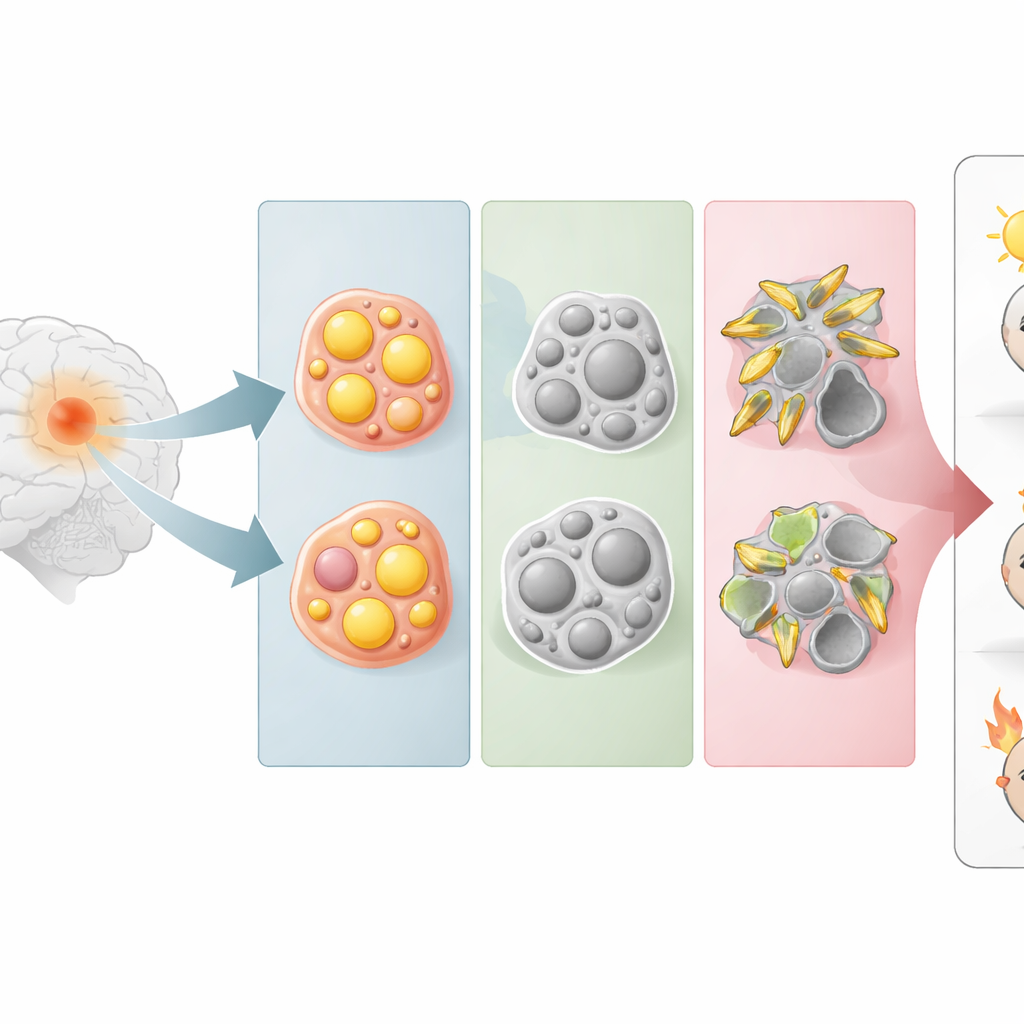
Три скрытых лица одной и той же опухоли
Вместо того чтобы исходить из того, как клетки опухоли выглядят под микроскопом, исследователи сгруппировали глиомы по степени активации пяти основных липидных путей, включая метаболизм стероидных липидов, триглицеридов и сфинголипидов (ключевых компонентов клеточных мембран). Используя профили активности генов из крупных общедоступных баз данных опухолей, они обнаружили, что глиомы естественным образом делятся на три группы. Одна группа опиралась преимущественно на метаболизм стероидов (ST-тип), другая — на метаболизм триглицеридов (TC-тип), а третья — на метаболизм сфинголипидов (SP-тип). Эти метаболические группы пересекают классические категории опухолей, показывая, что клетки с похожими липидными привычками встречаются в опухолях с различным внешним видом.
От метаболизма к прогнозу для пациента
Далее команда выясняла, как эти три стиля использования жиров соотносятся с реальными исходами. Пациенты с опухолями ST-типа в целом жили дольше: их опухоли чаще были низкой степени злокачественности и несли хорошо известные благоприятные генетические изменения. На другом полюсе располагались опухоли SP-типа — обычно высокоэнергетичные глиобластомы без защитных мутаций и чаще встречающиеся у пожилых пациентов. Даже после статистической коррекции на степень злокачественности и ключевые генетические маркеры принадлежность к SP-типу по-прежнему предсказывала значительно худший исход, что указывает на то, что обработка сфинголипидов опухолью отражает независимую меру угрозы, которую стандартные тесты не фиксируют.
Враждебное окружение внутри мозга
Углубившись, авторы изучили микроокружение опухоли — сочетание иммунных клеток, кровеносных сосудов и опорной ткани вокруг рака. Опухоли SP-типа демонстрировали перегруженный и конфликтный иммунный ландшафт: одновременно присутствовали и клетки, нацеленные на атаку, и иммунные подавляющие элементы, а также выраженные сигналы, тормозящие эффективный противоопухолевый ответ. Пути, связанные с быстрым делением клеток, инвазией, неоваскуляризацией, фиброзом и воспалением, были более активны в этом подтипе. Оценки чувствительности опухолей к облучению указывали, что SP-типы наиболее устойчивы к радиотерапии, что согласуется с их худшей выживаемостью. Напротив, опухоли ST-типа выглядели более «спокойными», с более низкими уровнями этих агрессивных признаков.
Чтение метаболизма опухоли по МРТ
Поскольку хирургическое удаление ткани опухоли инвазивно и не всегда возможно, исследователи изучили, может ли стандартная магнитно‑резонансная томография (МРТ) подсказать о липидном поведении опухоли. Они извлекли более двух тысяч тонких текстурных и формальных признаков из двух распространённых МРТ‑последовательностей и обучили модель машинного обучения отличать SP‑тип от всех остальных опухолей. Модель показала хорошую работу как на госпитальной тренировочной выборке, так и на независимой публичной валидационной выборке, значительно реже ошибаясь, чем случайное разделение. Это свидетельствует о том, что метаболический отпечаток особенно агрессивного подтипа глиомы оставляет обнаружимый след на рутинных снимках мозга.
Ключевой ген в центре агрессивной сети
Чтобы перейти от широких путей к конкретным мишеням, команда искала гены, центральные в липидных сетях, сильно сверхактивные в опухолях SP-типа, связанные с худшей выживаемостью и точные в различении SP-типа от других. Три гена — GLA, GLB1 и HSD3B7 — соответствовали всем критериям. Все они были более активны в SP‑типных глиомах и вместе составляли мощную диагностическую подпись. Авторы уделили особое внимание HSD3B7, роль которого в опухолях мозга ранее была мало изучена. Окрашивание тканей от 100 пациентов с глиомой показало, что белок HSD3B7 повышен в более развитых и более злокачественных опухолях, а пациенты с высокими уровнями этого белка жили значительно меньше.
Как один липидный ген перестраивает экосистему опухоли
Анализы на уровне отдельных клеток, которые профилируют отдельные клетки внутри опухолей, показали, что HSD3B7 активен не только в раковых клетках, но и в нескольких типах иммунных и опорных клеток. Высокая экспрессия этого гена ассоциировалась с сетью сигналов, способствующих росту сосудов, хроническому воспалению и уклонению от иммунного ответа. Между определёнными защитными типами клеток наблюдалось ослабление коммуникации, тогда как внутри клеток, поддерживающих опухоль, усиливались самоподдерживающие петли. Вместе эти паттерны указывают на то, что повышенная активность HSD3B7 способствует созданию и поддержанию враждебного микроокружения, благоприятствующего росту опухоли и её устойчивости к лечению.
Что это значит для пациентов и дальнейшей помощи
Практически это исследование показывает, что глиомы можно содержательно разделить на три липидно‑обусловленных подтипа, при этом сфинголипидно насыщенный SP‑тип выделяется как особенно опасный и нечувствительный к терапии. Эти различия не только академичны: их можно считывать по рутинным МРТ‑снимкам с помощью продвинутого анализа изображений и свести к конкретным генам, таким как HSD3B7, которые могут стать будущими мишенями для лекарств. Хотя нужны дополнительные экспериментальные исследования, чтобы проверить, замедлит ли блокирование этих липидных путей рост опухоли или повысит эффективность радиотерапии, работа открывает новую метаболическую призму для понимания рака мозга и приближает поле к более персонализированным, биологически обоснованным решениям в лечении.
Цитирование: Tu, S., Zhang, P., Chi, X. et al. Lipid metabolism classification of gliomas. Sci Rep 16, 8219 (2026). https://doi.org/10.1038/s41598-026-37697-3
Ключевые слова: глиома, липидный метаболизм, визуализация опухолей мозга, радиомика, микроокружение опухоли